Clear Sky Science · tr
Akciğer epitel progenitörlerine doğru anterior önbağırsak endodermin in silico modellenmesi
Kök Hücreleri Akciğer Oluşturan Hücrelere Dönüştürmek
Bilim insanları, bir hastanın kendi kök hücrelerini onarıcı akciğer dokusuna dönüştürmeyi öğreniyor; bu, bir gün KOAH, fibrozis veya ağır enfeksiyonlar gibi hastalıkların yol açtığı hasarı onarabilir. Bu makale, araştırmacıların bilgisayar modellemesi kullanarak bu yolculuktaki önemli bir adımı nasıl haritalayıp ince ayar yaptıklarını inceliyor: anterior önbağırsak endoderm adı verilen ara bir hücre tipini, hava yolları ve akciğer keseciklerini (alveoller) sonunda oluşturabilecek erken akciğer epitel progenitörlerine dönüştürmek.
Akciğer Başlangıç Hücrelerinin Önemi
İnsan uyarmalı pluripotent kök hücreler (iPSC'ler) erişkin dokulardan yeniden programlanabilir ve ardından birçok farklı organ yönünde yönlendirilebilir. Akciğer dokusu oluşturmak için bu hücreler önce birkaç gelişimsel ara noktadan geçer. Bunlardan biri, embriyoda normalde solunum ve sindirim sistemlerinin bazı kısımlarını veren anterior önbağırsak endodermidir. Doğru kimyasal işaretlerle buradan hücreler akciğer epitel progenitörlerine dönüşebilir; bu hücreler erken akciğer belirteçlerini taşır ve daha sonra özelleşmiş hava yolu veya alveolar hücrelere olgunlaşabilir. Gelecekteki hücre terapileri milyarlarca bu hücreyi gerektireceği için, araştırmacıların verimi güvenilir şekilde artıracak ve farklı hasta hücre hatlarına uyarlanabilecek, laboratuvarda sonu gelmeyen deneme‑yanılma gerektirmeyen yöntemlere ihtiyacı vardır.
Hücre Farklılaşmasının Sanal Bir Versiyonunu Kurmak
Ekip, daha önceki bir matematiksel çerçeveyi genişleterek önbağırsaktan akciğer progenitörlerine bu özgül geçişin, bildiklerine göre, ilk popülasyon düzeyindeki modelini oluşturdu. Hücreleri temsil etmenin iki yolunu değerlendirdiler: yalnızca yaşayan hücrelerin toplam sayısını izleyen basit bir versiyon ve anterior önbağırsak hücreleri ile akciğer progenitörlerini ayrı ayrı takip eden daha ayrıntılı bir versiyon. Her iki durumda da model, besin ve atığı temsil edecek şekilde kültür ortamındaki glukoz ve laktatı da izliyor. Sistem biyolojisi araçlarını kullanarak araştırmacılar, hücrelerin nasıl büyüdüğüne, öldüğüne ve farklılaştığına dair birçok aday denklem kurdular ve ardından tanımlanamaz (identifiability) testleriyle, parametreleri mükemmel veriyle bile belirlenemeyen modelleri ellediler.
Modelle Daha Akıllı Deneyler Tasarlamak
Sadece mevcut verileri uydurmak yerine, araştırmacılar yeni deneylerin nasıl yürütülmesi gerektiğini modelin yönlendirmesine izin verdiler. Model parametrelerini doğru tahmin etmek için hücre sayıları ve besin düzeylerinin ne sıklıkla ölçülmesi gerektiğini, sık örneklemenin maliyeti ve emeğiyle istatistiksel kesinliği dengeleyerek sormak için simüle edilmiş veriler kullandılar. Bu onları pratik bir plana götürdü: glukoz ve laktat için günlük ölçümler ve hücre sayımları için bir ila iki günlük aralıklarla ölçümler; day 10'da kültürün ne kadar sert bölündüğünün (split) ve büyüme ortamının günlük değiştirilip değiştirilmediğinin değiştirildiği dört koşul altında. Ardından bu deneyleri gerçekleştirdiler, toplam hücre popülasyonunu ve akış sitometrisi yoluyla önbağırsak hücreleri olarak kalan veya akciğer progenitörü haline gelen kesimleri ölçtüler.
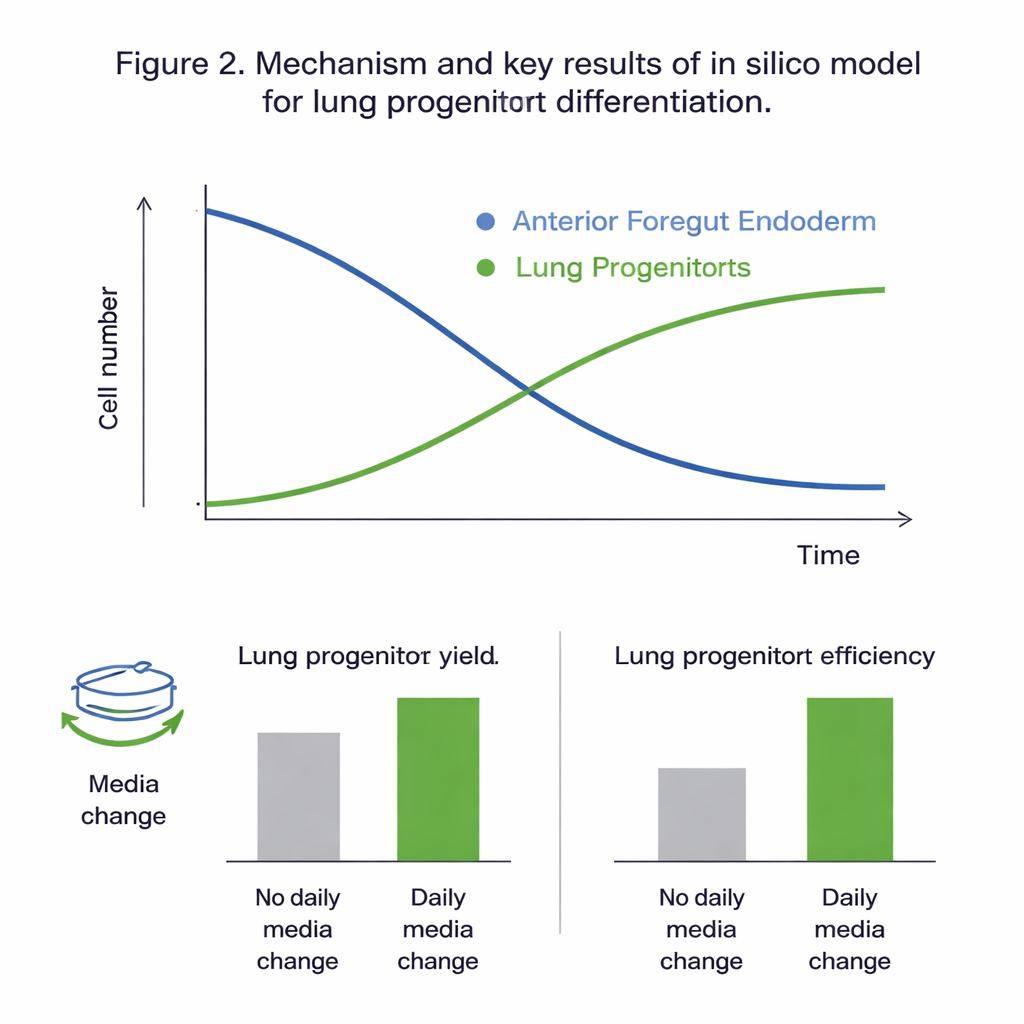
Sanal Deneylerin Ortaya Koydukları
Tüm aday modellerin deneysel verilere uydurulması, önbağırsak ve akciğer progenitör hücrelerini ayrı ayrı izleyen iki popülasyonlu modelin güvenilir şekilde kalibre edilebildiğini ve gözlemlenen davranışı en iyi yakaladığını gösterdi. İstatistiksel kontroller, incelenen zaman aralığında (protokolün 11. ile 15. günleri arasında) dinamiklerin esas olarak önbağırsak hücrelerinin proliferasyonu ve farklılaşması tarafından yönlendirildiğini, akciğer progenitörlerinin kendi proliferasyonunun ise az katkı sağladığını gösterdi. Küresel duyarlılık analizi bu resmi güçlendirerek önbağırsak hücresi büyümesi, ölümü ve farklılaşma hızlarını—ve glukozun etkisini—sonucu kontrol eden ana kollar olarak öne çıkardı. Kalibre edilen model, görülmemiş verileri deneylerin doğal değişkenliğiyle karşılaştırılabilecek hatalarla yeniden üretti; bu da in silico olarak "ya olursa" senaryolarını keşfetmek için yeterince doğru olduğunu gösterdi.
Ortam Değişikliklerini ve Hücre Bölmeyi Optimize Etmek
Güvenilir bir sanal sistemle ekip, iki pratik protokol seçeneğinin sonuçları nasıl etkilediğini test etti: 10. gündeki kültürün ne kadar inceltildiği (split oranı) ve büyüme ortamının her gün değiştirilip değiştirilmediği. Simülasyonlar, günlük ortam değişikliklerinin akciğer progenitör hücrelerinin sayısını ve başlangıç hücresi başına verimi neredeyse iki katına çıkaracağını öngördü; bu esas olarak besin tükenmesini ve atık ile kararsız sinyal moleküllerinin birikimini önlemekle ilişkilendirildi. Deneyler bu öngörülerle yakın uyum gösterdi. Model ayrıca, 10. günde hücrelerin daha seyrek dağıtılmasını sağlayan daha yüksek split oranlarının mutlak hücre sayısını azaltmasına rağmen "girdi hücre başına verimi" yaklaşık dörtte bir oranında artırdığını önerdi. Her iki durumda da bu değişikliklerin kültürdeki akciğer progenitörlerinin nihai oranı üzerinde az etkisi oldu; esas etki, kaç hücrenin verimli şekilde üretilebileceğinin değişmesiydi.
Gelecek Akciğer Terapileri İçin Anlamı
Uzman olmayanlar için ana mesaj, yazarların kök hücrelerden akciğer hücreleri yetiştirmenin kritik bir adımı için bir tür uçuş simülatörü inşa etmiş olmalarıdır. Özenle tasarlanmış deneyleri titiz matematiksel modellemeyle birleştirerek, kültür ortamının ne sıklıkla değiştirileceği ve hücrelerin hangi yoğunlukta ekileceği gibi basit protokol seçimlerinin, hücrelerin kalitesini değiştirmeden akciğer-oluşturan hücrelerin sayısını nasıl dramatik biçimde etkileyebileceğini gösteriyorlar. Bu tür in silico modelleme, gelecekteki protokolleri düzenlemeye, deneysel tahminleri azaltmaya ve nihayetinde araştırma, hastalık modelleme ve sonunda rejeneratif tedaviler için akciğer progenitörlerinin daha güvenilir ve ölçeklenebilir üretimini desteklemeye yardımcı olabilir.
Atıf: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Anahtar kelimeler: akciğer progenitör hücreleri, uyarılmış pluripotent kök hücreler, in silico modelleme, hücre farklılaşması, rejeneratif tıp