Clear Sky Science · tr
Kanserde bağışıklık transkriptomik manzarası ile kopya sayı değişikliklerinin ilişkisi
Kanser immünoterapisi için genlerimiz neden önemli
Kanser immünoterapisi, bağışıklık sisteminin tümörleri tanımasına ve onlara saldırmasına yardımcı olur; ancak kalıcı fayda gören hastalar yalnızca azınlıktadır. Bu çalışma, büyük klinik sonuçları olan temel bir soruyu ele alıyor: tümör hücrelerinin içindeki genetik kaos — özellikle kopya sayı değişiklikleri adı verilen geniş DNA kazançları ve kayıpları — kanser karşısındaki bağışıklık yanıtını nasıl şekillendiriyor ve bu etkileri gen aktivite kalıplarından okuyabilir miyiz?
Kanser verilerine geniş açıdan bakmak
Bunu ele almak için araştırmacılar, tümörlerden ve diğer dokulardan alınmış 294.159 gen aktivite profili gibi devasa bir derlemeyi bir araya getirdiler. Bu profiller, birkaç büyük kamu veritabanından alınmış olup hangi genlerin binlerce örnekte açık ya da kapalı olduğunu gösterir; örnekler birçok kanser türünü ve deneysel durumu kapsar. Bireysel genleri tek tek incelemek yerine ekip, her profili altta yatan “bileşenlere” ayırmak için matematiksel bir yöntem kullandı — birlikte artma ve azalma eğiliminde olan, her biri bir immün yanıt veya DNA değişikliğinin etkisi gibi bir biyolojik süreci yansıtan yinelenen gen kümeleri.
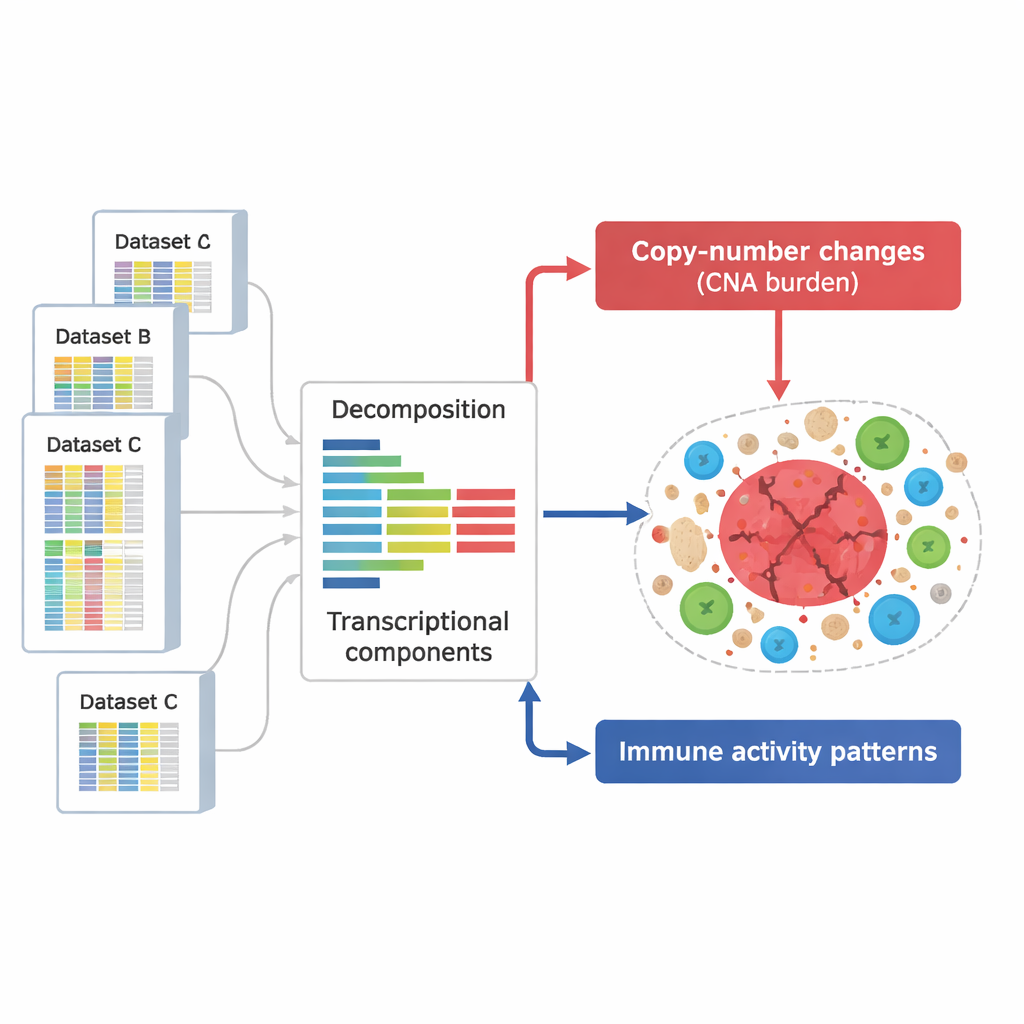
DNA hasar sinyallerini immün sinyallerden ayırmak
Bu bileşenlerden bilim insanları iki ana grup tanımladı. Bir grup, kopya sayı değişikliklerinin etkilerini yakaladı — kanser hücrelerinde tekrar tekrar kazanılan veya kaybedilen kromozom bölgeleri. Bu kalıplar neredeyse tüm genomu kapsıyordu; bu da bu tür değişikliklerden etkilenen bölgelerin çoğunun gen aktivitesi üzerinde tespit edilebilir bir izi bıraktığını gösteriyor. İkinci bir bileşen grubu ise T hücresi aktivasyonu, doğal öldürücü hücre etkinliği ve antijen sunumu gibi immün işlevlerle ilişkili genler bakımından zengindi. Toplamda 657 DNA ilişkili bileşen ve 283 immün ilişkili bileşen tanımlandı; bunların birçoğu bağımsız veri setleri ve teknolojilerde tekrarlanabilir şekilde görülebildi, bu da bunların tümör biyolojisinin sağlam, genel özelliklerini temsil ettiğini düşündürüyor.
Kalıpları tedavi yanıtına bağlamak
Araştırmacılar daha sonra bu immün ilişkili kalıpların immün kontrol noktası inhibitörlerine yanıt veren hastaları tahmin etmeye yardımcı olup olmayacağını sordular; bu ilaçlar kanser immünoterapisinin önemli bir sınıfını oluşturuyor. Yedi kanser türünü kapsayan 1.167 hastayı içeren 13 klinik çalışmadan elde edilen verileri kullanarak, ekip tedavi öncesi tümör örneklerindeki immün bileşenlerin aktivitesi temelinde yalnızca yanıt verenlerle yanıt vermeyenleri ayırt etmek üzere bilgisayar modelleri eğitti. Bazı modeller tamamen bağımsız hasta gruplarında test edildiğinde bile güçlü performans gösterdi; örneğin bir meme kanseri kohortu üzerinde eğitilmiş bir model ayrı bir meme kanseri kohortundaki yanıtları doğru şekilde tahmin etti ve birkaç diğer kanserde de faydalı performans sergiledi. İnterferon yanıtları, doğal öldürücü hücreler ve T hücresi aktivasyonu ile bağlantılı kalıplar dahil olmak üzere küçük bir immün desen seti bu tahminlere en güçlü katkıyı sağladı.
Genetik kaos tümör immünitesini nasıl yeniden şekillendiriyor
Bu çerçeve kurulduktan sonra araştırmacılar, genel kopya sayı değişikliği yükünü — bir tümörün DNA’sının ne ölçüde kazanılıp kaybedildiğinin bir ölçüsü — birçok kanser türünde her bir immün kalıbın aktivitesiyle sistematik olarak ilişkilendirdiler. Çoğu immün kalıp ters bir ilişki gösterdi: yüksek DNA değişikliği yüküne sahip tümörler, antijen sunumu ve kilit immün hücrelerin infiltrasyonu gibi yararlı immün işlevlerle ilişkili bileşenlerin daha düşük aktivitesine eğilimliydi. Ancak dikkat çekici bir azınlık kalıp zıt yönde hareket etti. Yüksek değişiklik yüküne sahip tümörler genellikle düzenleyici T hücreleri ve belirli makrofajlar da dahil olmak üzere immünsüpresif hücre tiplerinden artan sinyaller ve tümör yok etmekten ziyade tümör büyümesini destekleyebilen inflamatuar hücrelerden sinyaller gösteriyordu. Tümör dilimlerinin mekânsal analizleri, yoğun DNA değişikliklerinin olduğu bölgelerin sıklıkla yararlı immün kalıpların düşük aktivitesiyle ve immün hücrelerin tümör kenarlarına sıkıştığı "immün hariçlenmiş" alanlarla çakıştığını doğruladı.
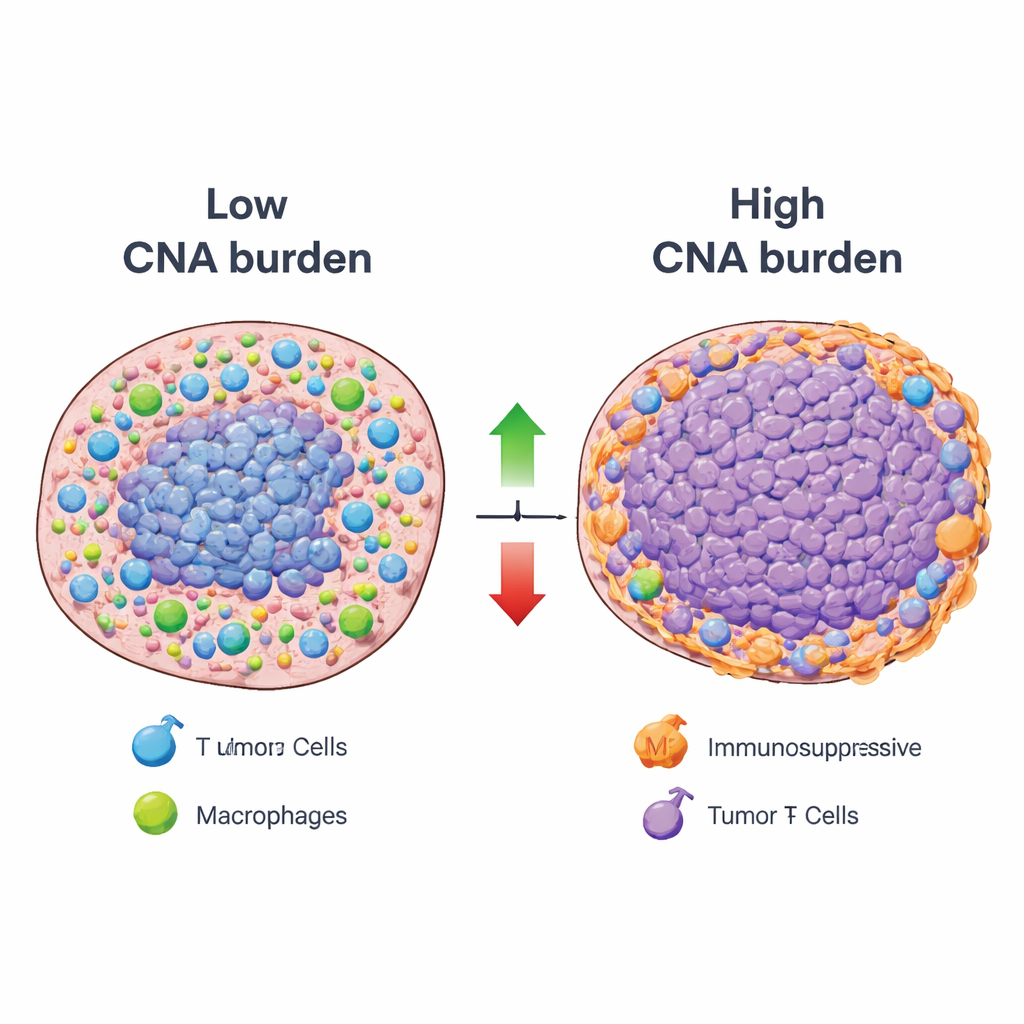
Geleceğin kanser tedavisi için bunun anlamı
Basitçe söylemek gerekirse, çalışma büyük ölçekli DNA kazanımları ve kayıplarıyla yüklü tümörlerin hem yararlı immün yanıtları körelttiğini hem de baskılayıcı veya tümörü destekleyen immün ortamları teşvik ettiğini gösteriyor. Yine de bu tümörler immünolojik olarak sessiz değiller; bunun yerine IL-17 veya IL-23 sinyalini engelleyen ilaçlar gibi hedefe yönelik tedavilere yatkın olabilecek, belirli ve yinelenen immün durumlar sergiliyorlar veya belirli makrofajları yeniden programlama stratejileri düşünülebilir. Bu DNA–immün ilişkilerini kanserler boyunca haritalayarak ve kaynağı kamuya açarak, çalışma bazı genetik olarak kararsız tümörlerin mevcut immünoterapilere neden direnç gösterdiğine dair ayrıntılı bir rehber sunuyor ve bağışıklık sisteminin bu direnci yenmesine yardımcı olacak yeni kombinasyon tedavi stratejilerini öneriyor.
Atıf: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
Anahtar kelimeler: kanser immünoterapisi, kopya sayı değişiklikleri, tümör mikroçevresi, immün kontrol noktası inhibitörleri, transkriptomik