Clear Sky Science · tr
Kompleks mekânsal ortamlarda hücre göç dinamiklerinin simülasyon tabanlı çıkarımı
Bağırışık dokuda bağışıklık hücreleri yollarını nasıl buluyor
Bağışıklık hücrelerimiz sıklıkla enfeksiyon bölgelerine veya lenf düğümlerine ulaşmak için yoğun, labirent benzeri dokulardan sıkışarak geçmek zorunda kalır. Bu çalışma, sonuçları geniş çıkarımlara açık, aldatıcı derecede basit bir soruyu soruyor: bu hücreler böyle dağınık ortamlarda nasıl yön buluyor ve mikroskop verilerinin karışıklığı içinde davranışlarını güvenilir şekilde nasıl çıkarabiliriz? Hassas şekilde mühendislik yapılmış laboratuvar “labirentleri”ni gelişmiş bilgisayar simülasyonları ve modern makine öğrenmesi araçlarıyla birleştirerek yazarlar, karmaşık çevrelerde hücre hareketini yönlendiren kuralları çözmenin yeni bir yolunu gösteriyor.
Bağışıklık hücreleri için küçük bir labirent inşa etmek
Çevrenin hareketi nasıl şekillendirdiğini araştırmak için araştırmacılar dendritik hücrelere odaklandı—çevre dokulardan lenf düğümlerine gitmesi gereken ve kemokin adı verilen kimyasal çekiciler tarafından yönlendirilen bağışıklık nöbetçileri. Silikon kauçuktan (PDMS) yapılmış düzenli aralıklı sütunlardan oluşan düz bir “sütun ormanı” içeren mikroüretimli bir çip inşa ettiler; dar 10 mikrometre aralıklar gerçek dokulardaki sıkışık boşlukları taklit ediyordu. Çipin bir tarafına on binlerce dendritik hücre yüklendi; karşı tarafta ise sütunlar boyunca stabil bir gradyan oluşturan kemokin CCL19 kaynağı vardı. Zaman atlamalı mikroskopi kullanılarak hücre çekirdekleri her 30 saniyede bir izlendi; hücreler kemokin kaynağına doğru hareket etmeye çalışıyordu. 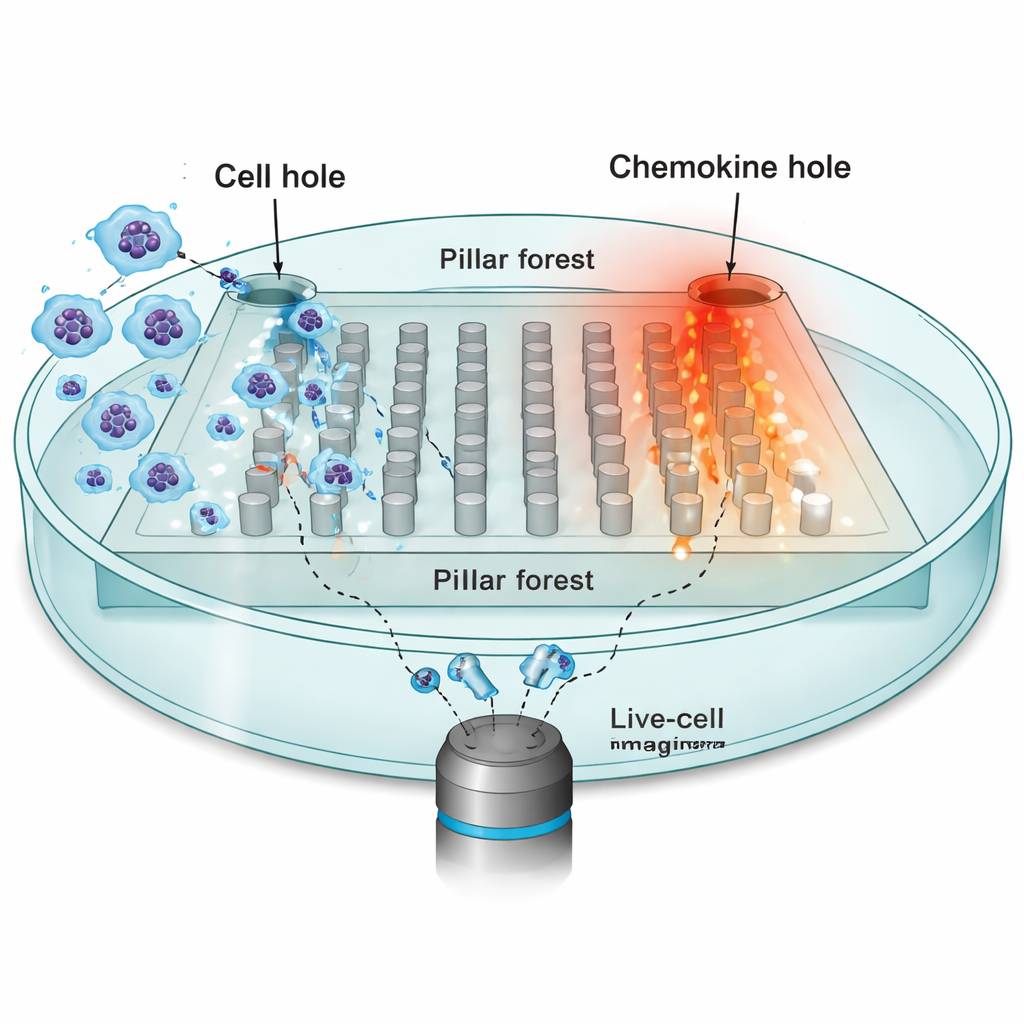
Biyolojiyi sanal bir deneye dönüştürmek
Bu çeşitliliği anlamlandırmak için ekip, Hücresel Potts modeli olarak bilinen bir çerçeve kullanarak hücre göçünün ayrıntılı hesaplama modelini oluşturdu. Bir hücreyi basit bir nokta olarak ele almak yerine bu yaklaşım her hücreyi bir ızgarada uzanmış bir yama olarak temsil eder; bu sayede hücre şekil değiştirebilir, sütunlar arasından sıkışarak geçebilir ve kimyasal sinyallere yanıt verebilir. Model dört ana bileşen içerir: bir hücrenin kemokin gradyanı tarafından ne kadar çekildiği (mdir), mevcut hareket yönünde ne kadar ısrarcı olduğu (mrand), ne sıklıkla yeniden yönlendiği (λ hızı ile yakalanır) ve etkili boyutu (a). Bu parametreleri ayarlayıp simülasyonlar çalıştırarak model, sütun ormanındaki kaydedilmiş hücre yolları ile doğrudan karşılaştırılabilecek sentetik yollar üretir.
Elle seçilmiş ölçümler neden yetersiz kalıyor
Geleneksel olarak araştırmacılar bu tür hareket verilerini birkaç tanıdık istatistikle özetler—bir hücrenin ne kadar yol katettiği (yer değiştirme), ne kadar hızlı hareket ettiği (hız) ve yönünün zaman içinde nasıl değiştiği (dönme açıları). Yazarlar önce bu insan tarafından tasarlanmış özetleri yaklaşık Bayes hesaplaması (ABC) adlı bir teknik içinde kullandılar; bu yöntem benzetim yollarını deneysel olanlara benzeten parametre setlerini arar. Bu özetlerin geniş eğilimleri yakaladığı görüldü, ancak verideki ince yapının çoğunu kaçırdılar. Sonuç olarak rastgele ısrar ve yeniden yönelim zamanlamasını yöneten bazı model parametreleri iyi sınırlanamıyor veya hatta yanlı kalıyordu. Ayrıca, ABC kabul edilebilir uyumlara ulaşmak için yüz binlerce simülasyon ve birçok saatlik hesaplama süresi gerektirdi.
Ağın hangi özelliklerin önemli olduğunu öğrenmesine izin vermek
Bu sınırları aşmak için çalışma, sinirsel olasılık kestirimi (NPE) olarak adlandırılan yeni bir yöntem ailesine yöneldi. Burada bir sinir ağı doğrudan çok sayıda benzetim verisi ile bu verilerin altında yatan parametre çiftleri üzerinde eğitilir. Ağın bir bölümü tüm hücre yolları koleksiyonlarından kendi sıkılaştırılmış “özet özellik” setini otomatik olarak öğrenir; diğer bir bölüm ise bu özelliklerin olası parametre değerlerine nasıl geri eşlendiğini öğrenir. Kritik olarak, bu öğrenilmiş özellikler insan tarafından yorumlanabilirlik yerine doğru parametre çıkarımı için açıkça optimize edilir. Yazarlar daha sonra öğrenilmiş özetleri bir ABC çerçevesi içinde yeniden kullandılar ve ABC'nin dayanıklılığını sinir ağlarının esnekliğiyle birleştiren hibrit bir boru hattı oluşturdular. 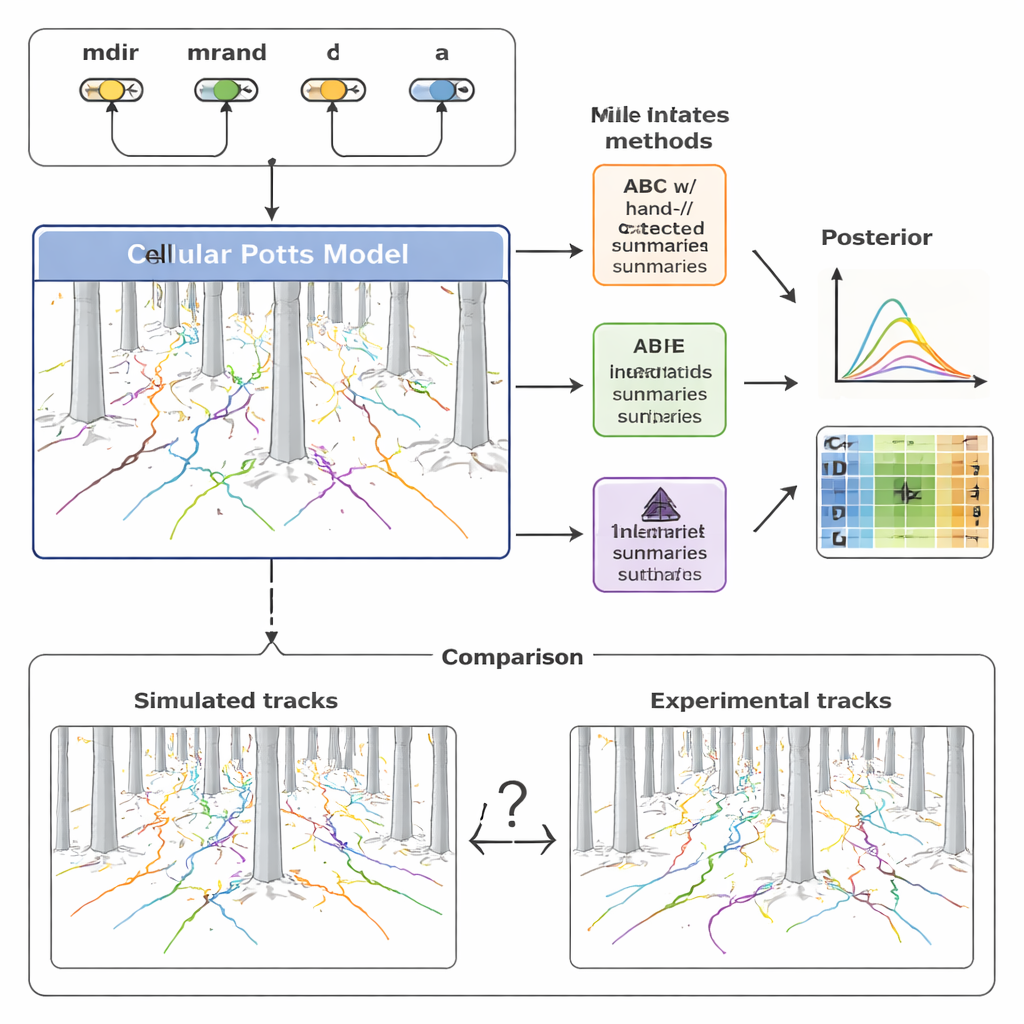
Yeni yaklaşım hücre navigasyonu hakkında neler ortaya koyuyor
Bu kalibre edilmiş modelle donanmış olarak araştırmacılar kemokin sinyallerinin ve fiziksel engellerin birlikte göçü nasıl şekillendirdiğini incelediler. Çıkarılan hücre boyutu, dendritik hücrelerin 10 mikrometre aralıklara uyum sağlamak için etkin olarak küçüldüklerini ve deforme olduklarını öne sürdü; bu, bilinen esneklikleriyle tutarlıdır. Simülasyonlar, kalıcı rastgele hareketin hücrelerin ne kadar geniş yayıldığının başlıca belirleyicilerinden biri olduğunu; hatta kemokin rehberliği olmasa bile bunun önemli olduğunu ve sütun ormanının güçlü yönelimsel ipuçları ve ısrar birlikteliğinde hücreleri hapsedebileceğini gösterdi. Sürpriz bir şekilde model, kısa süreli erken etkin bir kemokin sinyalinin bazı durumlarda sabit bir sinyale kıyasla daha fazla hücrenin hedefe ulaşmasına yardımcı olabileceğini öngörüyor; çünkü uzun süreli çekim hücreleri engeller içinde kaçmak yerine dönmeye devam ettirebilir.
Bunun biyoloji ve modelleme için önemi
Uzman olmayanlar için temel mesaj iki yönlü. Birincisi, dokulardaki bağışıklık hücresi göçü yalnızca kimyasal bir izi takip etmekle ilgili değildir; rehberlik ipuçları, hücrelerin kendi hareket eğilimleri ve çevrelerinin fiziksel düzeni arasındaki ince etkileşimden ortaya çıkar. İkincisi, bu kuralları görüntüleme verilerinden çıkarmak, bilgisayarın veride hangi örüntülerin en bilgilendirici olduğunu öğrenmesine izin vermeyi gerektirir; yalnızca basit, insan tasarımı ölçümlere dayanmak yeterli değildir. Mikro mühendislik deneyleri, şekil çözebilen simülasyonlar ve sinir ağı temelli çıkarımı birleştirerek bu çalışma, birçok hücre tipinin karmaşık ortamlarda nasıl hareket ettiğini incelemek için güçlü bir şablon sunar; uygulama alanları bağışıklık denetimini anlamaktan daha iyi kanser terapileri tasarlamaya kadar uzanabilir.
Atıf: Arruda, J., Alamoudi, E., Mueller, R. et al. Simulation-based inference of cell migration dynamics in complex spatial environments. npj Syst Biol Appl 12, 20 (2026). https://doi.org/10.1038/s41540-026-00648-9
Anahtar kelimeler: hücre göçü, dendritik hücreler, kemokin gradyanları, simülasyon tabanlı çıkarım, mikroakışkan sütun ormanları