Clear Sky Science · tr
Astım aracılı optik glioma büyümesinin T hücresi-mikroglia etkileşimleriyle kontrolü: Bir matematiksel model
Nefes Alma Sorunları Beyin Tümörleriyle Bağlandığında
Astım ile beyin tümörleri birbirinden çok farklı görünür: biri solunumumuzu etkiler, diğeri görme, düşünme ve hareketi etkiler. Yine de hekimler şaşırtıcı bir desen fark etti—astımlı çocukların optik sinirle ilgili belirli beyin tümörlerini geliştirme olasılığı daha düşük görünüyor. Bu makale, kronik bir akciğer hastalığının beklenmedik biçimde beyni nasıl koruyabileceğini araştırıyor; bağışıklık hücreleri ile tümör hücreleri arasındaki gizli kimyasal iletişimi izlemek için matematiksel bir model kullanıyor.
Yavaş Büyüyen Bir Tümör, Yüksek Risk
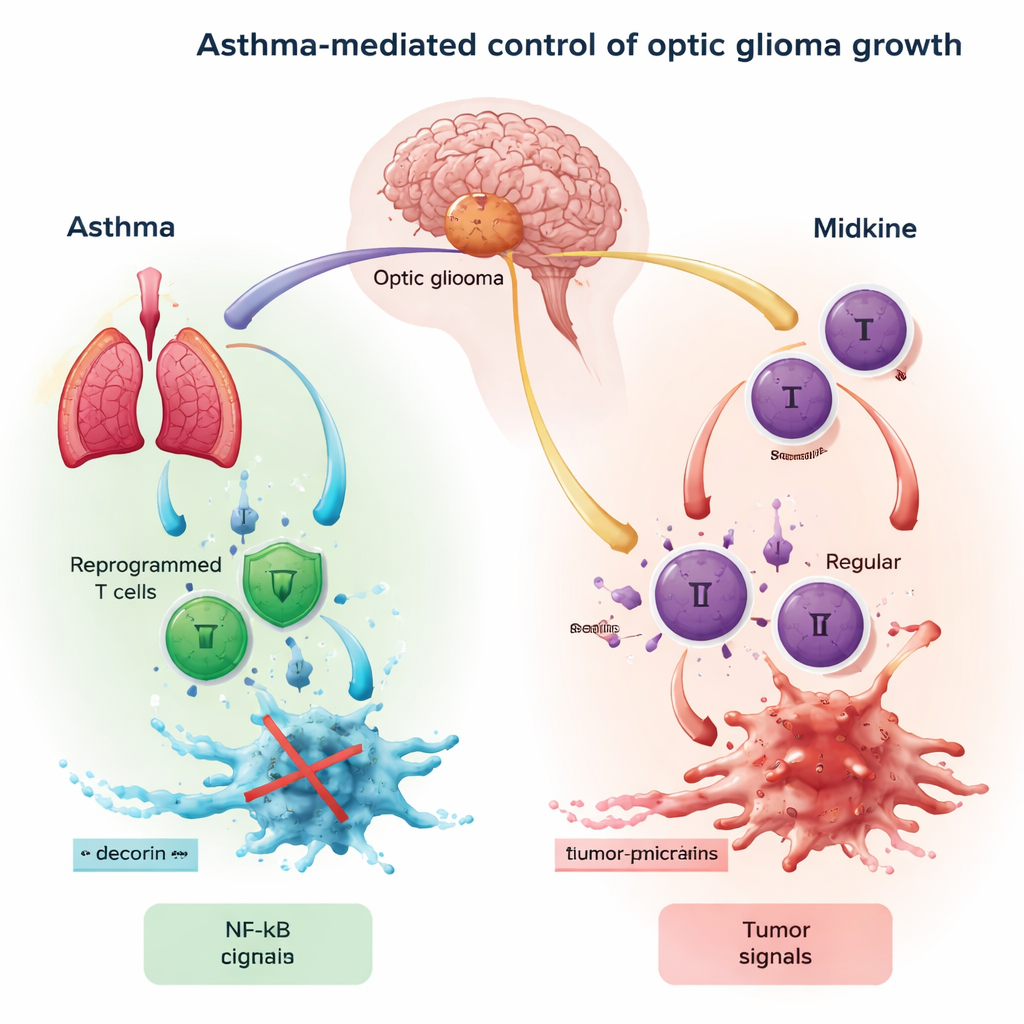
Optik gliomalar genellikle optik sinir boyunca oluşan ve çoğunlukla nörofibromatozis tip 1 (NF1) adlı genetik bir durumla ilişkilendirilen yavaş büyüyen tümörlerdir. Bu tümörler “düşük dereceli” olarak kabul edilse de görme kaybı ve hormonal sorunlara yol açabilirler. NF1’de bozuk bir gen, RAS adlı bir sinyal proteinini aşırı aktif hâle getirir. Bu aşırı aktivite başka bir molekül olan midkine üretimini açar; midkine optik sinirde bir megafon gibi davranarak bağışıklık hücrelerini çağırır ve genellikle tümöre yardım eden şekilde yerel ortamı yeniden şekillendirir.
Sinir ve Bağışıklık Hücreleri Arasında Tümörü Besleyen Bir Konuşma
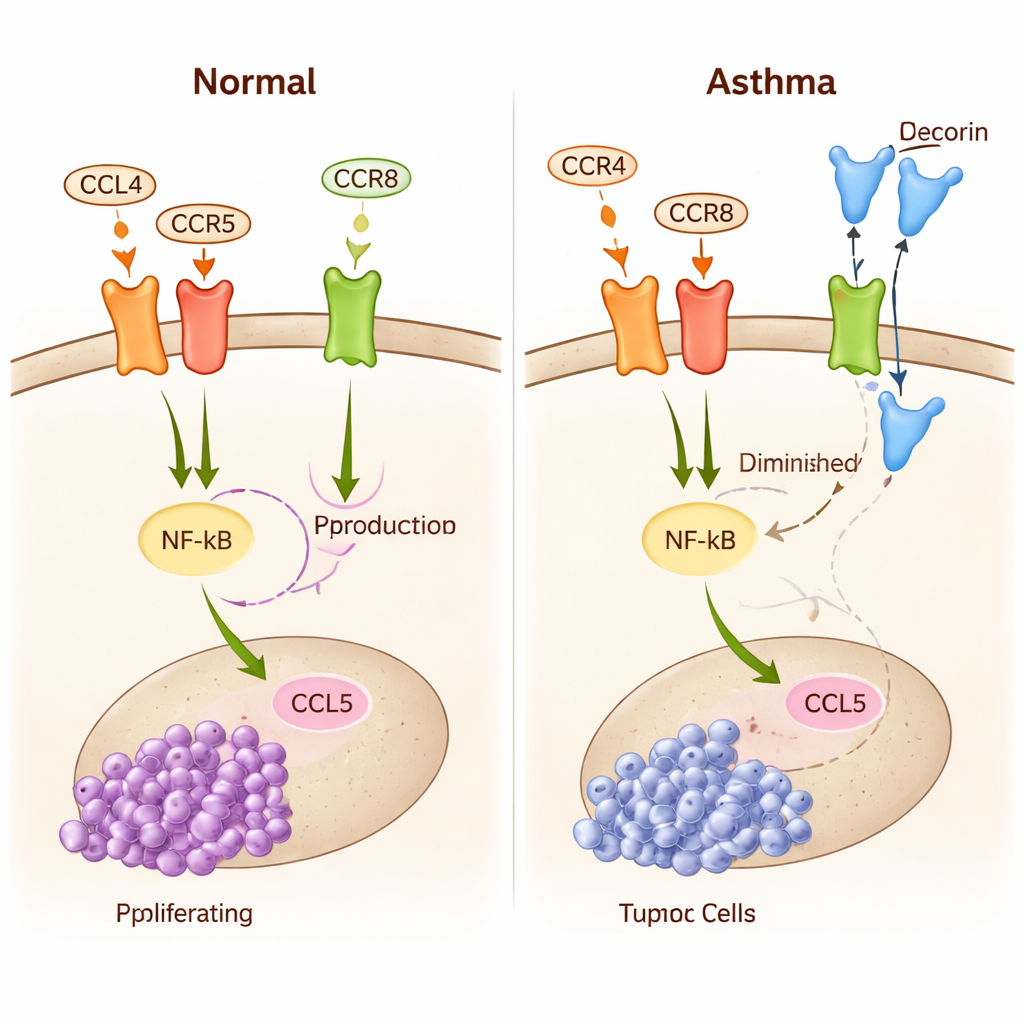
Yazarlar optik sinir, bağışıklık hücreleri ve tümör büyümesi arasında bağlantı kuran bir olay zincirine odaklanıyor. Optik sinirden salınan midkine önce T hücrelerini aktive eder ve bunların CCL4 adlı bir sinyal salgılamasına neden olur. Bu sinyal daha sonra mikroglialardaki (beynin yerleşik bağışıklık hücreleri) CCR5 ve CCR8 reseptörlerine bağlanır. Yeterli miktarda CCL4 bu reseptörlere bağlandığında, mikroglia içindeki NF-κB adlı bir ana anahtarı açar. NF-κB aktifleştiğinde CCL5 adlı başka bir sinyalin üretimini yönlendirir; CCL5 optik glioma hücrelerinin büyümesini, göçünü ve bağışıklıktan kaçışını teşvik eder. Özetle, midkine–CCL4–NF-κB–CCL5 ekseni tümör genişlemesi için döngüsel bir "ileri" sinyali oluşturur.
Astımın T Hücrelerini Tümör Kısıtlayıcılarına Nasıl Yeniden Programladığı
Astım kronik hava yolu inflamasyonu ile bilinir. Ancak astımlı kişilerde bazı T hücreleri "yeniden programlanır": doğrudan hücre öldürme yeteneklerinin bir kısmını yitirirler ve bunun yerine çevrelerini yeniden şekillendiren moleküller salgılarlar. Bu moleküllerden biri, tanımlanmış tümör karşıtı özellikleri olan küçük bir protein olan decorindir. Bu çalışmadaki temel fikir, astım tarafından önceden etkilenmiş T hücrelerinin akciğerden beyne gidip optik glioma çevresinde decorin salgılayabilmesidir. Decorin mikroglialardaki CCR8 reseptörü için CCL4 ile yarışır; bu da tümörü besleyen konuşmanın bir bölümünü etkili biçimde engeller ve mikroglialarda NF-κB ile CCL5 düzeylerini düşürür.
Görünmez Bir Ağı Matematikle İzlemek
Bu sinyal ağı sezgiyle kavranamayacak kadar karmaşık olduğundan, araştırmacılar diferansiyel denklemler kullanarak ayrıntılı bir matematiksel model kurdular. Model kilit moleküllerin (midkine, CCL4, decorin, NF-κB, CCL5) düzeylerini, mikroglialardaki reseptör aktivitesini ve tümör hücrelerinin zaman içindeki büyümesini izliyor. Her etkileşimin gücünü kalibre etmek için deneysel veriler kullandılar ve sonra birçok senaryo simüle ettiler. Model, bağlanma gücündeki küçük değişikliklerin—CCL4 veya decorin’in reseptörlere ne kadar kolay bağlandığı—mikrogliaları iki moda çevirebileceğini gösteriyor: yüksek NF-κB ve CCL5 ile tümörü destekleyen bir durum ve güçlü decorin bağlanması ile zayıf CCL4 sinyalleri içeren tümörü baskılayan bir durum. Decorin’e bağlı reseptörlerin CCL4’e bağlı reseptörlere oranına dayanan basit bir indeks, tümörün büyümeye meyilli mi yoksa duraklamaya mı eğilimli olduğunu doğru şekilde tahmin ediyor.
Daha Akıllı Bağışıklık Temelli Tedaviler Tasarlamak
Astımın neden optik gliomaya karşı koruma sağlayabileceğini açıklamanın ötesinde, model tedavi stratejilerini keşfetmek için kullanıldı. Decorin düzeylerini artıran veya CCL4’ün reseptörlere tutunuşunu zayıflatan tedavilerin tümör büyümesini yavaşlatabileceğini öne sürüyor. Yazarlar, decorin üreten T hücrelerinin tekrarlı infüzyonu veya bu faydalı hücreleri vücut içinde genişletmek için IL-2 gibi bağışıklık mesajcılarının kullanılması gibi yaklaşımları dijital ortamda test ediyorlar. İlginç şekilde simülasyonlar, yalnızca toplam dozun değil tedavilerin zamanlamasının da önemli olduğunu gösteriyor: ılımlı, iyi aralıklı dozlama, mikrogliaları tümörü bastıran durumda tutmayı, daha büyük ama daha seyrek dozlara benzer şekilde etkili biçimde başarabilir ve potansiyel olarak daha az yan etkiyle sonuçlanabilir.
Hastalar ve Aileleri İçin Ne Anlama Geliyor
Uzman olmayanlar için merkezi mesaj şudur: genellikle zararlı görülen astımın kronik inflamasyonu bazen bağışıklık sistemini bazı beyin tümörlerini engelleyecek şekilde yeniden şekillendirebilir. T hücrelerini decorin üreticisi fabrikalara dönüştürerek astım, optik sinirdeki dengeyi tümör dostu bir ortamdan kanser için daha düşmanca bir ortama kaydırıyor gibi görünür. Kimse astımı bir tedavi olarak önermiyor, ancak burada açığa çıkarılan mekanizmalar korunma sağlayan yönlerini taklit eden yeni tedavilere ilham verebilir—özelleştirilmiş T hücre tedavileri veya decorin’in engelleyici etkisini taklit eden ilaçlar kullanarak optik glioma riski taşıyan çocukları korumaya yönelik yaklaşımlar.
Atıf: Lee, D., Lawler, S. & Kim, Y. Asthma-mediated control of optic glioma growth via T cell-microglia interactions: A mathematical model. npj Syst Biol Appl 12, 26 (2026). https://doi.org/10.1038/s41540-026-00647-w
Anahtar kelimeler: optik glioma, astım, decorin, T hücreleri, matematiksel modelleme