Clear Sky Science · tr
Nöronal α‑sinükleinopatisinin düzeltilmesi için mitokondriyal morfoloji düzenleyicilerinin sistematik değerlendirmesi
Beyin Hastalıklarında Minik Enerji Santrallerinin Önemi
Hücresel “enerji santralleri” olan mitokondriler, sinir hücrelerinin hayatta kalması ve bağlantılarının işlev görmesi açısından kritik öneme sahiptir. Parkinson hastalığı gibi beyin bozukluklarında bu küçük yapılar sıklıkla hasarlı veya parçalanmış görünür; ancak hangi değişikliklerin zararlı olduğu ve hangilerini güvenle değiştirebileceğimiz belirsiz kalmıştır. Bu çalışma, Parkinson’a bağlı protein birikimini taklit eden bir laboratuvar modelinde temel mitokondriyal “şekil düzenleyicilerini” sistematik olarak test ediyor ve farklı nöron bölümlerindeki mitokondri morfolojisini ölçmek için yapay zekâ destekli bir araç kullanıyor. Çalışma, Fis1 adlı belirli bir düzenleyiciyi mitokondrileri — ve sinapsları — yeni yan etkilere yol açmadan sağlıklı tutmak için umut verici bir hedef olarak işaret ediyor.
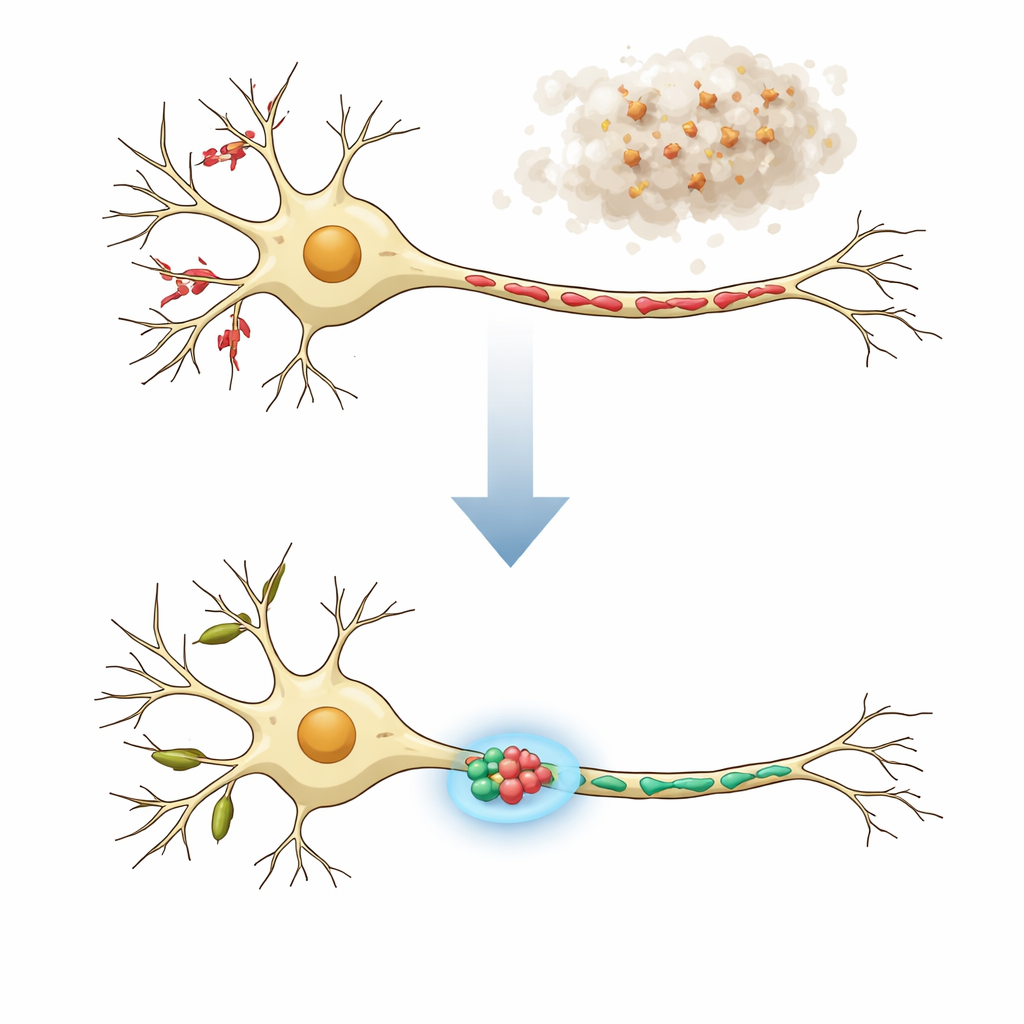
Bir Sinir Hücresinin İki Mahallesi
Nöronlar tek tip değildir: ağaçsı dalları (dendritler) ve uzun kabloları (aksonlar) farklı görevler üstlenir ve çok farklı şekillerde mitokondri barındırır. Sağlıklı sinir hücrelerinde dendritlerde genellikle yerel protein üretimini destekleyen ve dendritik dikenler adı verilen alıcı noktalarındaki esnek iletişimi sağlayan uzun, tübüler mitokondriler bulunur. Sinyal gönderen aksonlarda ise enerji sağlamak ve presinaptik terminallerde kalsiyum düzeylerini kontrol etmeye yardımcı olmak için birçok kısa mitokondri yer alır. Nörodejeneratif hastalıklarda hem mitokondrilerin işlevi hem de yapısı bozulabilir; bu, parçalanma, şişkin şekiller veya boncuklanmış diziler şeklinde ortaya çıkar. Yazarlar, gerçekten etkili tedavilerin dendritlerde ve aksonlarda mitokondrileri bölgeye özgü normal şekillerine geri döndürmesi gerektiği sonucuna vardı.
Parkinson‑Benzeri Bir Stres Testi Kurmak
Parkinson hastalığının ve ilişkili bozuklukların önemli bir özelliğini taklit etmek için araştırmacılar, kültürdeki fare kortikal nöronlarını zararlı agregatlar oluşturabilen bir protein olan alfa‑sinükleinin önceden oluşmuş fibrilleri ile muamele etti. Günler içinde bu fibriller hücrelerde anormal alfa‑sinüklein birikimini başlattı ve hem dendritlerde hem de aksonlarda belirgin mitokondri parçalanmasına yol açtı. MitoVis adlı derin öğrenme görüntü analiz sistemi sayesinde ekip, mikroskop görüntülerinde dendritleri aksonlardan otomatik olarak ayırabildi ve manuel çizime göre yaklaşık on kat daha hızlı biçimde yüzlerce mitokondrinin uzunluğunu, alanını ve şeklini ölçebildi. Bu yüksek verimli yaklaşım, hastalığa benzer koşulun mitokondrileri kısalttığını ve daha yuvarlak hale getirdiğini doğruladı; bulgular hayvan modelleri ve hasta dokuları raporlarıyla örtüşüyor.
Mitokondriyal Şekil Anahtarlarını Test Etmek
Ardından ekip, belirli füzyon ve bölünme (fusion‑fission) proteinlerini yönlendirmenin bu hasarı önleyip önleyemeyeceğini sordu. İki füzyon proteini (Mfn1 ve Mfn2) artırıldığında veya bir bölünme proteini (Mff) baskılandığında dendritik mitokondrilerin alfa‑sinüklein kaynaklı kısalmasından korunması ve dendritik dikenlerin kaybının engellenmesi gözlendi. Ancak aynı müdahaleler aksonlardaki mitokondrileri aşırı uzun hale getirerek daha önceki çalışmalarda sinyal salınımı ve akson dallanması sorunlarıyla ilişkilendirilmişti. Buna karşılık, farklı bir bölünme proteini olan Fis1’in azaltılması, dendritlerde ve aksonlarda mitokondri uzunluğunu aşırı uzamaya yol açmadan neredeyse normal değerlere geri getirdi. Önemli olarak, bu düzenekte Fis1’in azaltılması nöronları öldürmedi ve diğer müdahaleler gibi alfa‑sinüklein stresinde küçülecek olan dendritik diken yoğunluğunu korudu.
Kalsiyum Dengesini Korumak
Aksonlardaki mitokondriler elektriksel aktivite sırasında kalsiyumu tamponlayıp düzenlediği için araştırmacılar şekil değişikliğinin bu hassas dengeyi değiştirip değiştirmediğini test etti. Presinaptik düğümlerdeki mitokondrilere hedeflenmiş floresan bir kalsiyum sensörü kullandılar ve aksonları kısa aksiyon potansiyeli patlamalarıyla uyardılar. Alfa‑sinüklein koşulunda, hafifçe kısalmış aksonal mitokondrilerdeki kalsiyum işleme normalle benzer görünüyordu. Ancak Mfn1 aşırı eksprese edildiğinde veya Mff baskılandığında aksonal mitokondriler uyarı sonrası beklenenden daha fazla kalsiyum emdi. Bu artmış alım presinaptik işlevi bozabilir. Buna karşılık, mitokondri uzunluğunu normale döndüren fakat aşırıya kaçırmayan Fis1 baskılanması, sağlıklı kontrollerle yakından eşleşen mitokondriyal kalsiyum yanıtlarını koruyarak daha az gizli ödün olduğunu düşündürüyor.
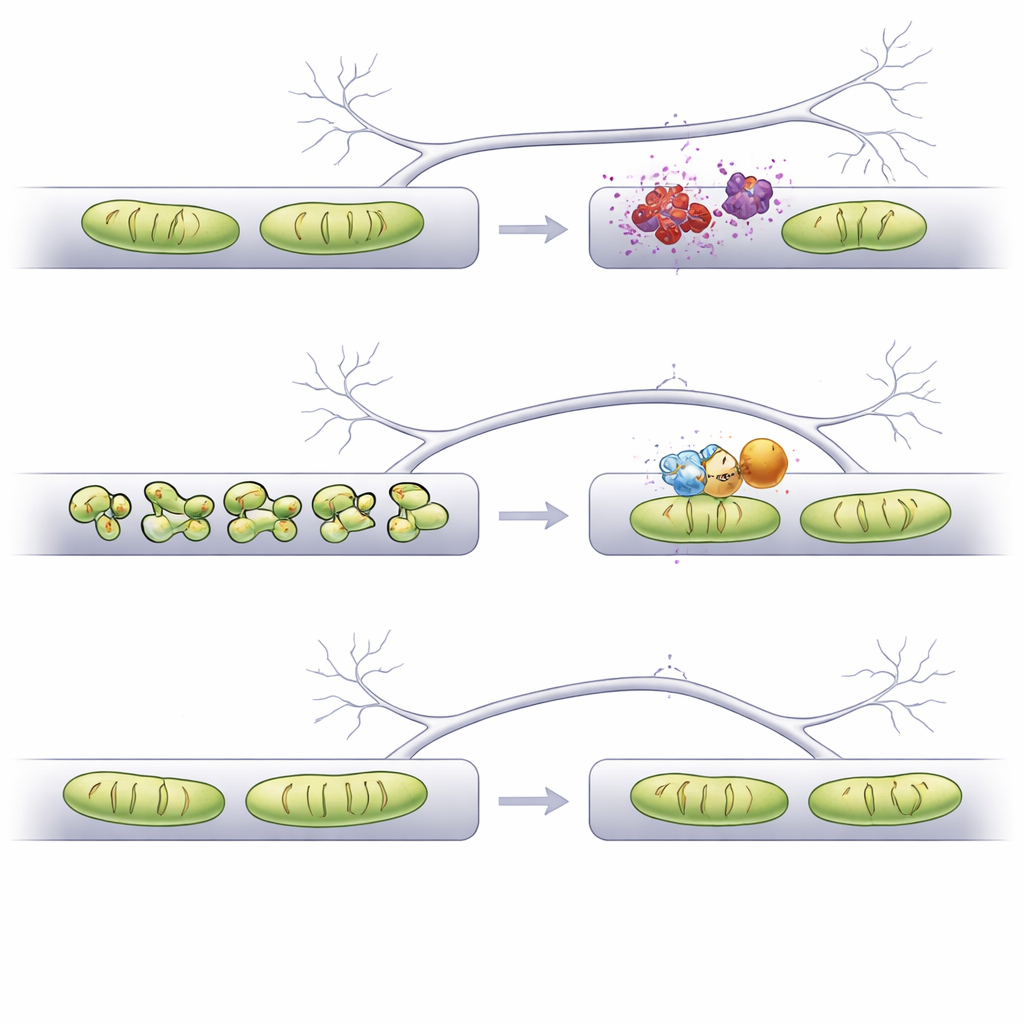
Gelecekteki Tedaviler İçin Anlamı
Bir arada ele alındığında çalışma, mitokondrileri basitçe daha uzun yapmakla yetinmenin yeterli olmadığını — doğru bölgedeki doğru boyuta geri getirmenin anahtar olduğunu gösteriyor. Yapay zekâ destekli bir görüntüleme iş akışı kullanarak yazarlar, Fis1’i özellikle çekici bir hedef olarak tanımlıyor: Fis1’in aşağıya çekilmesi dendritlerde ve aksonlarda mitokondrileri yapısal olarak kararlı tutuyor, dendritik diken kaybını önlüyor ve presinaptik terminallerde anormal kalsiyum işleyişinden kaçınıyor. Bu bulgular, Fis1’e yönelik ilaçlar veya antisens moleküllerle mitokondri şeklinin dikkatle ayarlanmasının, Parkinson ile ilişkili alfa‑sinükleinopatide ve mitokondrilerin bozulduğu diğer beyin hastalıklarında hassas sinapsları korumaya yardımcı olabileceği fikrini destekliyor.
Atıf: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
Anahtar kelimeler: Parkinson hastalığı, mitokondri, alfa‑sinüklein, sinaptik işlev bozukluğu, nörodejenerasyon