Clear Sky Science · tr
Yeni ceramid sentezinin engellenmesi, Parkinson hastalığı fare modelinde alfa-sinüklein patolojisini hafifletiyor
Beyindeki Yağların Parkinson için Neden Önemli Olduğu
Parkinson hastalığı en çok titreyen eller ve yavaşlayan hareketlerle tanınır, ama beynin derinliklerinde daha sessiz bir drama yaşanır. Hareketleri kontrol eden sinir hücreleri, alfa‑sinüklein adı verilen bir proteinin yapışkan kümeler halinde toplanmasıyla yavaşça ölür. Bu çalışma, ceramid adı verilen belirli bir yağ ailesinin bu hasarı tetiklemeye yardımcı olduğunu ve bunların üretimini engellemenin farelerde ve insan hücre modellerinde beyin hücrelerini koruyabileceğini gösteriyor. Çalışma, semptomları hafifletmenin ötesinde Parkinson’u yavaşlatabilecek veya önleyebilecek beklenmedik ve ilaçla hedeflenebilir bir yol haritasına işaret ediyor.
Otopsi Beyinlerinden Gelen İpuçları
Ceramidlerin Parkinson ve ilgili durumlardaki rolünü anlamak için araştırmacılar önce Lewy cisimcikli demansı olan kişilerin otopsi beyin dokusunu inceledi; bu durum Parkinson’da görülen aynı toksik protein kümelerini paylaşır. Hassas kimyasal ölçümler kullanarak, birçok ceramid türünün özellikle uzun yağ kuyruklu formlarının midbrain bölgesinde sağlıklı beyinlere göre belirgin biçimde daha yüksek olduğunu buldular. Ardından insan beyin hücrelerinden alınmış büyük genetik veri setlerini yeniden analiz ederek, ceramidleri üreten ve işleyen genlerin Parkinson hastalarından alınan dopamin üreten nöronlarda ve ayrıca astrositler ve oligodendrositler gibi bazı destek hücrelerinde daha aktif olduğunu keşfettiler. Bu bulgular birlikte, hastalıklı beyinde birkaç hücre tipinde ceramid dengesinin bozulduğunu düşündürüyor.
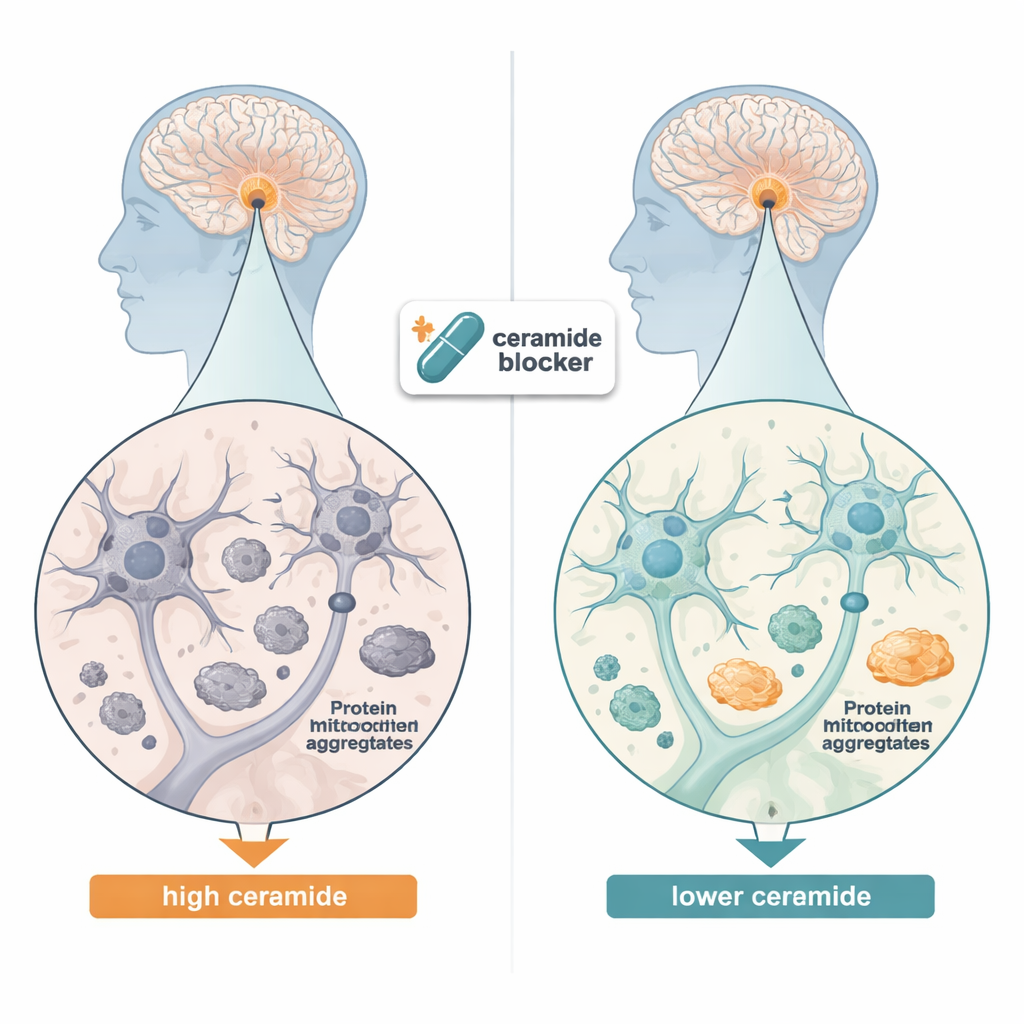
Hücrelerde Protein Kümelerini Temizlemek
Araştırma ekibi bir sonraki adımda ceramid seviyelerinin düşürülmesinin laboratuvarda yetiştirilen sinir benzeri hücrelerde protein birikimini azaltıp azaltmayacağını sordu. Kolayca kümelenen mutant bir alfa‑sinüklein formunu aşırı üreten insan nevroblastoma hücreleri kullandılar. Ceramid üretiminin ilk adımını—ya kritik bir enzim genini susturarak ya da myriocin adlı bir ilaç ekleyerek—kapatınca, çözünmeyen alfa‑sinüklein agregalarının miktarı keskin bir şekilde düştü. Aynı zamanda mitofajinin, yani hücrenin hasarlı mitokondrileri bulup geri dönüştürme sisteminin belirteçleri arttı ve istenmeyen proteinleri imha için etiketleyen makine daha aktif hale geldi. Bu değişimler, aşırı ceramidin normalde hücrenin temizlik ekiplerini engellediğini ve bu lipid yükünün azaltılmasının hücrenin hatalı mitokondrileri ve protein kümelerini daha verimli biçimde temizlemesine izin verdiğini gösteriyor.
Farelerde Beyin Fonksiyonunu Korumak
En kritik sınama, bu stratejinin yaşayan bir beyinde işe yarayıp yaramadığıydı. Araştırmacılar, mutant insan alfa‑sinükleini aşırı üreten ve zamanla hareket problemleri ile hafıza sorunları geliştiren iyi yerleşmiş bir fare modelini kullandılar. Orta yaşta başlayarak bazı farelere birkaç ay boyunca myriocin enjeksiyonları verildi, diğerleri ise zararsız taşıyıcı aldı. Myriocin hayvanların kanında ve midbrain’inde ceramid seviyelerini belirgin biçimde düşürdü. Davranış testleri, tedavi edilen farelerin daha fazla yürüdüğünü ve mekânsal çalışma belleğine dayanan basit bir labirentte daha iyi performans gösterdiğini ortaya koydu. Bu hayvanlardan alınan beyin dilimleri, önemli bölgelerde daha fazla dopamin üreten nöronun hayatta kaldığını ve fosforile olmuş, agregasyon eğilimli alfa‑sinüklein miktarının azaldığını gösterdi. Midbrain’in geniş ölçekli gen ifadesi profillemesi ayrıca myriocin’in inflamatuar yolakları baskıladığını, sinaptik iletişim ve sağlıklı mitokondri bakımıyla ilişkili genleri geri getirdiğini gösterdi.
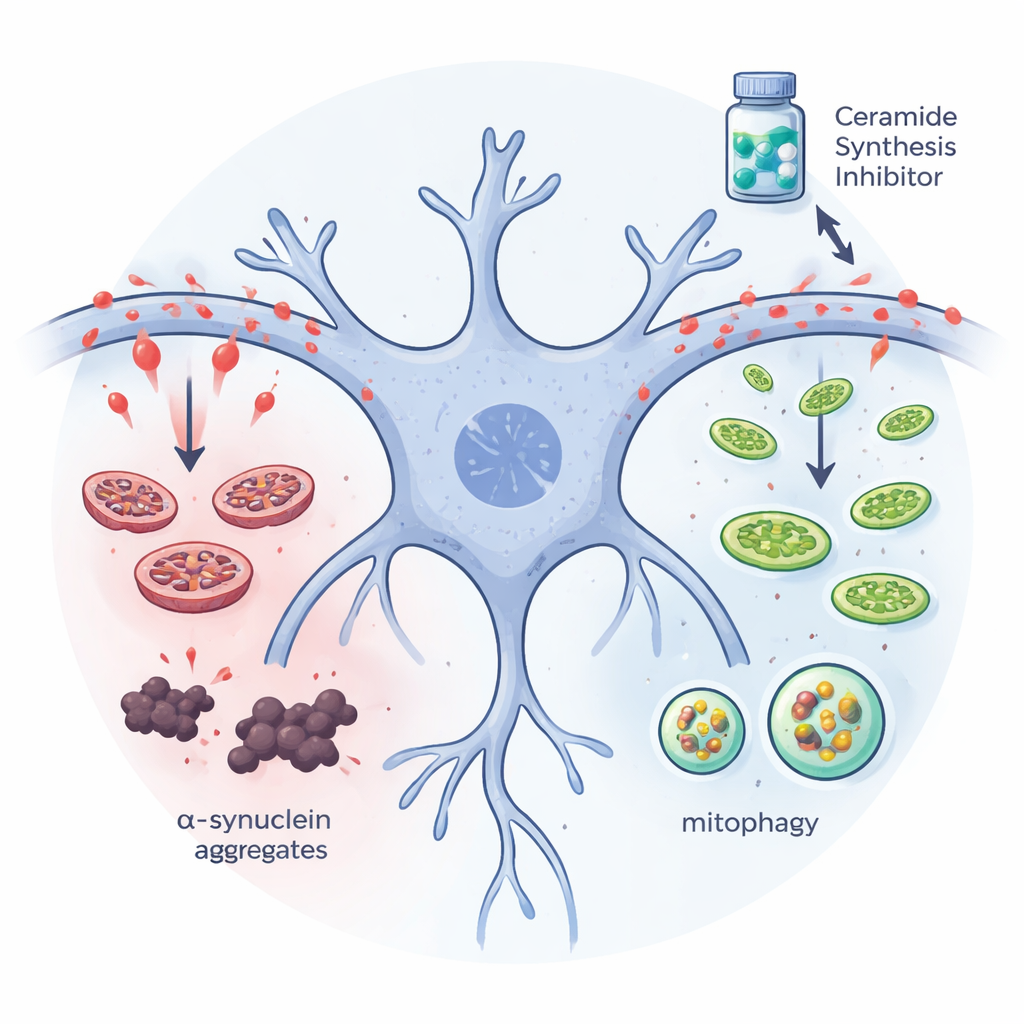
İnsan Nöronları ve Mini‑Beyinler Aynı Şeyi Söylüyor
Sonuçları hastalara daha yakın kılmak için ekip, Parkinson’lu kişilerden türetilmiş indüklenmiş pluripotent kök hücrelerden büyütülmüş nöronlar ve üç boyutlu midbrain organoidleri kullandı. Mitofaji için floresan bir sensör taşıyan hasta kökenli nöronlarda myriocin tedavisi, hasarlı mitokondrilerin hücresel geri dönüşüm merkezlerine taşındığını işaret eden sinyali güçlendirdi ve mitokondri ağının mimarisini iyileştirdi. Midbrain organoidlerinde myriocin, dopamin üreten hücreleri korudu ve zararlı alfa‑sinüklein agregalarını azalttı. Araştırmacılar bu mini‑beyinlere ek ceramid eklediklerinde ise tersine bir etki görüldü: daha fazla protein kümesi oluştu ve dopamin nöronları özellikle Parkinson bağışçılarından elde edilen organoidlerde kaybedildi. Bu deneyler, ceramid birikiminin insanla ilişkili dokuda doğrudan zarar verici bir rolünü destekliyor.
Gelecekteki Tedaviler İçin Anlamı
Uzman olmayanlar için temel mesaj açık: birden fazla Parkinson modelinde, belirli bir beyin yağının fazlalığı hücreleri protein kümeleri, hatalı mitokondriler ve kronik iltihabı teşvik ederek zehirliyor gibi görünüyor. Deneysel ilaç myriocin ile bu yağları yapan ana yolun bloklanması bu sorunları hafifletti, savunmasız nöronları korudu ve farelerde davranışı iyileştirdi; ayrıca insan nöronlarını kültürde kurtardı. Yazarlar, insanlarda uzun dönem güvenlik ve dozlamanın bilinmediğini ve Parkinson’un ceramidlerin ötesinde birçok nedeni olduğunu vurguluyor. Yine de çalışma, tahrip olan dopamin sinyalini yalnızca güçlendirmenin ötesinde yeni bir saldırı hattı açıyor: gelecekteki tedaviler lipid metabolizmasını ve hücresel temizlik mekanizmalarını normalize ederek beyin hücrelerine nörodejenerasyonun yavaş ilerleyişine karşı daha iyi dayanma şansı verebilir.
Atıf: Lee, E., Park, My., Park, M. et al. Inhibition of de novo ceramide synthesis mitigates alpha-synuclein pathology in a Parkinson’s disease mouse model. npj Parkinsons Dis. 12, 49 (2026). https://doi.org/10.1038/s41531-026-01263-5
Anahtar kelimeler: Parkinson hastalığı, ceramid, alfa-sinüklein, mitofaji, nörodejenerasyon