Clear Sky Science · tr
AR-pozitif üçlü-negatif meme kanserlerinde AR inhibisyonu ile radyosensitizasyon mekanizmasını ortaya çıkarmak için transkriptomik analiz
Meme kanseriyle karşılaşan kişiler için bu çalışmanın önemi
Radyoterapi, birçok agresif meme kanseri vakasında tedavinin temel taşlarından biridir, ancak bazı tümörler radyasyonla diğerlerine göre doğal olarak daha zor yok edilir. Bu çalışma, klinik açıdan önemli ve uygulanabilir bir soruyu ele alıyor: prostat kanserinde zaten kullanılan ve erkek hormonu sinyallerini engelleyen bir ilaç sınıfı, üçlü-negatif meme kanserlerinin bir alt türünü radyasyona karşı daha savunmasız hale getirebilir mi — ve bunun bazı vakalarda işe yaramasının ama bazılarında yaramamasının nedeni nedir?
Tedavisi zor bir meme kanseri türü
Üçlü-negatif meme kanserleri, östrojen reseptörleri, progesteron reseptörleri ve HER2 gibi üç ortak moleküler hedeften yoksundur; bu nedenle hastalar genellikle yalnızca cerrahi, kemoterapi ve radyoterapiye dayanmak zorunda kalır. Ancak bu tümörlerin bir kısmı, testosterona benzer hormonlara yanıt veren ve tümör büyümesini yönlendirebilen androjen reseptörü taşır. Önceki çalışmalar, bu reseptörü bloke etmenin bu kanserlerin büyümesini yavaşlatabileceğini ve radyasyon etkisini artırabileceğini gösterdi, fakat bunun nasıl olduğu ve hangi ilaçlar ile tümörlerin en çok fayda gördüğü belirsizdi.
Radyasyonla modern hormon blokerlerinin test edilmesi
Araştırmacılar, esas olarak ne kadar androjen reseptörü taşıdıklarına göre farklılık gösteren birkaç laboratuvar modelinde üçlü-negatif meme kanseri hücrelerini incelediler. İki yeni anti-androjen ilacı olan apalutamid ve darolutamidi odaklandılar ve bu ilaçların kısa süreli uygulamalarını standart X-ışını dozlarıyla birleştirdiler. Yüksek düzeyde androjen reseptörü taşıyan hücrelerde apalutamid, radyasyon hasarını açıkça artırdı ve yeni koloniler oluşturabilen hücre sayısını azalttı. Buna karşılık darolutamid aynı hücrelerde radyasyona duyarlılık üzerinde çok az veya hiç etki göstermedi ve her iki ilaç da androjen reseptörünü çok az ifade eden hücrelerde yardımcı olmadı. Bu bulgular, tüm meme kanserlerinde tüm anti-androjen ilaçların aynı şekilde davranmadığını ve kombinasyonun işe yaraması için tümörün bu reseptöre güçlü şekilde bağımlı olması gerektiğini düşündürüyor.
Hücre içinde bir ana proteinin yer değişimini izlemek
Hormon sinyalleri veya radyasyon sonrası kanser hücrelerinin içinde neler olduğunu anlamak için ekip androjen reseptörünün kendisinin nerede bulunduğunu izledi. Hücreler sentetik bir androjenle uyarıldığında reseptör çekirdeğe, yani genlerin açılıp kapandığı kontrol merkezine geçti. Radyasyon tek başına reseptörü çekirdekten çıkarmadı; aksine tedaviden sonra çekirdekte kaldı ve gen aktivitesini etkilemeye hazır durumdaydı. Bununla birlikte, hücrelere radyasyondan önce anti-androjen ilaç enzalutamid uygulandığında, çekirdekteki reseptör seviyeleri düştü ve daha fazlası hücrenin sitoplazmasında kaldı. Bu durum, reseptörün çekirdeğe girişinin engellenmesinin radyasyon sonrası koruyucu bir gen programının başlatılmasını bozduğu fikrini destekliyor.
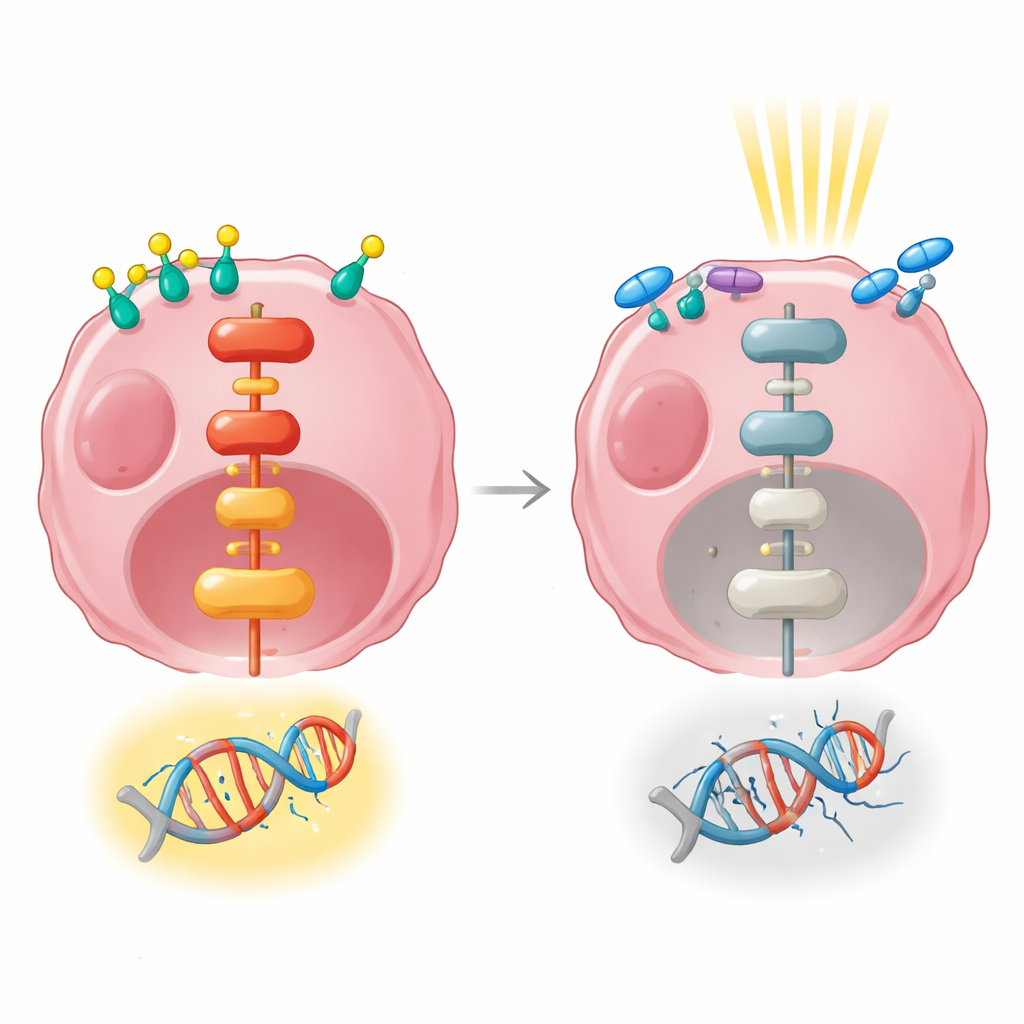
Hormonları dirence bağlayan gen sinyalleri
Araştırmacılar daha sonra RNA dizilemesi kullanarak hormon uyarımı, radyasyon veya her ikisi sonrası hangi genlerin yukarı veya aşağı yönlendirildiğine dair geniş bir anlık görüntü aldılar. Yalnızca hormon tedavisi yüzlerce genin aktivitesini değiştirdi ve hücre büyümesini, yapışmayı ve çevreyle iletişimi yöneten yolakları güçlü şekilde etkiledi. Erken bir zaman noktasında tek başına uygulanan radyasyon ise çok daha az sayıda geni değiştirdi. Hormon uyarımı ve radyasyon birleştirildiğinde, aynı büyümeyle ilgili yolakların birçoğu aktive oldu; bunların arasında hücre yüzeyinden çekirdeğe sinyal ileten ve DNA hasarının onarılmasına yardımcı olduğu bilinen MAPK/ERK adlı önemli bir sinyal yolu da vardı.
DNA’yı koruyan bir hayatta kalma yolunu incelemek
MAPK/ERK sinyal iletimi analizlerde sıkça öne çıktığı için araştırmacılar, bu yolun güçlendirilmesinin androjen blokajının radyasyondaki faydasını geri alıp almayacağını test ettiler. Hücrelere yolak bileşenlerinden biri olan ERK’in sürekli aktif bir versiyonunu fazla ürettirecek şekilde mühendislik yapıp sonra radyasyon artı apalutamid tedavisini tekrarladılar. Bu koşulda apalutamid artık hücreleri radyasyona daha duyarlı hale getirmedi: güçlendirilmiş ERK sinyali hücreleri koruyor gibiydi. Protein ölçümleriyle birlikte bu sonuçlar, androjen reseptörü aktivitesi ile hücrenin radyasyon kaynaklı DNA kırıklarını onarma yeteneği arasında kritik bir bağlantı olarak MAPK/ERK sinyal iletimini işaret ediyor.
Gelecekteki meme kanseri bakımına etkileri
Gündelik ifadeyle, bu çalışma bazı üçlü-negatif meme kanserlerinin radyasyondan kaçınmak için androjenle ilişkili sinyalleri kullanarak hasarlı DNA’yı onarmaya yardımcı olan bir iç hayatta kalma devresini açtığını gösteriyor. Apalutamid ve enzalutamid gibi ilaçlar, androjen reseptörüne güçlü şekilde bağımlı tümörlerde bu devreyi kesebilir ve radyasyonu daha etkili hale getirebilir; oysa reseptör düzeyi düşük veya alternatif hayatta kalma yolları olan tümörler fayda görmeyebilir. Özellikle MAPK/ERK yolunu içeren gen yolaklarının haritalanmasıyla, bu çalışma hormon blokerleri, yolak inhibitörleri ve radyasyonun daha hassas kombinasyonları için zemin hazırlıyor ve bu zor tedavi edilen meme kanseri türündeki hastalar için sonuçları iyileştirme potansiyeli taşıyor.
Atıf: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
Anahtar kelimeler: üçlü-negatif meme kanseri, androjen reseptörü, radyoterapi, radyosensitizasyon, MAPK ERK sinyal iletimi