Clear Sky Science · tr
CXCL10/CXCR3 ekseni, üçlü negatif meme kanserinde immünolojik uykuyu sürdürmek için esastır
Neden bazı kanserler yayılmak yerine uyur
Meme kanseri bazen bir uyuyan ajan gibi davranabilir. İlk tedaviden sonra, birkaç kanser hücresi yıllarca vücutta saklanabilir; görüntülemelerde görülmeyecek kadar büyümezler ama daha sonra uyanıp hayatı tehdit eden metastazlara yol açma potansiyeline sahiptirler. Bu makale, bu “uyku” hali olarak adlandırılan dormansın özellikle agresif bir hastalık biçimi olan üçlü negatif meme kanserinde neden oluştuğunu araştırıyor ve bağışıklık sisteminin bu hücreleri kontrol altında tutmasına yardımcı olan kimyasal bir sinyali ortaya koyuyor.
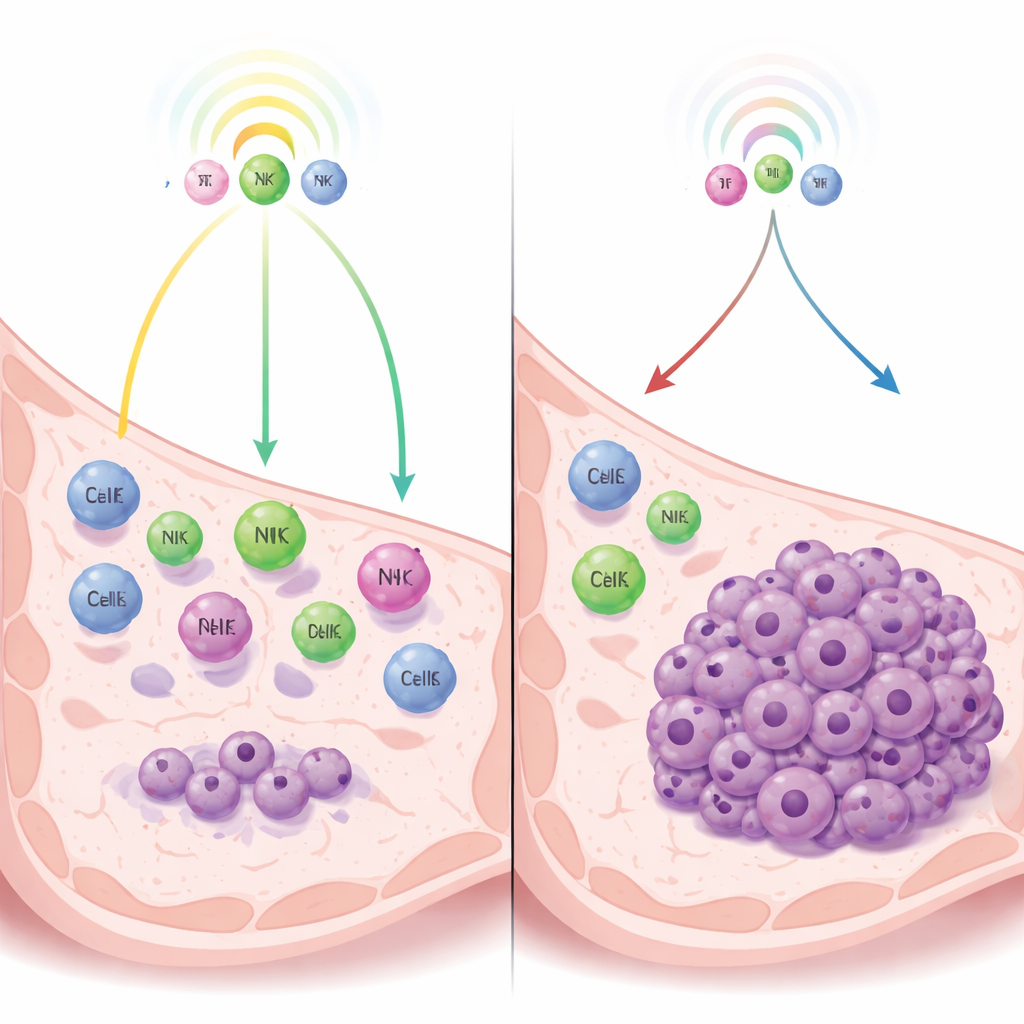
Kanser ile bağışıklık sistemi arasında bir çekişme
Yazarlar, dormansın kan akışının yetersizliği veya hücre içi frenlerden çok, tümörleri yok etmeksizin kontrol altında tutabilen immün gözetim tarafından yönetildiği bir türüne odaklanıyor. Üçlü negatif meme kanserinin fare modellerini kullanarak, doğal olarak uykuda kalan tümör hücrelerini hızlı büyüyen tümörler oluşturan yakından ilişkili hücrelerle karşılaştırıyorlar. Hangi genlerin etkinleştiğini inceleyerek, uykuda kalan hücrelerin interferon yolaklarını—bağışıklık alarm sistemlerini—güçlü biçimde aktive ettiğini ve bu yolakların tümör çevresine bağışıklık hücrelerini çeken kimyasal habercilerin salınımını uyardığını buluyorlar.
Tümörleri sessiz tutan kilit bir kimyasal haberci
Uykuda kalan hücrelerde açılan çok sayıda molekül arasında öne çıkan bir tane var: CXCL10, CXCR3 adlı eş reseptörünü taşıyan immün hücreleri çekmeye benzeyen küçük bir protein. Uykuda kalan kanser hücreleri, agresif muadillerine göre çok daha fazla CXCL10 üretiyor. Araştırmacılar uykuda kalan hücrelerde CXCL10’u kasıtlı olarak kapattıklarında ve bunları sağlam bir bağışıklık sistemine sahip farelere naklettiklerinde, bir zamanlar sessiz olan hücreler hızla tümör oluşturuyor. CXCR3 reseptörünü bir antikorla bloke etmek de benzer bir etki gösteriyor. Her iki durumda da kanser hücreleri immün çıkmaza son verip büyümeye başlıyor; bu da CXCL10/CXCR3 ekseninin yalnızca dormansla ilişkili olmadığını, aynı zamanda dormansı sürdürmek için gerekli olduğunu gösteriyor.
Yerel çevrenin değişmesi dengeleri nasıl değiştirir
CXCL10’un azaltılması tek bir yolu değiştirmekten daha fazlasını yapıyor; tüm yerel immün peyzajı yeniden şekillendiriyor. CXCL10’u kaybeden tümörlerde yardımcı CD4 ve CD8 T hücreleri azalırken, bağışıklık yanıtlarını baskılayabilen belirli miyeloid hücreler daha çok bulunuyor. Doğal öldürücü hücreler ve dendritik hücreler de sayıca değişiyor. Bu desen hem primer tümörlerde hem de kanser hücrelerinin seyahat edip sessiz kaldığı akciğerlerde görülüyor. Akciğer metastazları mikroskop altında görülmeyecek kadar küçük olsa bile, moleküler belirteçler CXCL10 yokluğunda daha fazla kanser hücresinin akciğeri kolonize etmeyi başardığını ve bu dokulara daha az T hücresinin girdiğini gösteriyor. Ancak tamamen işlevsiz bir bağışıklık sistemine sahip farelerde CXCL10’un çıkarılması fark yaratmıyor—uykuda olan hücreler her durumda büyüyor—bu da bu sinyalin doğrudan kanser hücresinin büyümesini frenlemekten ziyade immün kontrol aracılığıyla etkili olduğunu vurguluyor.
Daha fazla sinyal yardımcı ama sihirli bir anahtar değil
Ekip ters fikri de test ediyor: CXCL10’u artırmak agresif bir tümörü uykuda bir hale çevirebilir mi? Hızlı büyüyen kanser hücrelerini ekstra CXCL10 üretecek şekilde değiştirdiklerinde, tümörler daha yavaş büyüyor ve ortaya çıkmaları daha uzun sürüyor; kanda bazı immün hücre tipleri artış gösteriyor. Ancak tam dormans gelişmiyor; sonunda tüm farelerde yine de tümör oluşuyor. Bu, CXCL10’un, geri kalan immün makine yerinde olduğunda dormansı sürdürmek için gerekli olduğunu, ancak tek başına bu karmaşık durumu sıfırdan oluşturamayacağını gösteriyor. Uzun süreli bir denge kurmak için başka yolakların da iş birliği yapması gerekiyor.
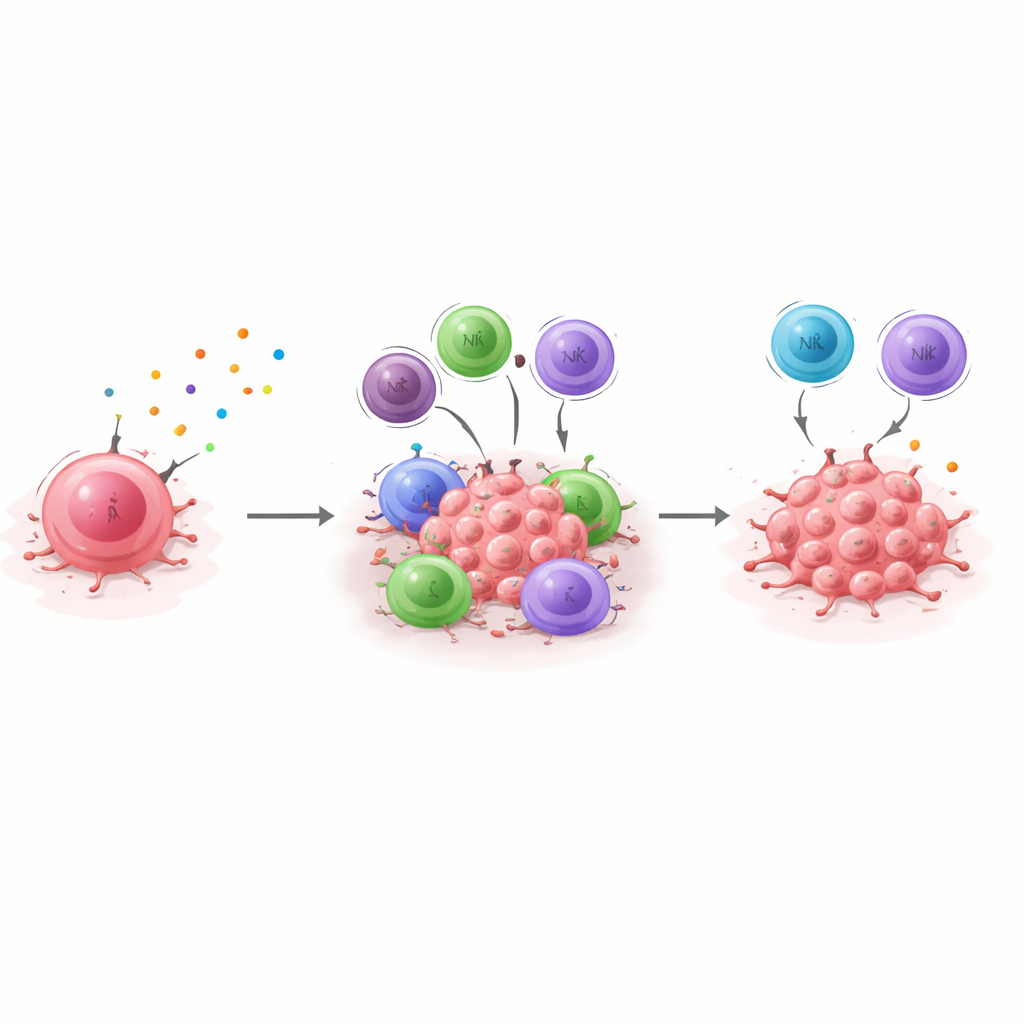
Fare deneylerinden hasta beklentisine
Bulgularını insan hastalığıyla ilişkilendirmek için araştırmacılar bir “dormansi imzası” türetiyor—uykuda olan hücrelerde tutarlı şekilde yüksek olan ve CXCL10 susturulduğunda düşen bir gen seti. Daha sonra büyük meme kanseri hasta veri kümelerine bakıp bu imzanın yaşam süresiyle nasıl ilişkili olduğunu sorguluyorlar. Üçlü negatif meme kanserinde, tümörleri bu dormansi imzasını daha yüksek düzeyde ifade eden hastalar genel olarak daha uzun yaşıyor ve daha uzun yıllar nüks olmadan kalma eğiliminde; bu, immün kontrollü bir dormansın tekrarı geciktirdiğiyle uyumlu. Bu etki hormon pozitif tümörlerde aynı şekilde görülmüyor; bu da meme kanseri alt tipleri arasındaki biyolojik farklılıkları vurguluyor. Sonuçlar birlikte, CXCL10/CXCR3 ekseninin üçlü negatif meme kanserinde immün aracılı dormansın merkezi bir direği olduğunu ve bu dormansi imzasının ölçülmesinin, immün kontrolü güçlendiren terapilerden yararlanma olasılığı yüksek hastaları belirlemeye—veya tersine, kanserleri daha az iyi kontrol edilen hastalar için daha yakından uzun dönem izleme gerektirebilecekleri konusunda yol göstermeye—yardımcı olabileceğini öne sürüyor.
Atıf: Yilmaz, A., Haerri, L., Granda, M.E. et al. The CXCL10/CXCR3 axis is essential for sustaining immunological dormancy in triple-negative breast cancer. npj Breast Cancer 12, 36 (2026). https://doi.org/10.1038/s41523-026-00903-6
Anahtar kelimeler: üçlü negatif meme kanseri, tümör uykuda kalma (dormansi), immün gözetim, kemokin sinyalleşmesi, CXCL10 CXCR3 ekseni