Clear Sky Science · tr
Hücresel düzeydeki gen ekspresyonu analizi, meme kanserinde çok erken lenf nodu metastazının sürükleyicilerini ortaya koyuyor
Neden küçük yolculuk yapan kanser hücreleri önemli?
Meme kanseri memeden yayıldığında, genellikle ilk olarak yakınlardaki lenf nodlarında durur—enfeksiyonla savaşmaya yardımcı küçük filtreler. Doktorlar, bu nodlarda kanser bulunmasının hastalığın yeniden ortaya çıkma riskinin genellikle daha yüksek olduğunun bir işareti olduğunu bilir. Ancak yalnızca birkaç hücrenin bir lenf noduna ulaştığı çok ilk anlarda gerçekte neler olduğu, gerçek hastalarda neredeyse görmek imkânsızdı. Bu çalışma, gen aktivitesinin yeni bir tür mikroskobik “haritasını” kullanarak bu en erken adımları benzeri görülmemiş bir ayrıntıyla izledi; hangi hücrelerin başarılı olduğunu, hangilerinin başarısız olduğunu ve bunun hasta sonuçları açısından neden önemli olduğunu ortaya koydu.
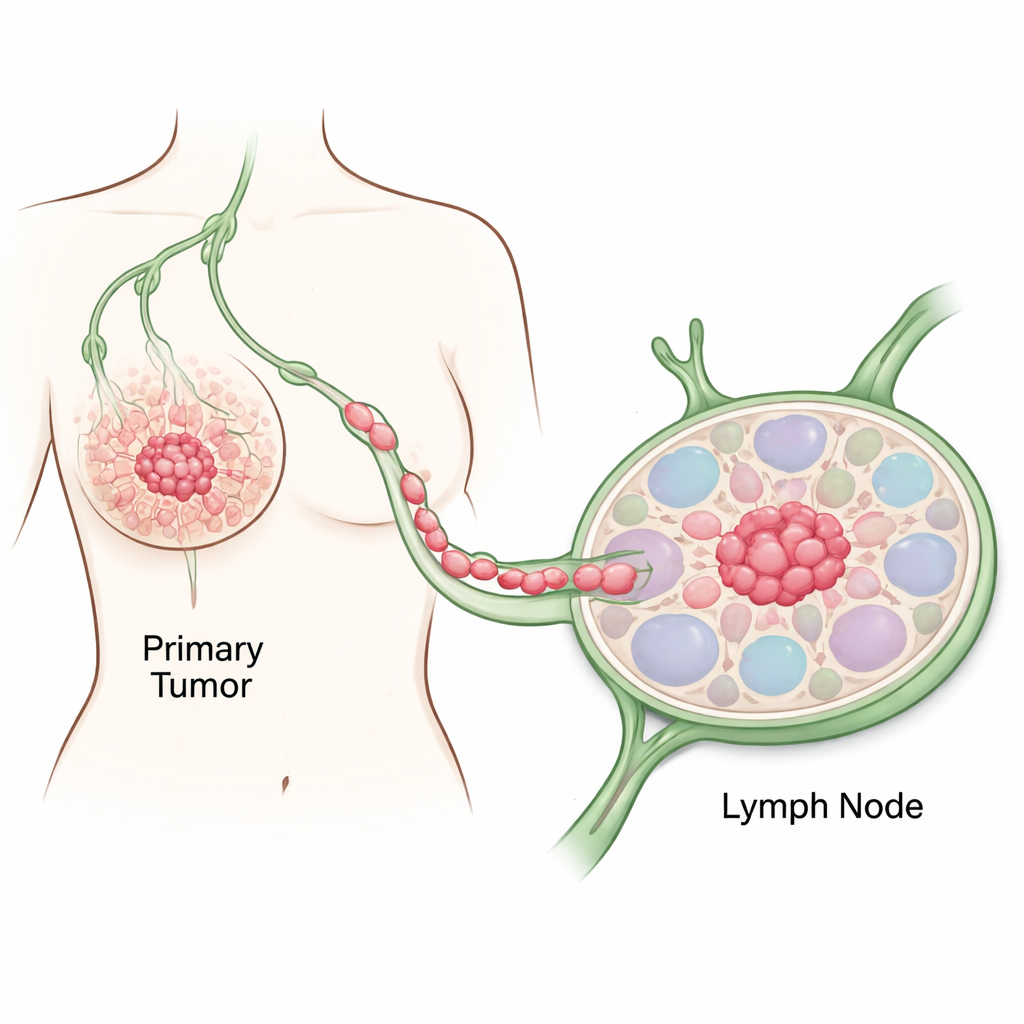
Kanserin ilk adımlarını izlemek
Araştırmacılar agresif, HER2-pozitif bir meme kanseri olan 80 yaşındaki bir kadından alınan dokuya odaklandı. Hem normal görünen meme bölgeleri hem de yakın tümör bölgelerinden örnek aldılar ve sıradan hücrelerin nasıl kansere dönüştüğünü izlemek için birden çok DNA ve RNA testi kullandılar. Sağlıklı doku ile karşılaştırıldığında, tümör bölgeleri kanserin klasik ayırt edici özelliklerini gösterdi: hücre adezyonunda bozulma, aşırı aktif hücre bölünmesi, geniş çaplı DNA metilasyon değişiklikleri ve büyüme ve genom kararlılığını kontrol eden genlerdeki önemli mutasyonlar. Bu moleküler değişimler patologların mikroskop altında gördükleriyle örtüştü ve normal meme hücrelerinden tamamen malign hücrelere doğru adım adım bir geçişi doğruladı.
Hareket halindeki şekil değiştiren hücreler
Tümör hücrelerinin nasıl yolculuğa başladığını anlamak için ekip, hücrelerin doku içindeki kesin konumlarını korurken bireysel hücrelerdeki gen aktivitesini okuyan yüksek çözünürlüklü bir teknik kullandı. Bu, kanser hücrelerinin normal meme yapılarından ayrılıp metastaz yönünde ilerlerken kimliklerinin nasıl değiştiğini yeniden yapılandırmalarına izin verdi. Kanserin belirli olgun bir meme hücresi türünden kaynaklandığı ve bunun daha sonra hücrelerin gevşemesine, hareket etmesine ve çevre dokuya invazyonuna yardımcı olan epitel–mezenkimal dönüşüm olarak adlandırılan bir sürecin özelliklerini kademeli olarak benimsediği bulundu. Basit bir açma-kapama anahtarı yerine, hücreler epitel özellikleri (düzenli, birbirine yapışık) ile mezenkimal özellikleri (hareketli, invaziv) harmanlayan bir dizi karışık durumda yer aldı. Bu hibrit hücrelerin bazıları tümör içinde dağıldı, bazıları ise lenf nodlarına yayılmaya hazır daha ileri kanser kümeleri halinde toplandı.
Lenf nodunda ilk uzak köprübaşı
Standart klinik testlerle metastazsız olarak değerlendirilen bir lenf nodunda, bilim insanları dikkat çekici bir şey fark etti: yaklaşık 200 mikrometre genişliğinde—insan kılının yaklaşık iki katı—sadece 30 başıboş tümör hücresi. Bu izole tümör hücreleri, her birinin kendine özgü gen aktivite desenine sahip birkaç farklı hibrit durumdan geliyordu. İlişkili kanser hücrelerini gruplayarak ekip, farklı rollere sahip altı alt tip tanımladı. Güçlü biçimde "mezenkimal" olan bir alt tip, özellikle hücre ölümüne direnme ve bağışıklıktan kaçma konusunda başarılı görünüyordu. Daha fazla epitel özellikler kazanan başka bir alt tip ise enerji kullanımında çarpıcı bir değişim göstererek yağ asidi metabolizmasını tercih ediyordu. Yalnızca bu metabolik olarak yeniden programlanmış, daha epitel-benzeri grup lenf nodlarında küçük koloniler oluşturmayı başardı; bu da yakıt seçiminin—sadece invazivlik değil—erken gelenlerin yerleşip yerleşemeyeceğini belirlemeye yardımcı olduğunu düşündürüyor.
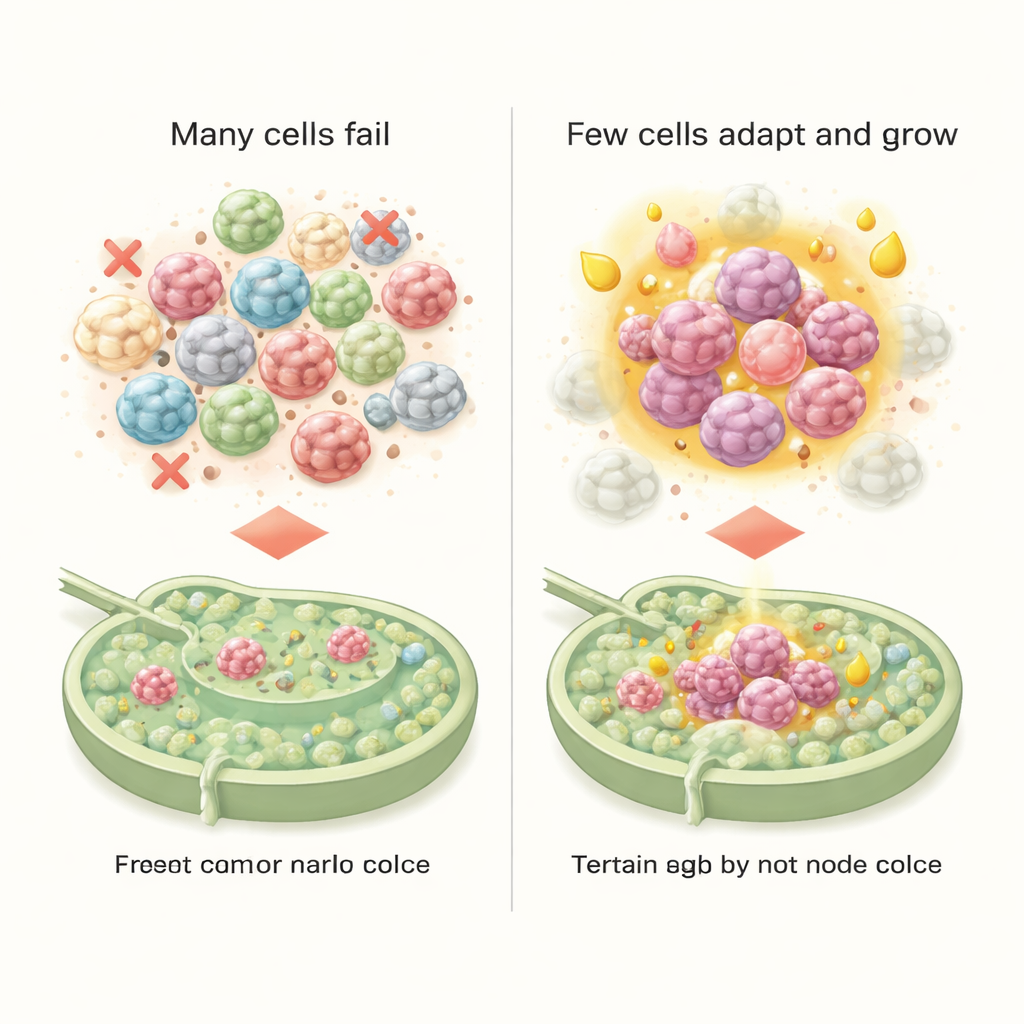
Sessizce kansere yardım eden bir lenf nodu
Çalışma ayrıca lenf nodu ortamının bu istilacılara nasıl yanıt verdiğini inceledi. Görünür bir metastaz oluşmadan bile bağışıklık hücreleri, kan damar hücreleri ve bağ dokusu çoktan bağışıklık tepkilerini zayıflatan ve tümörün hayatta kalmasını destekleyen sinyaller göndermeye başlamıştı. Bağışıklık hücreleri arasındaki belirli reseptör–ligand eşleşmeleri erken bağışıklık toleransını ima ederken, diğerleri yeni kan damarlarının büyümesini ve doku iskeletinin yeniden şekillenmesini teşvik ediyordu. Bu değişiklikler birlikte, metabolik olarak uyum sağlamış kanser hücrelerine şaşırtıcı derecede elverişli bir niş oluşturdu; bu da onların hayatta kalmasına, büyümesine ve potansiyel olarak gelecekteki yayılımlara tohum teşkil etmesine yardımcı oldu.
Bu, hastalar için ne anlama geliyor?
Bulgularını büyük, mevcut hasta veri setleriyle karşılaştırarak araştırmacılar sezgilere ters bir keşif yaptı. Erken lenf nodu kolonileri oluşturma konusunda en iyi olan hücreler ve hatta en güçlü mezenkimal özelliklere sahip olanlar en kötü klinik sonuçlarla ilişkili değildi. Bunun yerine, hastalar en kötü gidişatı tümörde yüksek hücre döngüsü aktivitesi ve MYC gibi genlerin yönlendirdiği glikoliz (şeker yakma) programlarıyla işaretlenmiş belirli agresif hibrit hücre tiplerine sahip olduklarında yaşadı. Başka bir deyişle, farklı şekil değiştirmiş hücre durumları uzmanlaşıyor gibi görünüyordu: bazıları yeni bölgeleri sessizce kolonize etmede uzmandı, bazıları ise hızlı büyüme ve nüksü tetikliyor. Bu farklı hücre durumlarını ve onların metabolik tercihlerinin anlaşılması ve hedeflenmesi, yalnızca en erken yayılmayı daha güvenilir şekilde tespit eden değil, aynı zamanda ölümcül nüksleri en çok tetikleme olasılığı olan tümör hücresi tiplerini de kesintiye uğratan daha hassas tedavilere yol açabilir.
Atıf: Nagasawa, S., Kajiya, K., Ishikawa, E. et al. Spatial gene expression analysis reveals drivers of extremely early lymph node metastasis in breast cancer. npj Breast Cancer 12, 28 (2026). https://doi.org/10.1038/s41523-026-00897-1
Anahtar kelimeler: meme kanseri metastazı, lenf nodu, epitelyal mezenkimal dönüşüm, mekânsal transkriptomik, kanser metabolizması