Clear Sky Science · tr
Mezenkimal kök hücreler tarafından kemokin CXCL9 ve kostimülatör ligand TNFSF9’un eşzamanlı verilmesi, üçlü-negatif meme kanseri için bağışıklık mikroçevresini yeniden programlıyor
Bu yeni meme kanseri yaklaşımı neden önemli
Üçlü-negatif meme kanseri, hızlı büyümesi, erken yayılması ve birçok ilacın hedeflediği yaygın hormon hedeflerinden yoksun olması nedeniyle en tehlikeli meme kanseri türlerinden biridir. İmmünoterapi umutları artırdı, ancak birçok hastada bağışıklık sisteminin savaşçı hücreleri tümöre yeterince girmiyor. Bu çalışma yaratıcı bir stratejiyi inceliyor: bağışık gücünü artıran sinyalleri zor tedavi edilen tümörlerin içine doğrudan taşıyan yaşayan kura hücreleri kullanmak — adeta yönlendirilmiş “dağıtım kamyonları” — böylece daha fazla hastayı güçlü immün temelli tedavilere uygun hale getirmek mümkün olabilir.
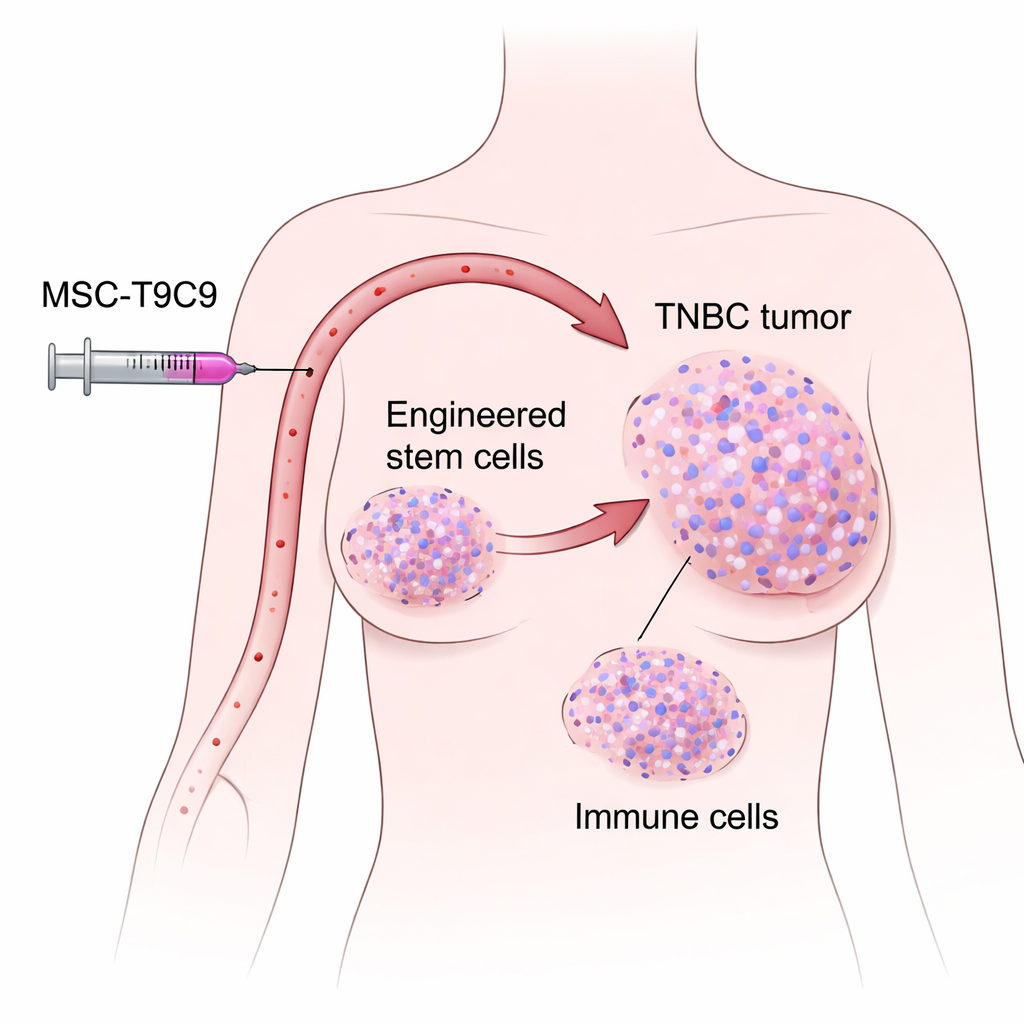
Yeterince bağışıklık desteği olmayan zor bir kanser
Üçlü-negatif meme kanseri için standart tedaviler—cerrahi, kemoterapi ve radyasyon—genellikle nüksü engelleyemiyor ve ilerlemiş hastalıkta ortalama yaşam süresi iki yılın altında kalmaya devam ediyor. Bunun başlıca nedenlerinden biri birçok tümörün “soğuk” olması; yani kanserle savaşan bağışıklık hücrelerini az bulundurması. Büyük hasta veri tabanları, tümörleri doğal olarak iki immün ilişkili molekül olan CXCL9 ve TNFSF9’u daha yüksek miktarda üreten kişilerin daha uzun yaşama eğiliminde olduğunu ve tümörlerinde daha fazla T hücresi ile doğal öldürücü (NK) hücre bulunduğunu gösterdi. CXCL9, bağışıklık hücrelerini dokuya çağıran kimyasal bir sinyalken, TNFSF9 bu hücrelerin daha güçlü saldırmasını sağlayan ek bir “harekete geçir” düğmesi gibi davranır. Bu desen, her iki sinyalin doğrudan tümör içinde yükseltilmesinin bağışıklık sisteminin lehine dengeyi değiştirebileceğini düşündürdü.
Kök hücreleri akıllı dağıtım kamyonlarına dönüştürmek
Araştırmacılar, bağışlanmış insan göbek kordonlarından alınan mezenkimal kök hücrelere odaklandı. Bu hücrelerin yararlı bir özelliği var: meme tümörü taşıyan farelerin kan dolaşımına enjekte edildiğinde doğal olarak tümör bölgelerine yönelir ve günlerce orada kalırken normal organlardan büyük ölçüde kaçınırlar. Ekip, bu kök hücreleri CXCL9 salgılayacak ve yüzeylerinde TNFSF9 sergileyecek şekilde genetik olarak mühendislik yaptı; böylece MSC‑T9C9 adını verdikleri çift amaçlı bir hücre tedavisi oluşturuldu. Laboratuvar testleri, modifiye hücrelerin yüksek düzeyde CXCL9 ürettiğini ve kendi büyüme davranışlarını değiştirmeden veya kendileri tümör oluşturmadan fare T hücrelerini ve NK hücrelerini güçlü biçimde aktive ettiğini gösterdi. Bu bulgu, onları hedefe yönelik bağışıklık güçlendiricileri olarak umut verici adaylar haline getirdi.
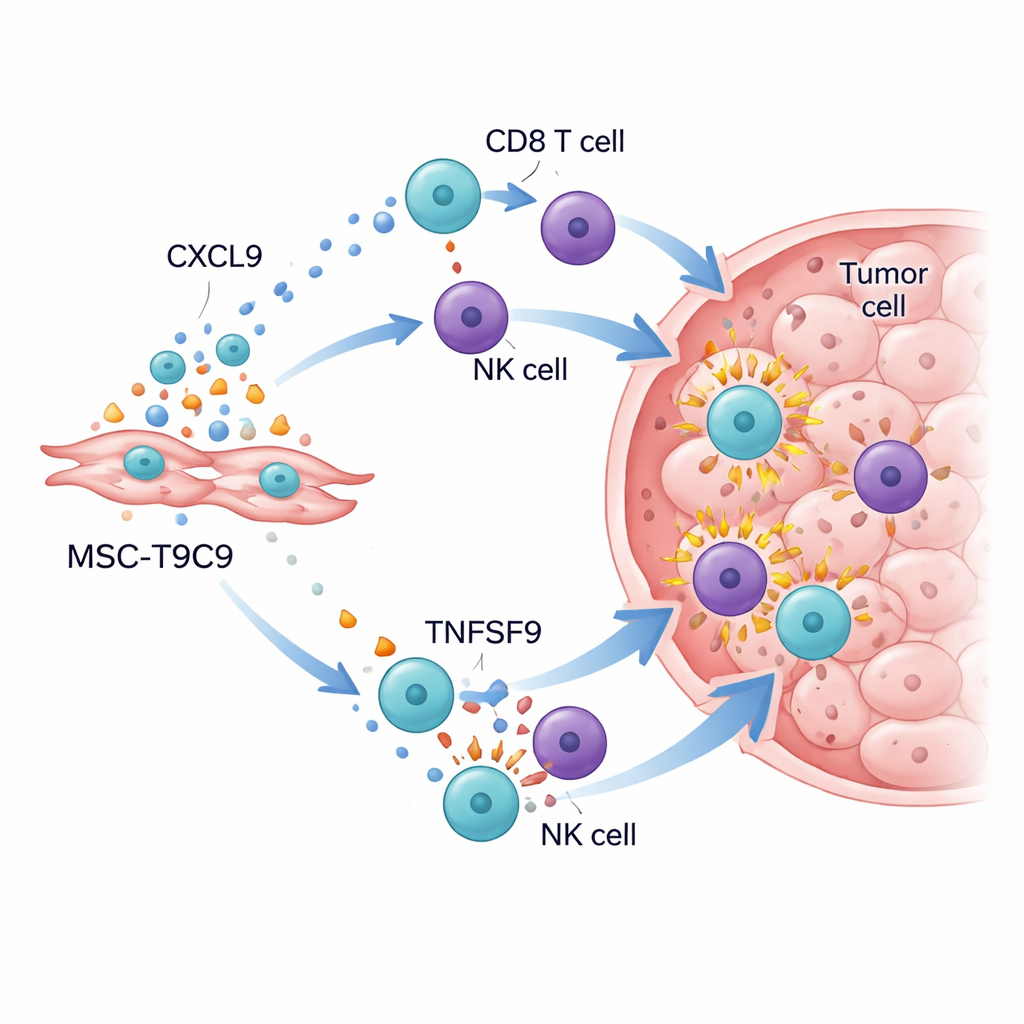
Tümörün bağışıklık savaş alanını uyandırmak
Mühendislik yapılmış hücreler üçlü-negatif meme tümörü taşıyan farelere verildiğinde sonuçlar çarpıcıydı. Çalışan bir bağışıklık sistemi olan farelerde MSC‑T9C9’in tekrarlayan enjeksiyonları tümör büyümesini büyük ölçüde yavaşlattı ve kanser hücresi ölümünü artırdı; kontrol kök hücrelerinin ise az etkisi oldu. Tümörlerin ayrıntılı analizi, CD8 “katil” T hücreleri ve NK hücrelerinin sayısında dramatik bir artış ile birlikte granzyme B, interferon‑γ, tümör nekroz faktörü‑α ve interlökin‑2 gibi güçlü saldırı moleküllerinin düzeylerinde artış gösterdi. Aynı zamanda tümör çevresi baskılayıcı halden uzaklaştı: yardımcı iltihabi makrofajlar arttı ve düzenleyici T hücreleri hala mevcut olmasına rağmen yeni gelen savaşçı dalgası tarafından sayıca gölgede bırakıldılar. T ve NK hücrelerinin eksik olduğu bağışıklık yetmezliği olan farelerde MSC‑T9C9 tümör büyümesini yavaşlatmadı; bu da faydasının vücudun kendi savunmasını harekete geçirmeye bağlı olduğunu doğruladı.
Checkpoint terapisi için tümörleri hazırlama
Anti‑PD‑1 antikorları gibi modern immünoterapi ilaçları T hücreleri üzerindeki moleküler “frenleri” gevşetir, ancak zaten yeterli sayıda T hücresi tümör içinde mevcut olduğunda en iyi sonucu verirler. Çalışma, MSC‑T9C9’in sadece daha fazla CD8 T hücresini tümörlere çekmekle kalmadığını, aynı zamanda bu hücreleri PD‑1 reseptörü ile işaretlenen yüksek aktiviteye fakat frenlere duyarlı bir duruma ittiğini buldu. Bir fare modelinde MSC‑T9C9 ile bir anti‑PD‑1 ilacının kombinasyonu, tek başına verilen tedavilere kıyasla en güçlü tümör küçülmesini ve en uzun sağkalımı sağladı. İnsan kanser veri setlerinin analizleri de bu fikri destekledi: TNFSF9 ve CXCL9’un birlikte daha yüksek düzeylerine sahip hastaların checkpoint blokaj terapilerinden daha fazla yarar görme olasılığı vardı; bu da aynı biyolojinin insanlarda da geçerli olabileceğini öne sürüyor.
Güvenlik ve gelecekteki umut
Bağışıklığı artıran her tedavi yaygın iltihap veya organ hasarı gibi tehlikeli yan etki endişelerini gündeme getirir. Teşvik edici olarak, MSC‑T9C9 alan fareler normal kilo ve davranışı korudu, önemli organlarda belirgin bir yaralanma göstermedi ve kan ile karaciğer‑böbrek testleri normaldi. Önemli olarak, bağışıklık aktivitesindeki sıçrama büyük ölçüde tümörle sınırlı kaldı ve kanda iltihabi sinyaller artmadı. İnsan denemelerinden önce—daha gerçekçi modellerde testler ve dikkatli doz belirleme dahil olmak üzere—daha fazla çalışma gerektiği halde bu çalışma, mühendislik yapılmış kök hücrelerin tümörlere yönlendirilerek bağışıklık hücrelerini çağırıp aktifleştirmesinin, “soğuk” üçlü-negatif meme kanserlerini immünoterapiye daha duyarlı “sıcak” hale getirmenin hedefli ve daha güvenli bir yolu olabileceğini öne sürüyor.
Atıf: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Anahtar kelimeler: üçlü-negatif meme kanseri, immünoterapi, mezenkimal kök hücreler, tümör mikroçevresi, checkpoint blokajı