Clear Sky Science · tr
Konak kaynaklı interlökin-1α, tümör ilişkili myeloid hücreleri yeniden programlayarak tümör immünsüpresyonunu tetikliyor
Bu araştırma kanser hastaları için neden önemli
İmmünoterapi bazı kanserlerin tedavisini kökten değiştirdi, ancak birçok meme tümörü hâlâ bağışıklık sisteminden kaçabiliyor. Bu makale, kanser hücrelerinin kendisi tarafından değil, vücudun normal hücreleri tarafından üretilen interlökin‑1 alfa (IL‑1α) adlı daha az bilinen bir sinyal molekülünü inceliyor. Yazarlar, konağa ait IL‑1α’nın bağışıklık hücrelerini sinsi bir şekilde tümörün müttefiki hâline getirebileceğini ve bu sinyali farelerde engellemenin meme tümörlerinin küçülmesine veya ortadan kalkmasına neden olabileceğini gösteriyor. Bu dönüşümün anlaşılması, hekimlerin immünoterapinin meme kanserinde daha etkili olmasını sağlayacak tedaviler tasarlamasına yardımcı olabilir.
Tümör mahallesindeki gizli bir etken
Kansere yalnız büyüyen bir hücre kitlesi gözüyle bakmamak gerekir; tümörler bağışıklık hücreleri, kan damarları ve bağ dokudan oluşan yoğun bir “mahalle”de yaşar — buna tümör mikroçevresi denir. En önemli sakinlerden biri myeloid hücrelerdir, özellikle makrofajlar; bunlar tümörleri ya yok edebilir ya da koruyabilir. Klasik kaynaklar makrofajları M1 (tümörle savaşan) ve M2 (tümörü destekleyen) diye ayırsa da, gerçek tümörlerde bu kutuplaşmanın arasındaki çok sayıda ara durum bulunur. Yazarlar, konağa ait bir sinyal olan ve kanser dışı dokular tarafından normalde üretilen IL‑1α’ya odaklanarak, bu sinyalin gelen myeloid hücreleri meme tümörleri içinde yardımcı mı yoksa zarar verici rollere mi yönlendirdiğini sorguladılar.
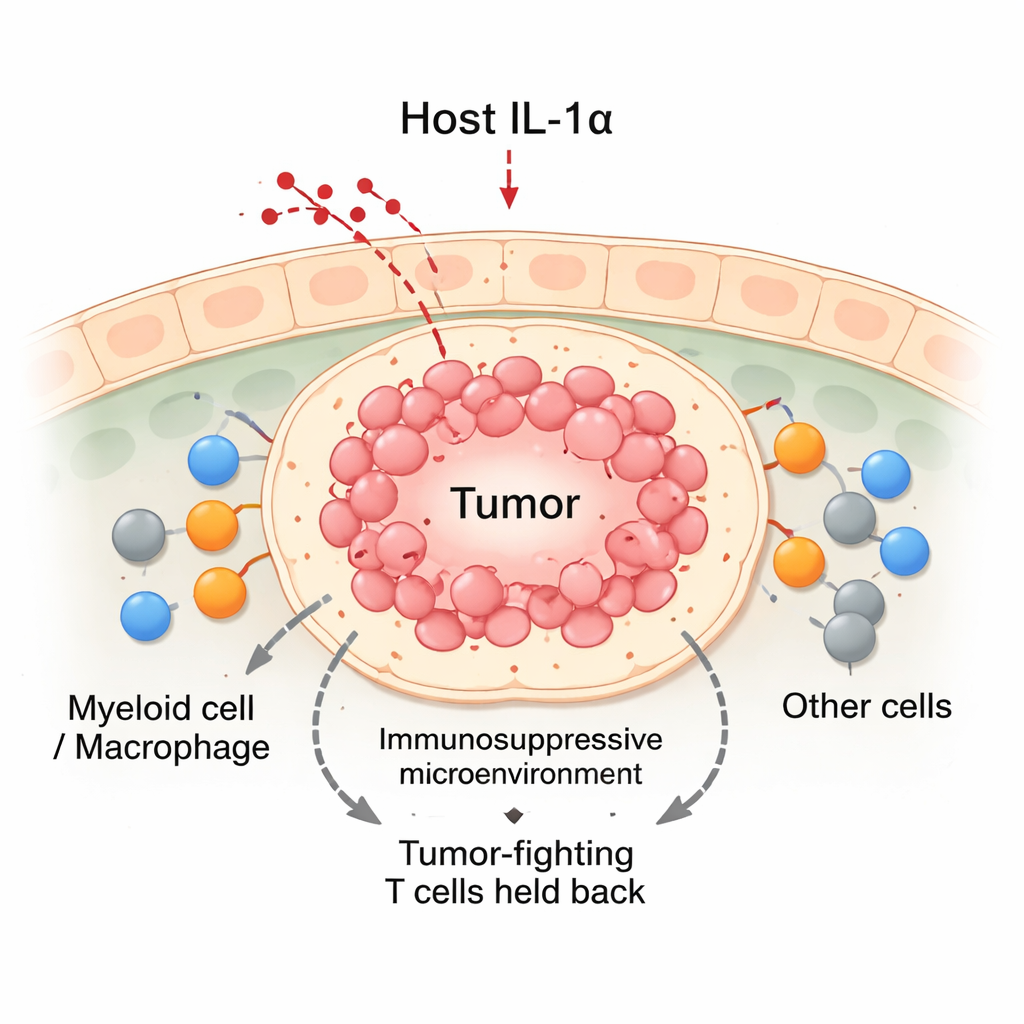
IL‑1α’yı kapatmak tümörlere karşı dengeyi değiştiriyor
Meme kanseri fare modellerinde ekip, normal hayvanları IL‑1α eksikliği ile genetik olarak üretilmiş olanlarla karşılaştırdı. Meme bezine kanser hücreleri nakledildiğinde, normal farelerde tümörler istikrarlı şekilde büyüdü. Buna karşılık, IL‑1α eksik farelerde tümörler yaklaşık iki hafta boyunca büyüdükten sonra sıklıkla geriledi. Bu gerileyen tümörlerde genel olarak daha fazla bağışıklık hücresi vardı; CD8 “katil” T hücreleri ve myeloid hücrelerde bir artış gözlendi. IL‑1α eksik farelerin kan dolaşımında daha az akyuvar bulunsa da, tümör bölgesine çok daha fazla bağışıklık hücresi biriktiriyorlardı. Ayrıntılı analizler, IL‑1α eksik tümörlerdeki infiltre olan CD8 T hücrelerinin daha aktif olduğunu, daha yüksek düzeyde tümör‑öldürücü moleküller ürettiğini ve tükenme belirtilerinin daha az olduğunu gösterdi.
IL‑1α, tümör ilişkili myeloid hücreleri nasıl yeniden şekillendiriyor
IL‑1α’nın hücresel düzeyde ne yaptığını anlamak için araştırmacılar, tümörlerden binlerce bireysel hücreyi incelemek üzere tek hücre RNA dizilemesi kullandılar. Sadece küçük bir tümör ilişkili makrofaj alt kümesinin — CX3CR1 adlı bir reseptörle işaretlenenlerin — IL‑1α ürettiğini keşfettiler. Normal farelerde birçok gelen monosit bu CX3CR1‑pozitif makrofajlara olgunlaşıyordu ve bunlar bağışıklığı baskılayan davranışlarla ilişkilendiriliyordu. IL‑1α eksik farelerde bu olgunlaşma yolu bozulmuştu. Bunun yerine, myeloid hücreler iNOS‑pozitif inflamatuar makrofajlar hâline gelmeye daha yatkındı; bu profil anti‑tümör aktivite ile ilişkilidir. İşlevsel olarak, IL‑1α eksik tümörlerden alınan myeloid hücreler T hücrelerinde PD‑1 ve CTLA‑4 gibi frenleyicileri indükleme konusunda daha az yetenekliydi ve T hücresi proliferasyonunu baskılama kapasiteleri daha zayıftı.
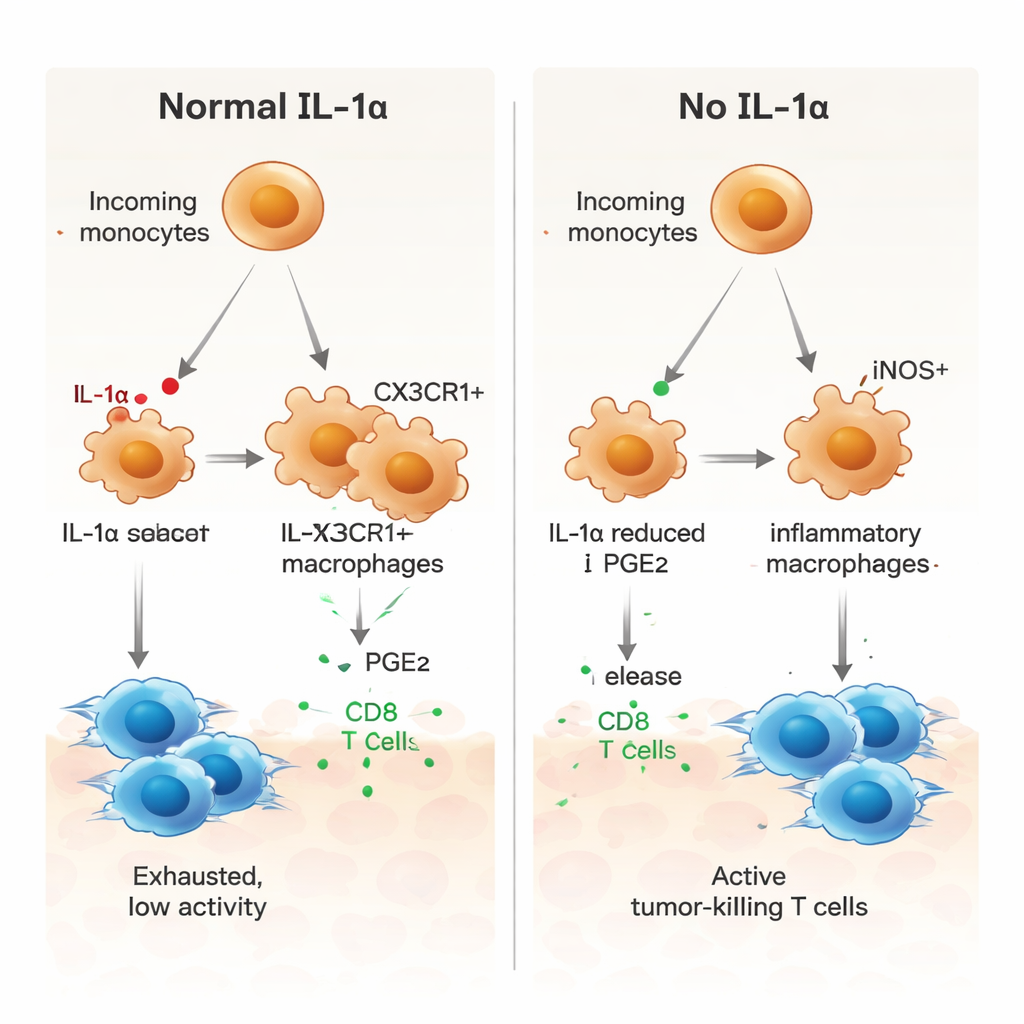
Bir lipid haberci: PGE2’nin kilit rolü
Daha sonra yazarlar IL‑1α’nın myeloid hücreleri tümör‑destekleyici bir duruma nasıl ittiğini sordular. Tek hücre verilerinin iletişim analizi, prostaglandin E2 (PGE2) içeren bir yol da dahil olmak üzere birkaç sinyal yoluna işaret etti; PGE2 bağışıklık baskısını teşvik eden bir lipid aracıdır. IL‑1α eksik tümörlerde makrofajlar, makrofaj büyüme faktörü (M‑CSF) reseptörleri, TGF‑β reseptörleri ve bir PGE2 reseptörü için daha düşük ekspresyon gösterdi ve yakın stromal hücreler PGE2 üreten enzimleri daha az üretiyordu. Laboratuvar kültürlerinde, IL‑1α eksik farelerden elde edilen kemik iliği kaynaklı makrofajlar daha inflamatuar bir profil sergiledi; iNOS yüksek, CX3CR1 düşük bulundu. PGE2 eklenmesi bu değişimi tersine çevirdi ve daha baskılayıcı bir örüntüyü geri getirdi; normal makrofajlarda PGE2 bloke edildiğinde ise bunlar pro‑inflamatuar bir duruma kaydı. IL‑1α olmayan makrofajlar ayrıca tümör‑spesifik CD8 T hücresi proliferasyonunu daha güçlü şekilde uyardı; PGE2 eklendiğinde bu etki zayıfladı.
Fare bulgularını insan bağışıklığına köprülemek
Fare verilerinin insan biyolojisini yansıtıp yansıtmadığını görmek için ekip, farklı fare makrofaj alt kümelerinden elde edilen gen imzalarını, laboratuvarda çeşitli durumlara yönlendirilen geniş bir insan myeloid hücre paneliyle karşılaştırdı. Normal farelerin tümörlerinden alınan makrofaj kümeleri, IL‑10, IL‑4 ve glukokortikoidler gibi moleküller tarafından M2‑benzeri, bağışıklığı zayıflatan durumlara itilen insan hücrelerine benzedi. Buna karşılık, IL‑1α eksik tümörlerden gelen aynı kümeler daha inflamatuar ve daha az baskılayıcı koşullara giren insan hücreleriyle eşleşti. Önemli olarak, PGE2 sinyaline bağlı gen örüntüleri IL‑1α‑bağımlı makrofajlarda zenginleşmişken IL‑1α yokluğunda yoktu; bu, IL‑1α ile PGE2’nin birlikte immünsüpresif bir niş oluşturduğunu güçlendiriyor.
Gelecekteki meme kanseri tedavisi için ne anlama gelebilir
Basitçe söylemek gerekirse, bu çalışma konağa ait bir molekül olan IL‑1α’nın belirli makrofajlara tümörü korumalarını ve katil T hücrelerini dizginlemelerini sinsi bir şekilde söyleyebileceğini; bunun bir kısmının PGE2 sinyali aracılığıyla gerçekleştiğini öne sürüyor. Farelerde IL‑1α kaldırıldığında makrofajlar daha inflamatuar, tümör‑saldırgan bir profile kayıyor, CD8 T hücreleri daha aktif hâle geliyor ve nakledilen meme tümörleri sıkça reddediliyor. Mevcut immünoterapiler hâlihazırda tükenmiş T hücreleri yeniden canlandırmayı hedeflediğinden, bunları IL‑1α veya bunun aşağı akıştaki PGE2 yolunu engelleyen yaklaşımlarla birleştirmek tümör mikroçevresini hastanın bağışıklık sistemi lehine daha da eğebilir. İnsanlarda güvenlik ve etkinliği test etmek için daha fazla çalışma gerekli olsa da, bu bulgular IL‑1α’yı meme kanserini bağışıklık saldırısına daha açık hâle getirebilecek umut verici yeni bir hedef olarak öne çıkarıyor.
Atıf: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Anahtar kelimeler: meme kanseri immünoterapisi, tümör mikroçevresi, makrofajlar, interlökin-1 alfa, prostaglandin E2