Clear Sky Science · tr
Sentetik fag tabanlı CRISPR‑Cas taşıma sistemleriyle Staphylococcus aureus mastitis enfeksiyonlarının hedeflenmiş ortadan kaldırılması
Yüksek Maliyetli Bir Süt Enfeksiyonuyla Mücadele
İnekler ve diğer çiftlik hayvanlarının sütü, sıklıkla Staphylococcus aureus bakterisinin neden olduğu ağrılı bir meme enfeksiyonu olan mastitis tarafından bozulabilir. Bu enfeksiyonların tedavisi genellikle uzun süreli antibiyotik kullanımını gerektirir; bu yöntemler hem maliyetli ve hayvanlar için streslidir hem de artan antibiyotik direnci sorununa katkıda bulunur. Bu çalışma kökten farklı bir yaklaşımı araştırıyor: bakterilere özgü doğal bir virüs benzeri paraziti, bakterinin DNA’sını seçici olarak kesebilen ve direnç genleri yaymadan enfeksiyonları temizleyebilen hassas bir silaha dönüştürmek.
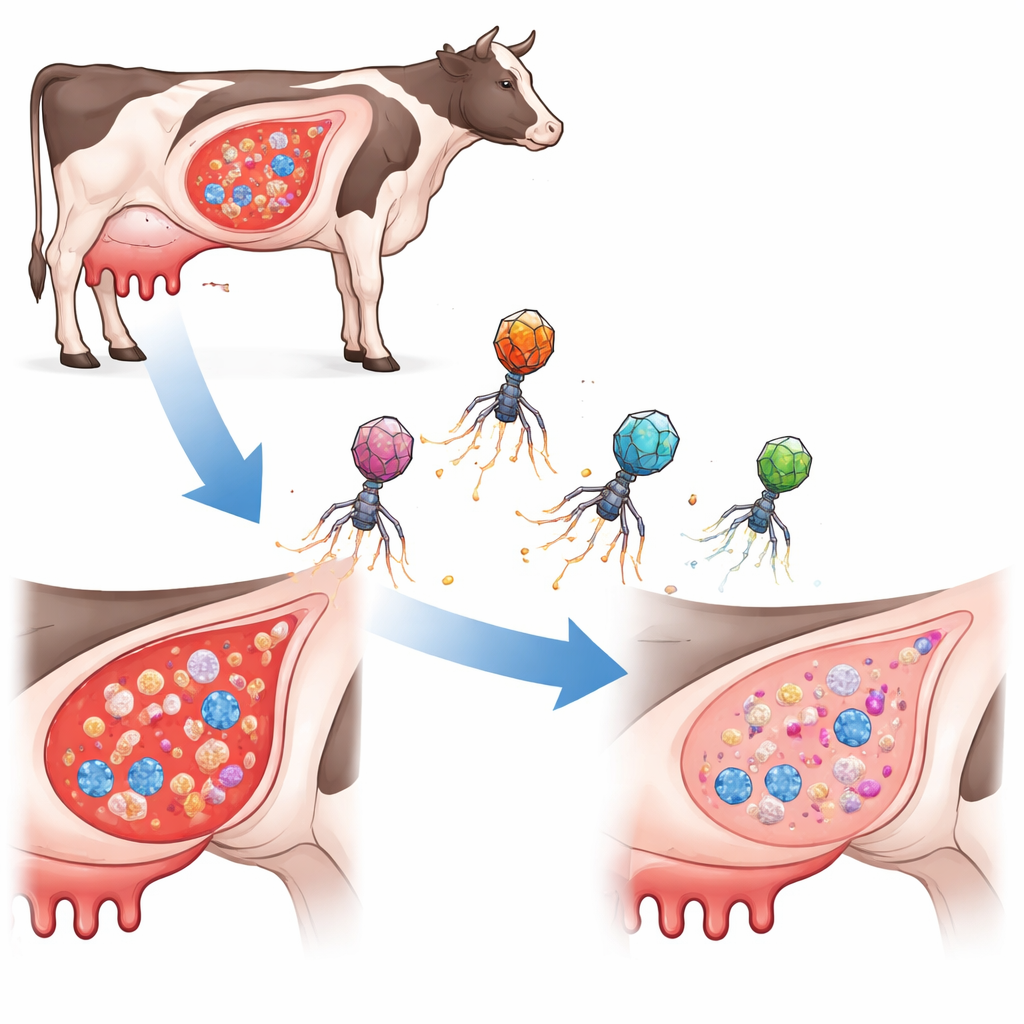
Hedefe Yönelik Yeni Bir Bakteri Avcısı Türü
Geleneksel antibiyotikleri veya sıradan bakteriyofajları (bakterileri enfekte eden virüsler) kullanmak yerine araştırmacılar, fag kabukları içinde DNA taşıyan küçük elemanlar olarak bilinen fag‑indüklenebilir kromozomal adacıkları mühendisliklediler. Doğada bu adacıklar, bakteriler arasında geçiş yapmak için fag kabuklarına atlayarak yolculuk ederler. Burada ekip, CRISPR‑Cas9 gen‑düzenleme aracını ve S. aureus içindeki üç küçük ama önemli düzenleyici RNA’yı hedefleyen kısa yönlendirici dizileri taşıyan “ePICI”ler olarak yeniden tasarladı. Bir ePICI hedef hücreye girdiğinde Cas9 üretilir ve seçilen bölgede bakterinin kromozomunu keser; hücreyi içeriden öldürür. Kritik olarak, bu mühendislik ürünleri kendi başlarına çoğalmaz, bu da yayılmalarını sınırlayarak zararlı genlerin yanlışlıkla taşınma riskini azaltır.
Bakteriyel Kalkanın Mücadeleyi Nasıl Değiştirdiği
S. aureus sıklıkla biyofilmler oluşturarak tedaviden kurtulur—hücrelerin kendi yaptıkları bir matriks içinde gömülü olduğu yapışkan topluluklar. Ekip iki yaygın matriks türünü karşılaştırdı: esas olarak Bap adlı bir proteinden oluşan bir tür ve PIA/PNAG olarak bilinen bir şeker polimerinden oluşan diğer tür. Laboratuvar testlerinde Bap‑çağrışımlı biyofilmler, ePICI’lere ve standart bir yardımcı faga karşı bakterileri güçlü şekilde koruyarak enfeksiyonu engelleyen yoğun bir zırh gibi davrandı. Buna karşın şeker polimerine dayanan biyofilmler, viral kabuklardaki enzimlerin bu şekerleri parçalayarak parçacıkların hedeflerine ulaşmasına yardımcı olabileceği için bakterileri öldürmeyi daha kolay hale getirdi.
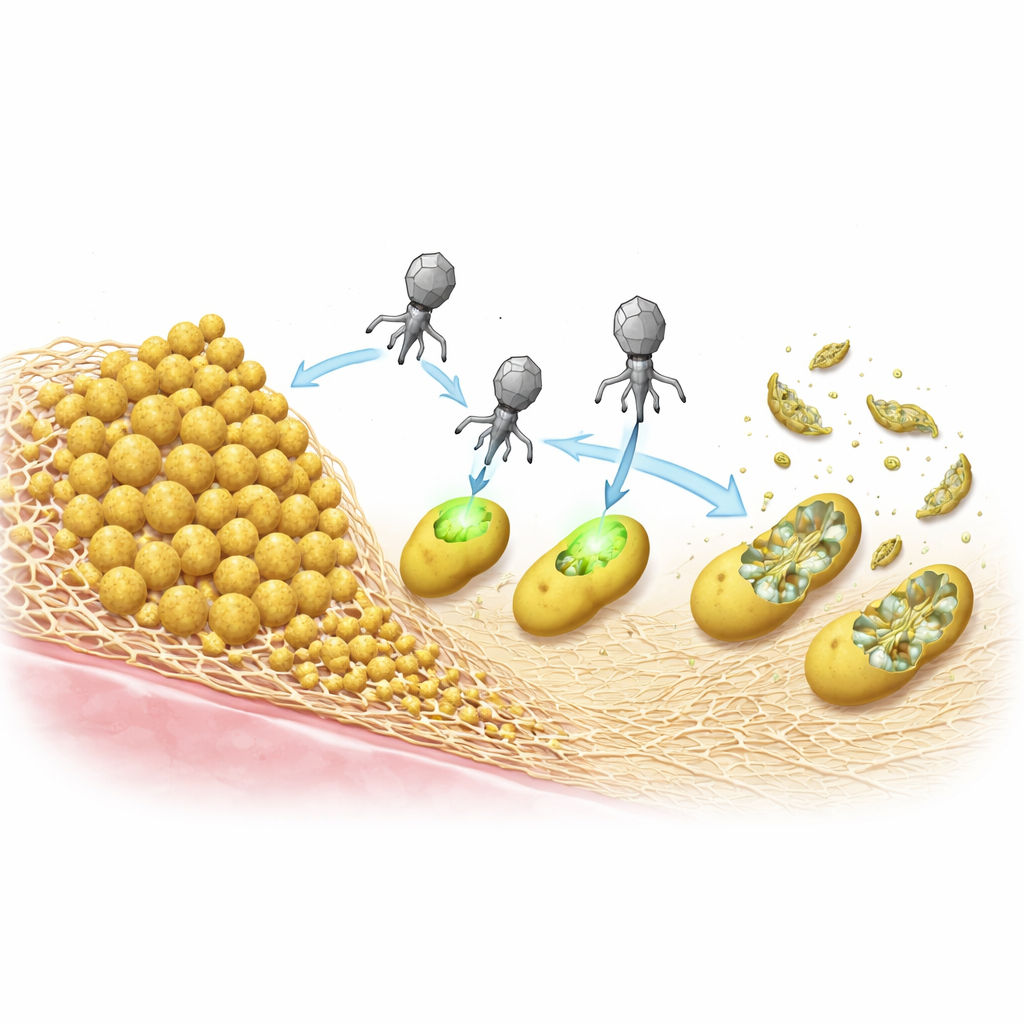
DNA’larına Katılmadan Bakterileri Öldürmek
Bir hücre içine girdikten sonra ePICI’ler bakteriyel kromozoma entegre olabiliyor, ancak araştırmacılar bu adımın gerçekten öldürme için gerekli olup olmadığını sordular. Entegre olamayan bir versiyon yarattılar ve parçacığın kaynak suşta doğru şekilde üretildiği sürece orijinali kadar öldürücü olduğunu gösterdiler. Bu, CRISPR sisteminin gelen dairesel DNA’dan doğrudan ifade edilebileceği, görevini yapabileceği ve hücre ölürken kaybolabileceği anlamına geliyor. Entegrasyonsuz bu eylem, istem dışı gen transferi olasılığını daha da düşürür ve bu parçacıkları viral çoğalma ve hücre lizisine dayanan klasik fag terapisinden ayırır.
Petri Kabından Enfekte Meme Bezlerine
Bap üreten suşların süt mastitinde yaygın olması nedeniyle ekip, en iyi performans gösteren yapılarından biri olan ePICIrsaE’yi meme enfeksimini taklit eden bir fare modelinde test etti. Sütte ve laboratuvar kültürlerinde Bap‑zengin biyofilmler açıkça ePICI etkinliğini zayıflattı. Buna rağmen meme bezinin içinde tekrarlanan ePICIrsaE dozları, Bap üretenler de dahil olmak üzere test edilen tüm suşlarda bakteri sayısını keskin bir şekilde azalttı. Etkisi güçlü son basamak antibiyotik vancomycin ile karşılaştırılabilirdi. Sonuçlar, canlı dokudaki koşulların—daha düşük Bap üretimi, serbest yüzen bakterilerin varlığı ya da sütte bulunan yardımcı bileşenler gibi—mühendislenmiş parçacıkların statik laboratuvar biyofilmlerine kıyasla çok daha iyi çalışmasına izin verdiğini gösteriyor.
Çiftlikler ve Ötesi İçin Ne Anlama Gelebilir
Çalışma, çoğalmayan, fagla paketlenmiş CRISPR sistemlerinin kendilerini yaymadan veya büyük sayıda hücreyi aynı anda patlatmadan biyofilm ilişkili zor bir enfeksiyon olan S. aureus’u seçici olarak ortadan kaldırabileceğini gösteriyor. Yüksek parçacık dozlarının gerektiği ve farelerden ineklere ölçeklendirmenin zorlu olacağı kabul edilse de, bu parçacıklar mastitis gibi lokalize enfeksiyonlar için antibiyotiklere alternatif olarak umut verici ve kontrol edilebilir bir seçenek sunuyor. Daha geniş anlamda, basit laboratuvar testlerinde hayal kırıklığı yaratan tedavilerin hayvanın karmaşık ortamında yine de başarılı olabileceğini vurguluyor ve farklı bakteriler, viral kabuklar ve yönlendirici dizilere uyarlanmış özelleştirilmiş ePICI kütüphanelerinin kapısını aralıyor.
Atıf: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Anahtar kelimeler: sığır mastiti, Staphylococcus aureus, CRISPR tedavisi, fag tabanlı tedavi, biyofilm enfeksiyonları