Clear Sky Science · tr
Etiket kullanmadan optik metabolik görüntüleme ile canlı bakterilerin gerçek zamanlı, yüksek çözünürlüklü metabolik karakterizasyonu
Germlerin Gerçek Zamanlı Tepkilerini İzlemek
Bakteriler vücudumuzun üzerinde ve içinde her yerde bulunur ve sessizce sağlığımızı şekillendirir. Besinleri sindirmeye yardımcı olurlar, cildimizi korurlar ve bazen antibiyotiklere direnç gösteren inatçı enfeksiyonlara yol açarlar. Bu çalışma, canlı bakterilerin stres ve ilaçlara karşı tepkilerini tek tek hücre düzeyinde, boyar madde veya etiket eklemeden gerçek zamanlı izlemenin bir yolunu tanıtıyor. Bu yetenek, zamanla doktorların doğru tedaviyi daha hızlı seçmesine yardımcı olabilir ve bazı enfeksiyonların neden bu kadar zor iyileştiğini anlamada bilim insanlarına ipucu verebilir.
Bakteri Yaşamına Işıkla Bakmak
Araştırmacılar boyalar veya genetik etiketler eklemek yerine bakterilerin içindeki belirli moleküller lazer ışığıyla uyarıldığında doğal olarak çok zayıf bir şekilde parladıkları gerçeğine dayanıyor. NAD(P)H ve FAD olarak bilinen bu moleküllerden ikisi, hücrelerin besini enerjiye dönüştürme süreçlerinde merkezi rol oynar. Hızlı, yüksek çözünürlüklü lazer mikroskobu kullanılarak ekip, bu parlaklığın hem yoğunluğunu hem de bu parlama sinyalinin çok kısa zaman gecikmesini ölçebiliyor; bu da bir hücrenin metabolizmasının ne kadar aktif olduğunu ortaya koyuyor. Yöntem etiket gerektirmediği ve tahrip edici olmadığı için aynı canlı bakteriler çevreleri değiştikçe saniyeler ve dakikalar içinde izlenebiliyor. 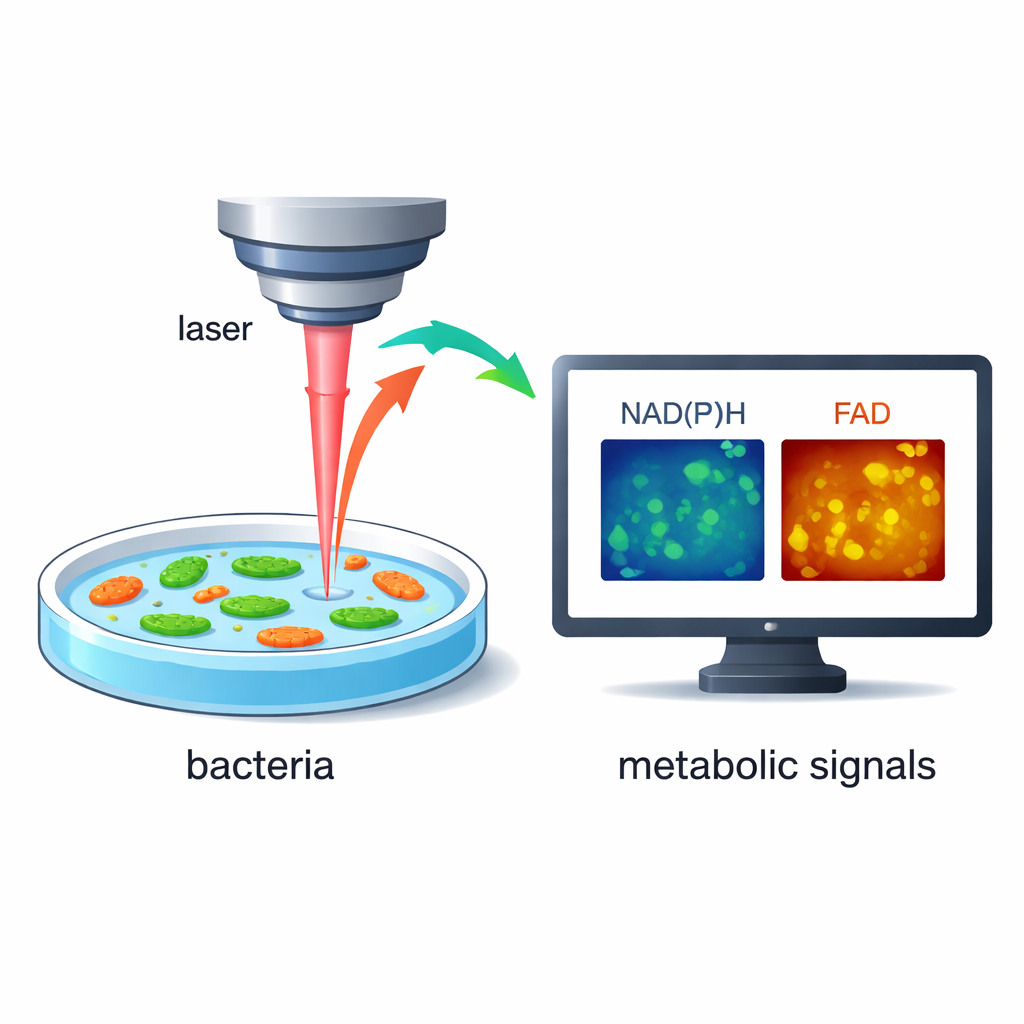
Bireysel Bakteriler Arasındaki Farkları Görmek
Çoğu standart laboratuvar testi milyonlarca bakteriyi bir arada değerlendirir ve yalnızca ortalama bir yanıt bildirir. Burada yazarlar, görüntüleme yöntemlerinin sıvı kültürde tek tek Staphylococcus aureus hücrelerini ayırt ederek her birini ayrı ayrı analiz edebildiğini, hatta yüksek hücre yoğunluklarında bile bunu yapabildiklerini gösteriyor. Aynı koşullarda yetiştirilen iki S. aureus kolonisini karşılaştırdıklarında, FAD’dan gelen bir ana sinyal koloniler arasında farklılık gösterdi ve her koloni içinde değerlerin dağılımı vardı. Bu, aynı şişe içinde genetik olarak benzer bakterilerin bile çok farklı metabolik durumlarda olabileceği anlamına geliyor; bu gizli çeşitlilik standart toplu testlerin kaçırabileceği ancak enfeksiyonların tedaviye yanıtı açısından önemli olabilecek bir fark oluşturuyor.
Antibiyotiklerin Saniyeler İçinde Etki Etmesini İzlemek
Ekip daha sonra tek tek S. aureus hücrelerini, yaygın antibiyotikler ve ev tipi çamaşır suyu dahil olmak üzere birkaç antimikrobiyal işlemle karşılaştıklarında izledi. Hızlı görüntüleme düzeneklerini kullanarak, ilaç çözeltisi hücrelere dokunduğu andan itibaren sonraki 30 dakikayı kapsayan değişiklikleri yakaladılar. Güçlü tedaviler NAD(P)H sinyallerinin düşmesine ve FAD sinyallerinin yükselmesine neden oldu; bu genellikle saniyeler içinde gerçekleşti ve enerji üretiminin aksadığını ve hücre içinde daha okside bir duruma kayıldığını yansıttı. Bu değişikliklerin tam zamanlaması ve deseni ilaç türüne ve doza bağlıydı: örneğin proteinleri engelleyen ve hücre duvarını hedef alan antibiyotikler kısa bir düşüş ve kısmi iyileşme oluştururken, çamaşır suyu keskin ve kalıcı bir değişime yol açtı. Bu ayırt edici “ışık imzaları”, tekniğin hücrelerin stres altında mı yoksa ölüp ölmedikleri dışında nasıl zarar gördüklerini de algılayabileceğini gösteriyor. 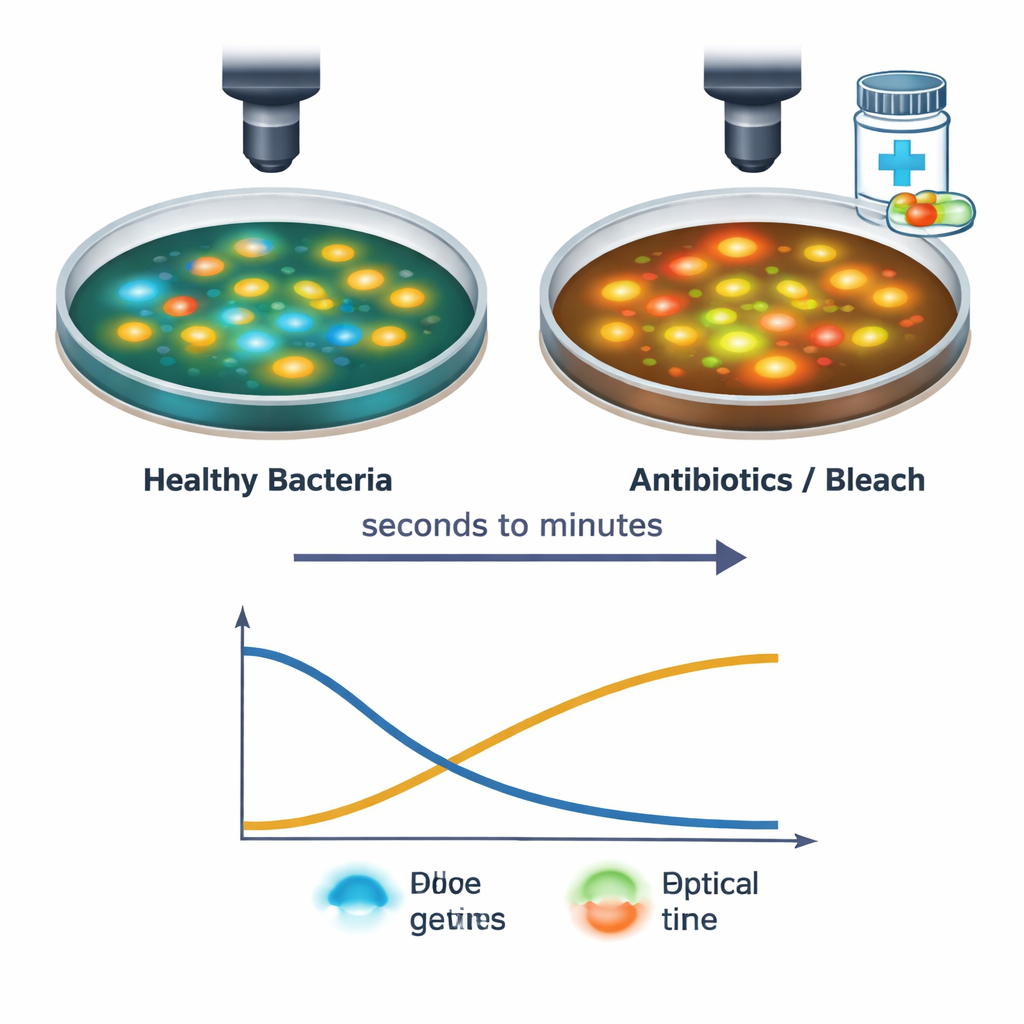
Biyofilmlerin Gizli Dünyasına Bakmak
Bakteriler doğada nadiren yalnız yaşar; bunun yerine tıbbi implantlardan dişlere kadar yüzeylerde biyofilm adı verilen sümüksü, koruyucu topluluklar oluştururlar. Bu yoğun katmanlarda bazı hücreler son derece aktifken diğerleri uyku halinde olabilir; bu karışım topluluğun antibiyotiklere karşı hayatta kalmasına yardımcı olur. Araştırmacılar geniş birleştirilmiş görüntüler kullanarak S. aureus biyofilm içindeki metabolik manzarayı haritaladı ve bunu serbest yüzen hücrelerle karşılaştırdı. Parlak, metabolik olarak aktif ceplerin daha az aktif bölgelerle çevrelendiğini buldular ve birkaç tür arasında biyofilm bakterilerinin serbest yaşayan muadillerine göre daha okside bir metabolik profil eğiliminde olduğunu gösterdiler. Ek optik sinyaller ekstra lipidler ve proteinleri işaret etti; bu da biyofilmleri bir arada tutan yapıştırıcı benzeri maddeyle tutarlı bir bulgu.
Geleceğin Tıbbı İçin Neden Önemli
Bu bulgular birlikte, etiket gerektirmeyen optik metabolik görüntülemenin bakterilerin nasıl yaşadıklarına, uyum sağladıklarına ve öldüklerine dair hızlı, ayrıntılı ve invazif olmayan anlık görüntüler sağlayabileceğini gösteriyor. Genel okuyucu için ana mesaj, bilim insanlarının artık hücreleri rahatsız etmeden, sadece dikkatle ayarlanmış ışık kullanarak bakterilerin enerji kullanımını gerçek zamanlı “dinleyebildikleri”dir. Uzun vadede bu tür bir teknoloji, kültürde zor üreyen bakterileri tanımlamaya, biyofilm içindeki ilaç toleranslı hücre ceplerini tespit etmeye veya bir hastanın enfeksiyonunun farklı antibiyotiklere nasıl cevap verdiğini hızlıca test etmeye yardımcı olabilir. Bu, daha hızlı ve daha kişiselleştirilmiş tedavileri destekleyebilir ve her gün sağlığımızı etkileyen görünmez mikrobiyal dünyaları daha derinlemesine anlamamıza katkıda bulunabilir.
Atıf: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
Anahtar kelimeler: bakteriyel metabolizma, optik görüntüleme, biyofilm, antibiyotik yanıtı, mikrobiyom