Clear Sky Science · tr
Enzim destekli antibiyotik tedavisi, implant ilişkili enfeksiyon modelinde biyofilmleri algılanamayan düzeye indiriyor
İnatçı implant enfeksiyonlarının önemi
Kalça ve diz protezleri yaşamları değiştirir; ancak bakteriler bu metal implantları kolonize ettiğinde, biyofilm adı verilen yapışkan topluluklar oluşturabilirler. Bu biyofilmler, mikropları hem bağışıklık sistemi hem de antibiyotiklerden koruyan zırhlı şehirler gibi davranır; bu da ağrılı, uzun süreli ve tedavisi çok zor enfeksiyonlara yol açar. Bu çalışma, önce biyofilm savunmasını parçalamaya yardımcı olan, ardından çevreyi yüksek doz antibiyotiklerle dolduran iki aşamalı yeni bir tedaviyi araştırıyor—bu yaklaşım bir gün implantların değiştirilmesi yerine kurtarılmasına yardımcı olabilir.
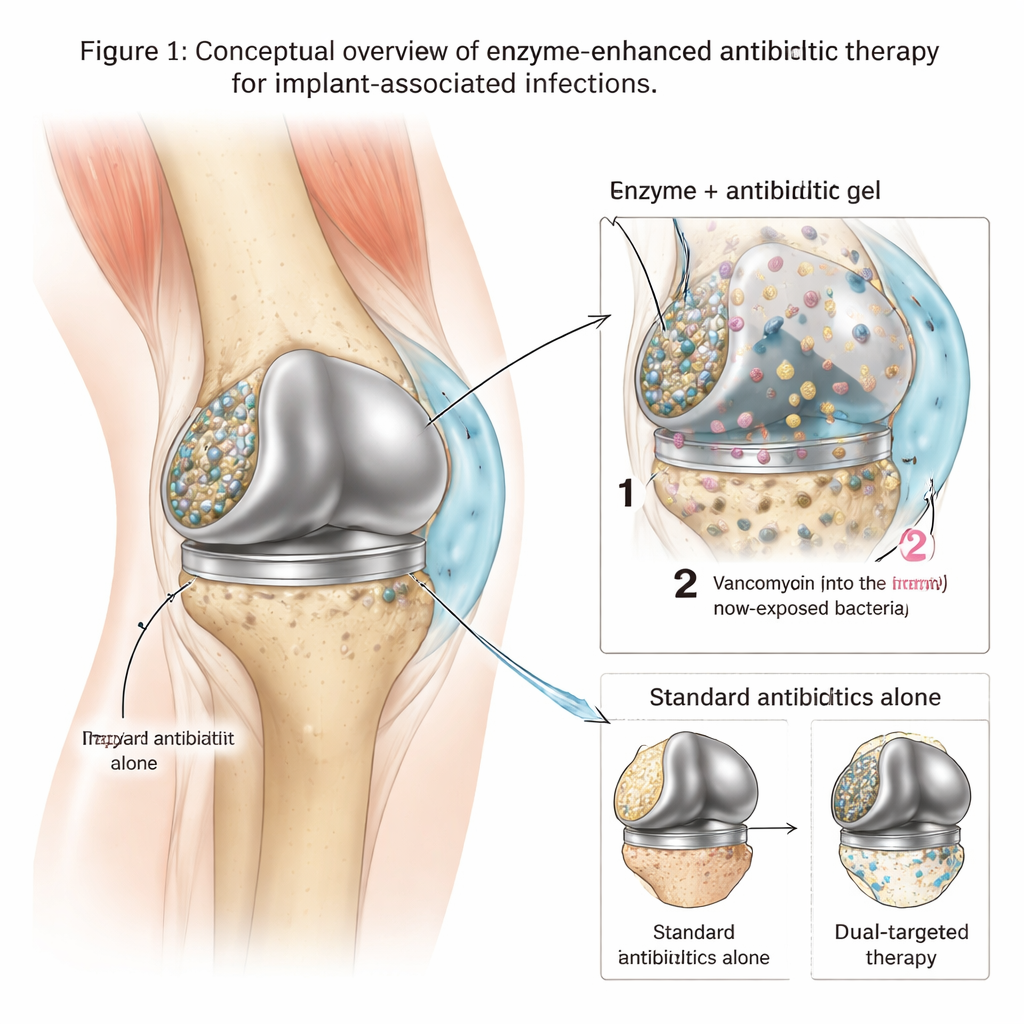
Metal implantlardaki gizli mevziler
Methicillin‑dirençli Staphylococcus aureus (MRSA) gibi bakteriler yapay bir eklem yüzeyine tutunduğunda, hızla metal yüzey üzerinde DNA, şekerler ve diğer moleküllerden oluşan yapışkan bir matris oluştururlar. Bu korunmuş biyofilm içinde bakteriler yavaş büyür, davranışlarını değiştirir ve serbest yüzen mikropları öldüren düzeylerin yüzlerce hatta binlerce katı kadar yüksek antibiyotik düzeylerine tolerans gösterebilirler. Sonuç olarak standart tedaviler—vankomisin gibi güçlü ilaçlar bile—enfeksiyonu tamamen temizleyemeyebilir ve hastaları tekrarlayan ameliyatlara veya implantın tamamen değiştirilmesine zorlar. Doktorların, sadece bakterileri öldürmekle kalmayıp aynı zamanda ilaçların onlara ulaşabilmesi için koruyucu kaleyi açan araçlara ihtiyaçları var.
Enzim ve antibiyotik taşıyan akıllı jel
Araştırmacılar, poloksamer 407 adı verilen bir bileşikten yapılan termosensitif bir hidrojel etrafında yerel bir tedavi tasarladı. Bu jel soğukken sıvıdır, bu da implant çevresine enjekte etmeyi kolaylaştırır; ancak vücut sıcaklığında hızla yumuşak bir katı haline gelerek yerinde kalmasına yardımcı olur. Bu jelin içine ekip iki ana bileşen yükledi: güçlü bir antibiyotik (vankomisin) ve biyofilm matrisinin ana bileşenlerini parçalayan üç enzimin karışımı. Laboratuvar testlerinde, enzimlerin önce salınması—biyofilmi gevşetip inceltmesi—ve vankomisinin daha yavaş, birkaç gün boyunca salınarak bakterilerin yaşadığı yerde çok yüksek yerel ilaç düzeylerini koruması için jeli ayarladılar.
Laboratuvar kaplarından kobaylara
Stratejinin gerçekten işe yarayıp yaramadığını görmek için ekip önce laboratuvarda titanyum parçaları üzerinde büyütülen biyofilmler üzerinde, sonra da enfekte implantları taklit eden bir kobay modelinde test etti. In vitro olarak, enzim‑antibiyotik jelin 48 saat ara ile iki uygulanması, metal yüzeylerdeki canlı bakteri sayısını 100.000’den fazla kat azalmaya uğrattı ve biyofilm kütlesini neredeyse yok etti. Hayvanlarda, araştırmacılar deri altına titanyum boncuklar içeren delikli kafesler cerrahi olarak yerleştirdiler, bunları MRSA ile enfekte ettiler ve sonra sistemik antibiyotikler ile yerel jellerin farklı kombinasyonlarıyla tedavi ettiler. En etkili rejim şunların birleşimiydi: (1) hem enzim hem de vankomisin içeren yerel jel, iki kez uygulandı ve (2) vankomisin ile birlikte vücut genelini kapsayan ikinci bir antibiyotik olan rifampisinle yapılan tedavi; rifampisin biyofilmlere özellikle iyi nüfuz eder.
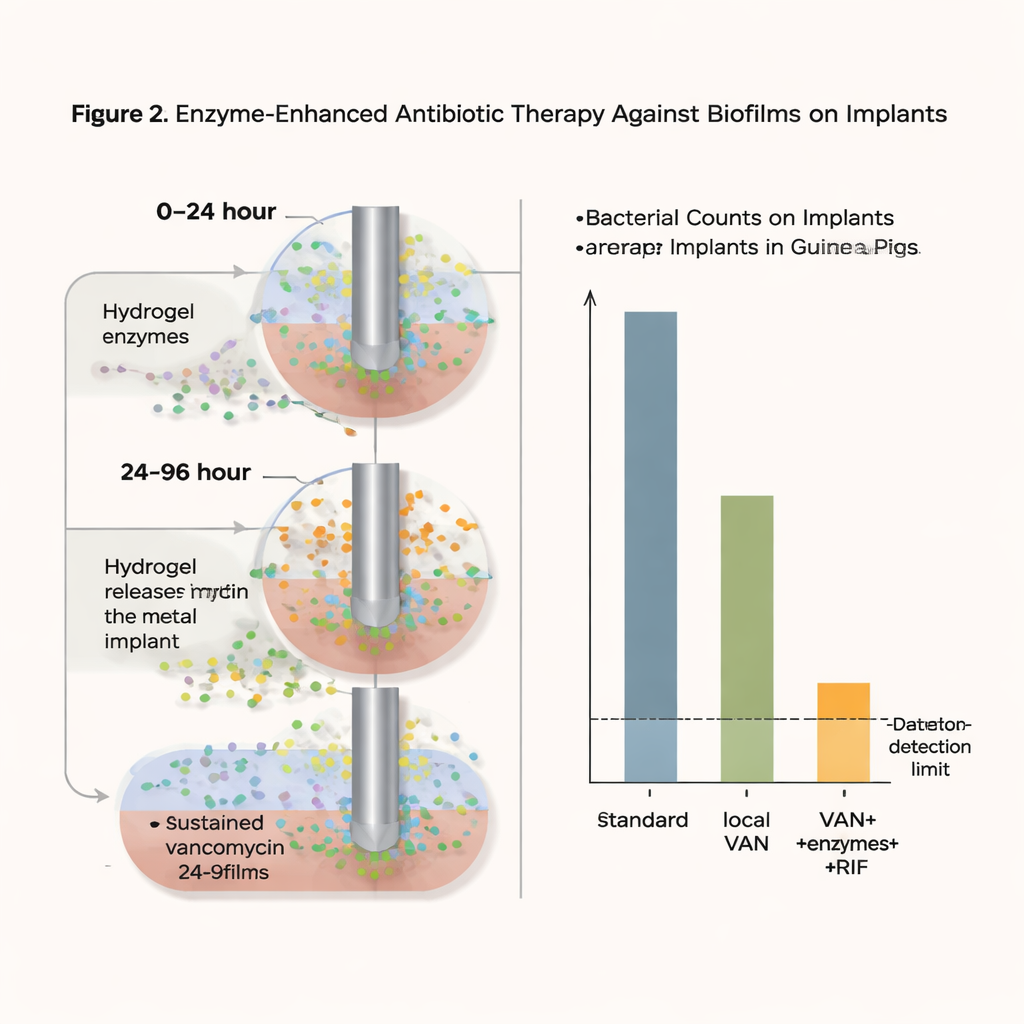
Yeni yaklaşımın elde ettikleri
Bu yoğun fakat lokalize stratejiyle, implant malzemesi üzerindeki bakteri sayıları tespit sınırına kadar düştü—bu modelde etkili olarak “geri kazanılabilir bakteri yok”—tedavinin bitiminden bir gün sonra tedavi edilen kafeslerin yüzde 75’inde ve beş gün sonra bile yüzde 37,5’inde. Önemli olarak, vankomisine karşı antibiyotik direncinde herhangi bir artış gözlenmedi ve yüksek yerel vankomisin düzeyleri rifampisine dirençli suşların ortaya çıkmasını önlüyor gibi görünüyordu. Kültür hücreleri ve rekonstrükte insan cildi modeli kullanılarak yapılan güvenlik testleri, jel formülasyonlarından toksisite veya tahriş belirtisi bulmadı. Hafif bir bakteri yeniden büyümesi bazı vakalarda hâlâ görüldü ve tedavi süresi hastaların tipik olarak aldığı süreden daha kısaydı; yine de sonuçlar, biyofilmi parçalayan enzimlerin sürekli lokal antibiyotik verimiyle birleştirilmesinin aksi takdirde inatçı olan enfeksiyonları dramatik biçimde azaltabileceğini gösteriyor.
Bu hastalar için ne anlama gelebilir
İmplant ilişkili enfeksiyonlarla karşı karşıya kalan kişiler için bu çalışma, cerrahların enfekte eklem etrafına akıllı bir jel enjekte edebileceği bir geleceğe işaret ediyor; donanımı derhal çıkarmak veya değiştirmek yerine. Önce biyofilm kalkanını zayıflatıp sonra bölgeyi yüksek, sürdürülebilir antibiyotik dozlarıyla—tüm vücut tedavisiyle desteklenen—doldurarak bu çift hedefli strateji, bakteri sayısını algılanamayan düzeye çekmeyi ve direnç riskini azaltmayı amaçlıyor. Daha fazla çalışma, daha uzun tedaviler ve insan denemeleri hâlâ gerekse de, bu yaklaşım en ısrarcı ortopedik enfeksiyonların bazılarının daha yönetilebilir ve potansiyel olarak tedavi edilebilir sorunlara dönüştürülmesi için umut verici bir yol haritası sunuyor.
Atıf: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Anahtar kelimeler: biyofilm enfeksiyonu, ortopedik implantlar, vankomisin, enzimatik tedavi, rifampisin