Clear Sky Science · tr
Çok katmanlı moleküler profilleme, desmoplastik küçük yuvarlak hücreli tümörün tanısını ve hedefe yönelik tedavisini aydınlatıyor
Niteliği düşük, daha iyi yanıtlar bekleyen nadir bir kanser
Desmoplastik küçük yuvarlak hücreli tümör (DSRCT), çoğunlukla çocukları, ergenleri ve genç yetişkinleri etkileyen son derece nadir ve agresif bir kanserdir. Oldukça nadir olması ve mikroskop altında diğer tümörleri taklit edebilmesi nedeniyle hekimler doğru tanı koymakta ve etkili tedavileri seçmekte sık sık zorlanır. Bu çalışma basit ama güçlü bir soruyu ortaya koyuyor: DSRCT tümörlerini yalnızca DNA değil, aynı zamanda RNA, protein desenleri ve DNA üzerindeki kimyasal işaretler gibi birden çok moleküler düzeyde derinlemesine analiz edersek, hem tanıyı keskinleştirebilir hem de standart tedaviler tükenmiş hastalar için yeni, daha hassas tedavi seçenekleri keşfedebilir miyiz?
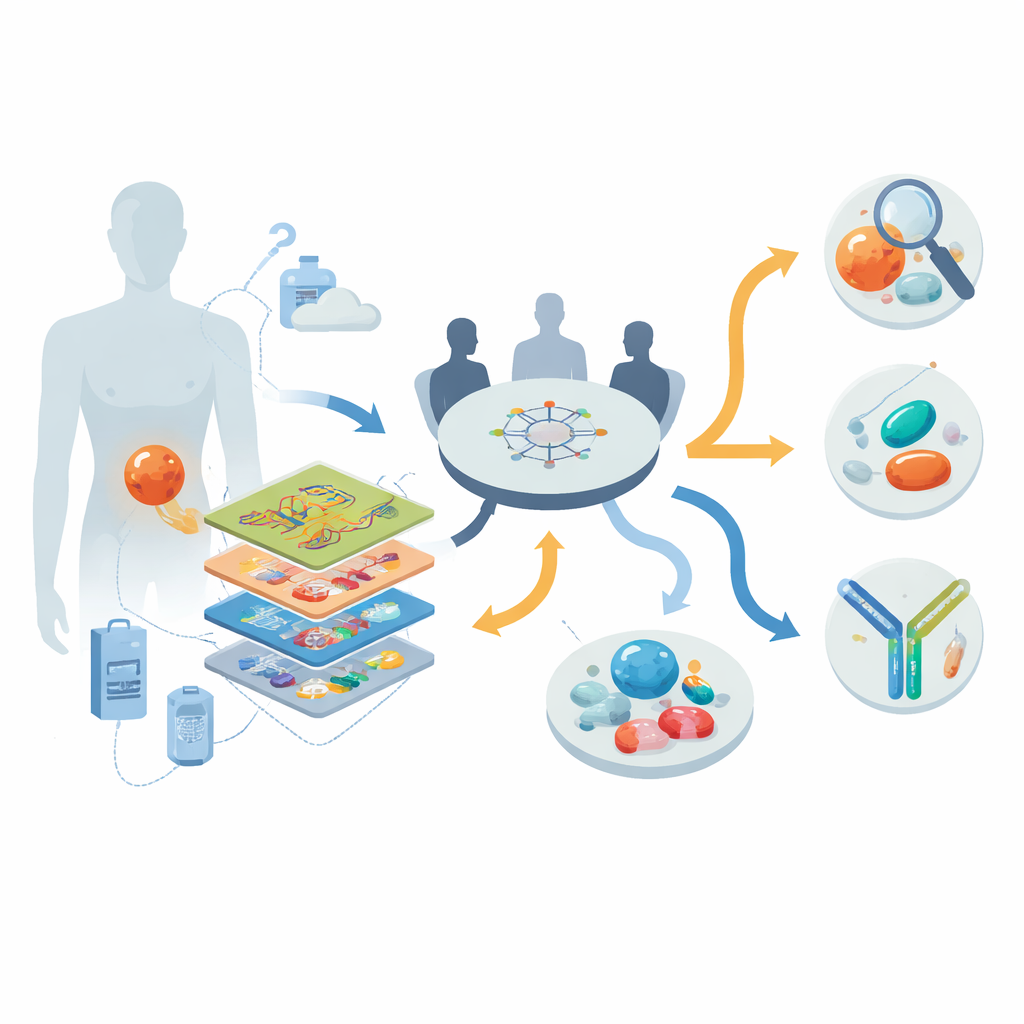
Tümörleri katman katman incelemek
Araştırmacılar, 2013 ile 2022 yılları arasında Almanya’daki ulusal bir kişiselleştirilmiş onkoloji programı kapsamında, ileri evre ve çoğunlukla tedaviye dirençli 30 kişiyi çalışmaya dahil ettiler. Her hasta için bir “çoklu omik” araç takımı uygulandı: DNA’yı incelemek için tüm genom veya ekzon dizilemesi; hangi genlerin aktif olduğunu göstermek için RNA dizilemesi; epigenetik parmak izlerini yakalamak için DNA metilasyon profillemesi; ve dokuz hastada hangi sinyal yollarının gerçekten aktif olduğunu açığa çıkaran ayrıntılı protein ve fosfoprotein ölçümleri. Çok disiplinli bir tümör kurulu, bu verileri her hastanın klinik geçmişiyle birlikte gözden geçirerek tanının netleştirilmesi, hedefe yönelik ilaç önerileri ve klinik denemeler için bireyselleştirilmiş öneriler oluşturdu.
Yanlış tanıları düzeltmek ve gizli hedefleri açığa çıkarmak
Çarpıcı bulgulardan biri, derin profillemenin özgün tanıyı ne sıklıkla düzelttiğiydi. 30 hastanın sekizinde, başlangıçta kaynağı bilinmeyen kanserler veya belirsiz sarkomlar gibi başka varlıklar olarak etiketlenen tümörler, EWSR1::WT1 gibi ayırt edici bir gen füzyonu ve karakteristik bir metilasyon deseni tespit edildikten sonra DSRCT olarak yeniden sınıflandırıldı. Aynı zamanda, bu tümörlerin DNA’sı nispeten sessiz çıktı: az sayıda mutasyon ve sadece aralıklı kopya sayısı değişiklikleri vardı; bu nedenle klasik "mutasyonlu gen = ilaç hedefi" yaklaşımları çok az sonuç verdi. Bunun yerine en zengin ipuçları RNA ve protein katmanlarından geldi. DSRCT’deki gen aktivitesini yüzlerce diğer sarkomla karşılaştırarak, mevcut veya geliştirilen ilaçlarla teorik olarak hedeflenebilecek çeşitli yüzey molekülleri ve sinyal enzimlerinin tekrarlayan aşırı ekspresyonu saptandı.
Moleküler sinyallerden kişiye özel tedavilere
Bu desenlere dayanarak, tümör kurulu 30 hastanın 28’i için 107 moleküler bilgilendirilmiş yönetim önerisi sundu. Önerilerin çoğu, hücre büyümesini ve damar oluşumunu yönlendiren anahtar enzimler olan tirozin kinazlarını bloke eden ilaçları veya yüksek düzeyde ifade edilen yüzey proteinlerine tutunan daha yeni stratejileri içeriyordu. Örnekler arasında pazopanib gibi küçük moleküllü kinaz inhibitörleri; somatostatin reseptörlerine yönelik peptit bazlı radyoterapi; adezyon molekülü CLDN6’yı hedefleyen deneysel CAR T hücreleri; ve ERBB2 (HER2) reseptörünü taşıyan hücrelere toksin teslim eden antikor–ilaç konjugatları yer aldı. On yedi hasta, biyobelirteç ile eşleştirilmiş klinik çalışmalara uygun bulundu; bu durum, ayrıntılı moleküler verilerin ultra-nadir bir hastalıkta erişilmesi zor olabilecek çalışmalara kapı açabileceğini vurguluyor.
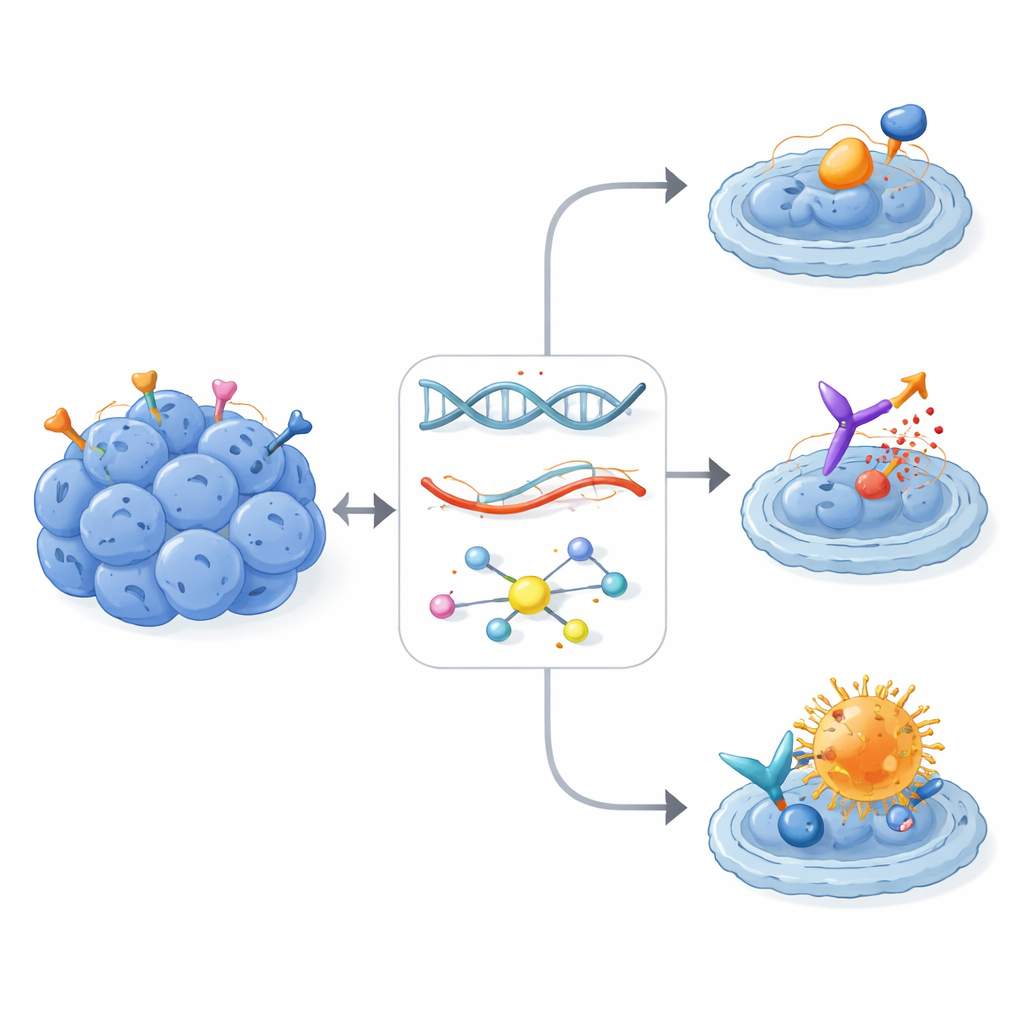
Ağır önceden tedavi görmüş hastalarda gerçek dünya etkisi
Tavsiye edilen kişiselleştirilmiş tedavilerden 16’sı aslında 13 hastaya uygulandı; bunların tümü RNA düzeyindeki sinyallerle yönlendirildi ve bazen fosfoprotein verileriyle daha da netleştirildi. Bu bireyler çok sayıda kemoterapi ve lokal tedavi süreçlerinden geçmiş olmalarına rağmen, 13 hastadan sekizi hastalık kontrolü elde etti—beşi kısmi tümör küçülmesi, üçü stabil hastalık gösterdi. Çok hedefli tirozin kinaz inhibitörleri, çoğunlukla pazopanib, özellikle ilacın bilinen hedefleri tümörde açıkça aşırı aktif olduğunda birkaç hastada anlamlı ve bazen uzun süreli fayda sağladı. Belki de en dikkat çekici olanı, yüksek ERBB2 ekspresyonu gösteren iki hastanın antikor–ilaç konjugatı trastuzumab deruxtecan (T‑DXd) almasıydı. Her iki hasta da birçok önceki tedavi hattını tüketmiş olmalarına ve ERBB2 reseptörünün klasik ERBB2 bloke edici ilaçlar için tipik olan güçlü aktivasyon desenini göstermemiş olmasına karşın iki yıl veya daha uzun süren uzamış yanıtlar yaşadı.
Hastalar ve gelecekteki bakım için anlamı
DSRCT’li kişiler için çalışma temkinli bir iyimser mesaj sunuyor. Bu kanserde sömürülebilecek bariz DNA mutasyonları az olsa da, birden çok moleküler katmana bakmak hem yanlış tanıları düzeltebilir hem de standart testlerle görünmeyen eyleme geçirilebilir zayıflıkları ortaya çıkarabilir. Çalışma, nadir ve agresif bir hastalıkta bile biyolojiye dayalı bir yaklaşımın pazopanib ve trastuzumab deruxtecan gibi ilaçlara karşı kalıcı yanıtlar dahil olmak üzere gerçek klinik fayda sağlayabileceğini gösteriyor. Daha geniş açıdan, DSRCT’li hastaların—ve dolayısıyla diğer ultra-nadir kanserlerin—kapsamlı moleküler profillemeye ve uzman değerlendirmeye düzenli erişiminden yararlanabileceğini, böylece tedavilerin yalnızca tümör tipine göre değil, her hastanın kanserinin benzersiz moleküler parmak izlerine göre seçildiği gelecekteki çalışmalar için yol açılabileceğini savunuyor.
Atıf: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
Anahtar kelimeler: desmoplastik küçük yuvarlak hücreli tümör, kişiselleştirilmiş onkoloji, çoklu omik profilleme, hedefe yönelik tedavi, antikor–ilaç konjugatları