Clear Sky Science · tr
SLC33A1’e bağlı ve bağımsız Golgi sialik asit O-asetilasyonunun CASD1 katalizi içindeki etkileşimi
Küçük şeker değişiklikleri sağlığı ve hastalığı nasıl şekillendirir
Hücrelerimizin yüzeyi, bağışıklık, gelişim ve hatta virüslerin bağlanmasını yönlendiren moleküler kimlik kartları gibi davranan karmaşık şeker zincirleriyle kaplıdır. Bu çalışma, bu şekerlere yapılan ince ama etkili bir değişikliği — terminal bir şeker olan sialik aside küçük kimyasal “kapakçıklar” yani asetil grupları eklemeyi — inceliyor ve hücrenin Golgi aygıtı içinde bu süreci kontrol eden sürpriz bir iki parçalı moleküler makineyi ortaya koyuyor. Bu gizli sistemi anlamak, bazı ağır nörolojik bozuklukları açıklamaya yardımcı oluyor ve hücrelerin yüzeylerini sağlık ve hastalık durumunda nasıl hassas biçimde ayarladığına dair ipuçları veriyor. 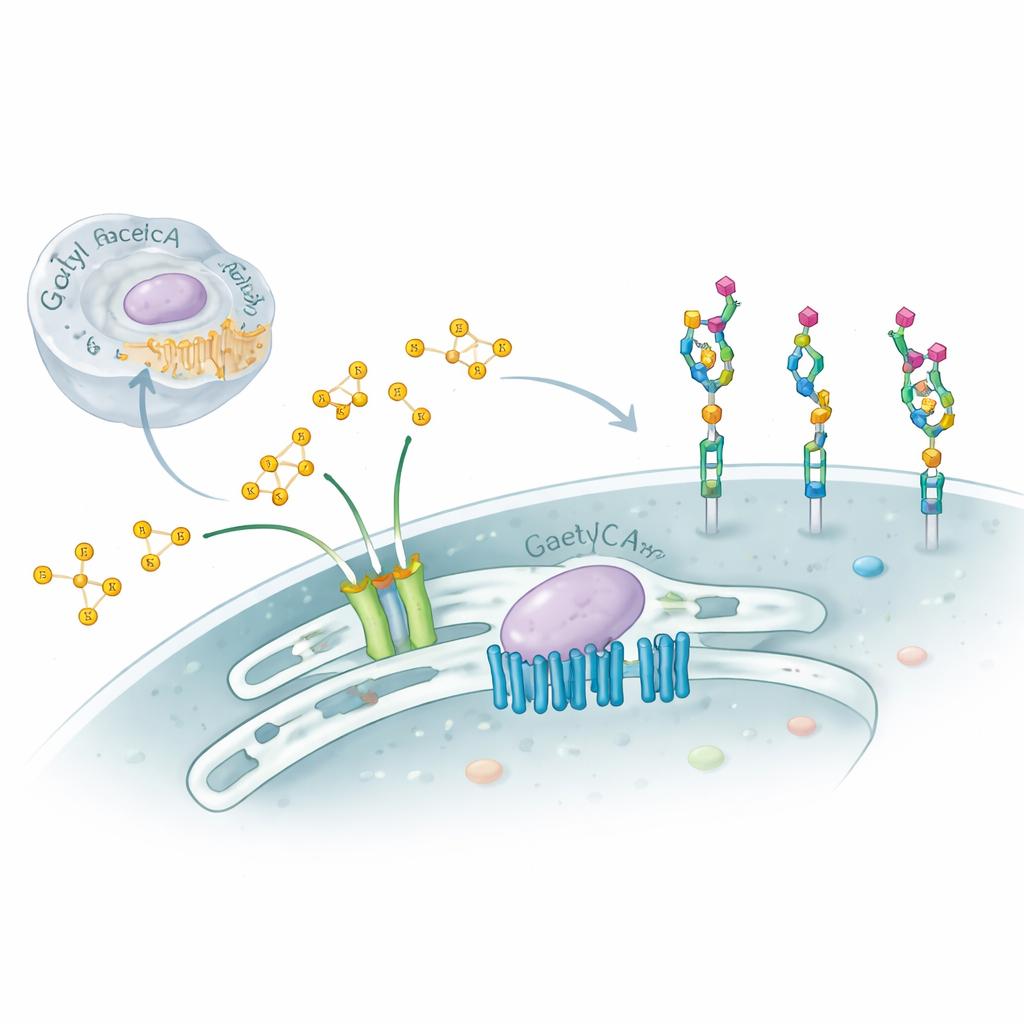
Hücre yüzeyindeki özel şekerler
Sialik asitler birçok protein ve lipitteki hücre yüzeyi şekerlerinin dış uçlarında bulunur; özellikle beyindeki gangliozit adı verilen moleküllerde yoğundur. Sialik asitleri hafifçe değiştirerek — örneğin belirli pozisyonlara bir veya iki asetil grubu ekleyerek — hücreler mevcut tanıma bölgelerini maskeleyebilir veya yeni tanıma bölgeleri oluşturabilir. İnfluenza C ve bazı koronavürüsler gibi virüsler özellikle bu modifiye şekerleri hedefler ve asetillenmiş gangliozitler sinir hücrelerinin yaşayıp yaşamamasını etkileyebilir ve kanser büyümesini yönlendirebilir. Buna rağmen, Golgi içinde bu asetil grupları yerleştiren hücresel makinenin iç işleyişi uzun süre iyi anlaşılamamıştır.
Bir taşıyıcı ve bir enzim el ele çalışıyor
Araştırmacılar Golgi içinde veya çevresinde bulunan iki proteine odaklandı: asetil‑CoA’yı (hücrenin temel asetil bağışlayıcısı) membranlar aracılığıyla taşıyan taşıyıcı SLC33A1 ve sialik asitlere asetil grupları aktardığı bilinen enzim CASD1. İnsan ve hamster hücre hatlarında gen düzenlemesi kullanarak SLC33A1’i ortadan kaldırdılar ve belirli gangliozitlerde ne olduğunu izlediler. SLC33A1 olmayan hücreler temel gangliozitler GD3 ve GD2’yi hâlâ üretebiliyor, ancak kanser ve sinir fonksiyonuyla ilişkilendirilen bir belirteç olan 9‑O‑asetillenmiş formlarını tamamen kaybetti. İnsan SLC33A1’i yeniden eklemek bu asetillenmiş gangliozitleri geri getirerek SLC33A1’in bu yol için kritik bir asetil‑CoA tedarikçisi olduğunu gösterdi. 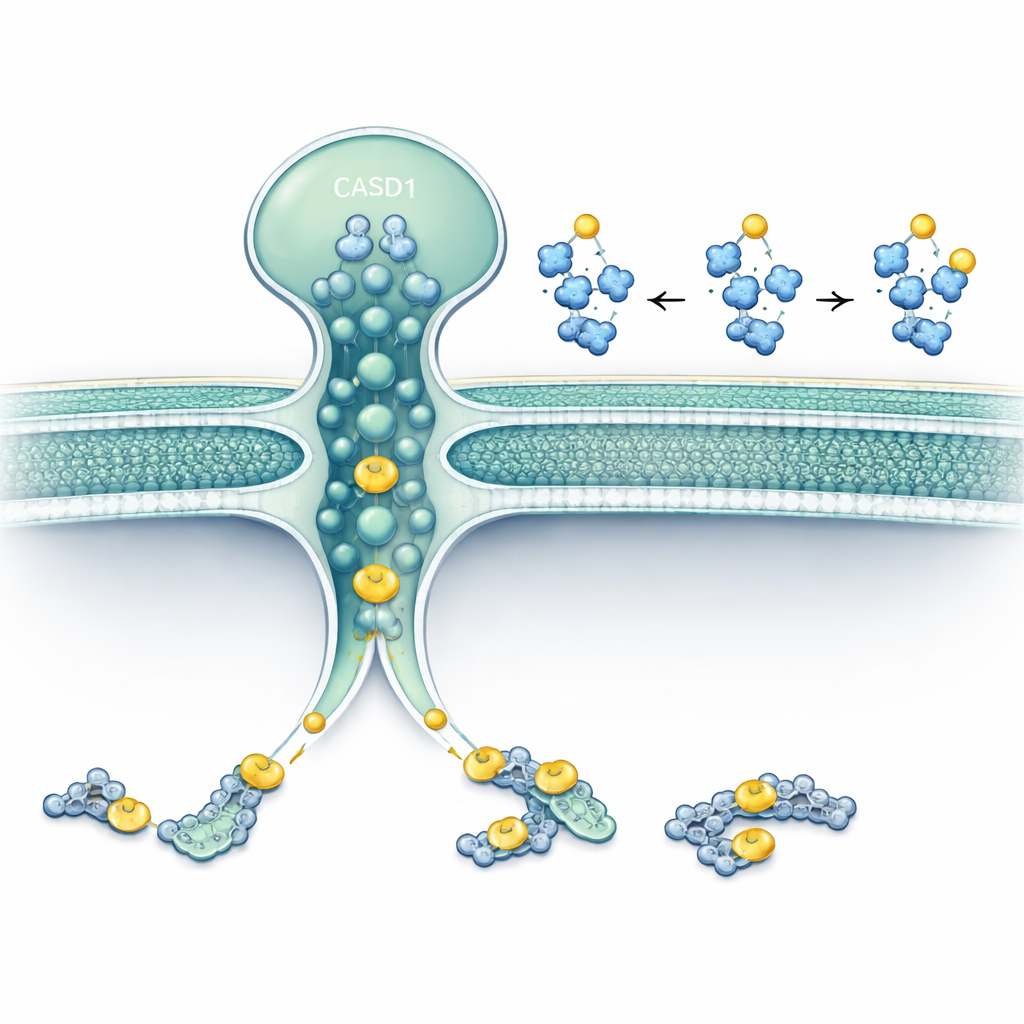
Hastaların mutasyonları tıbbi önemi ortaya koyuyor
SLC33A1 birkaç nadir nörolojik durumda rol oynar; bunlar arasında ağır çocukluk dönemi hastalığı (Huppke–Brendel sendromu), ailesel spastik parapleji formlarından biri ve geç başlangıçlı serebellar ataksi yer alır. Ekip, normal taşıyıcıdan yoksun hücrelerde dört hasta kaynaklı SLC33A1 varyantını yeniden yarattı ve bu değişmiş proteinlerin gangliozit asetilasyonunu geri getirebilip getirmediğini test etti. Dörtünün tamamı azalmış fonksiyon gösterdi ve en ağır çocukluk başlangıçlı mutasyonlar neredeyse hiç asetilasyon geri getirmedi. Yakın zamanda çözülen SLC33A1’in üç boyutlu yapısından yararlanarak yazarlar bu mutasyonları proteine haritaladı ve büyük olasılıkla yapısını veya asetil‑CoA bağlama yeteneğini nasıl bozduklarını gösterdi. Bu durum, bozulmuş gangliozit asetilasyonunun hastalardaki nörolojik semptomlara katkıda bulunduğunu kuvvetle düşündürüyor.
CASD1’de gizli ikinci bir aktif bölge
Çalışma ayrıca beklenmedik bir kıvrımı ortaya koydu: CASD1’in kendisinin çift amaçlı bir enzim olduğu görünüyor. Golgi lümenindeki bilinen bölümü SLC33A1 tarafından sağlanan asetil‑CoA’yı kullanıyor. Ancak SLC33A1 yok edildiğinde, hücreler bazı koşullar altında belirli sialik asitlere tek bir asetil grubu yerleştirmeyi yine de başardı; buna karşın daha karmaşık desenler için gereken ikinci asetil grubunu ekleyemediler. İleri yapı tahmini ve moleküler simülasyonlar kullanarak yazarlar, CASD1’in membranı geçen bölümünün lizozomlardan bilinen bir transmembran asetiltransferaza yakından benzediğini gösterdiler. Bu bölgede sitozolik tarafta asetil‑CoA’yı bağlayan ve asetil grubunu doğrudan sialik aside membran boyunca ileten anahtar amino asitleri belirlediler. Bu kalıntılar değiştirildiğinde, CASD1 hem denen tüp deneylerinde hem de canlı hücrelerde bu ikinci aktivitesini kaybetti.
İki yol, tek ince ayarlı şeker kodu
Veriler bir “iki‑katalitik‑bölge” modelini destekliyor. Bir yol, SLC33A1’in asetil‑CoA’yı Golgi lümenine taşımasına dayanıyor; burada CASD1’in lümenal domaini sialik aside bir asetil grubu ekliyor ve hem basit hem çift asetillenen desenlere olanak sağlıyor. Diğer yol ise CASD1’in membranı geçen çekirdeğine gömülü; bu kısım sitozolik asetil‑CoA’ya doğrudan erişiyor ve SLC33A1 eksik olsa bile temel düzeyde asetilasyon yapabiliyor. Bir okuyucu için bunun anlamı şudur: tek bir enzim, iki farklı asetil kaynağıyla beslenerek hücre yüzeyi şekerlerine ince “noktalama işaretleri” yazıyor. Taşıyıcı veya enzimin herhangi bir kısmı bozuk olduğunda bu işaretler yanlış yere konuyor veya eksik kalıyor; bu durum bazı nörogelişimsel ve nörodejeneratif hastalıkları açıklamaya yardımcı olabilir ve hücrelerimizin dış kimliğini şekillendirmede yeni bir düzenleme katmanını vurgular.
Atıf: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Anahtar kelimeler: sialik asit, Golgi asetilasyonu, gangliozitler, SLC33A1, CASD1