Clear Sky Science · tr
Ubikuitin bağımsız substrat dönüşümü sırasında midnolin-proteazomun yapısal dinamikleri
Hücreler Çöpleri Hızla Nasıl Dışarı Atıyor
Her hücrenin içinde proteinler sürekli üretilir ve yıkılır. Birçoğu, hücrenin ana geri dönüşüm makinesi olan proteazoma beslenmeden önce ubikuitin adı verilen küçük moleküllerle işaretlenir. Ancak bazı nükleer proteinlerin o kadar çabuk uzaklaştırılması gerekir ki işaretlemeye zaman kalmaz. Bu çalışma, az bilinen bir yardımcı protein olan midnolinin, bu acil hedefleri temizlemek için proteazoma doğrudan nasıl bağlandığını ortaya koyuyor ve hücrelerin gen aktivitesini sıkı ve hızlı biçimde nasıl kontrol ettiğine dair ipuçları sunuyor.
Hücresel Öğütücüye Kısa Yol
26S proteazom, proteinleri küçük parçalara ayıran fıçı biçimli bir komplekstir. Geleneksel olarak hedefleri, üzerlerine bağlanmış ubikuitin zincirlerini okuyarak tanır. Son çalışmalar alternatif bir yolu ortaya çıkardı: midnolinin belirli nükleer proteinleri—özellikle genleri hızla açıp kapatan hemen erken gen ürünlerini—herhangi bir ubikuitin etiketi olmadan doğrudan proteazoma götürdüğü bir “kısa yol” mekanizması. Stres yanıtı ve inflamasyonda rol alan transkripsiyon faktörleri gibi bu proteinlerin ortaya çıkıp kaybolması dakika mertebesinde gerçekleşmelidir. Yeni makale, yüksek çözünürlüklü kriyo-elektron mikroskobu ile biyokimyasal deneyleri birleştirerek midnolinin proteazoma nasıl tutunduğunu ve yükünü yok edilmek üzere nasıl konumlandırdığını adım adım haritalıyor.
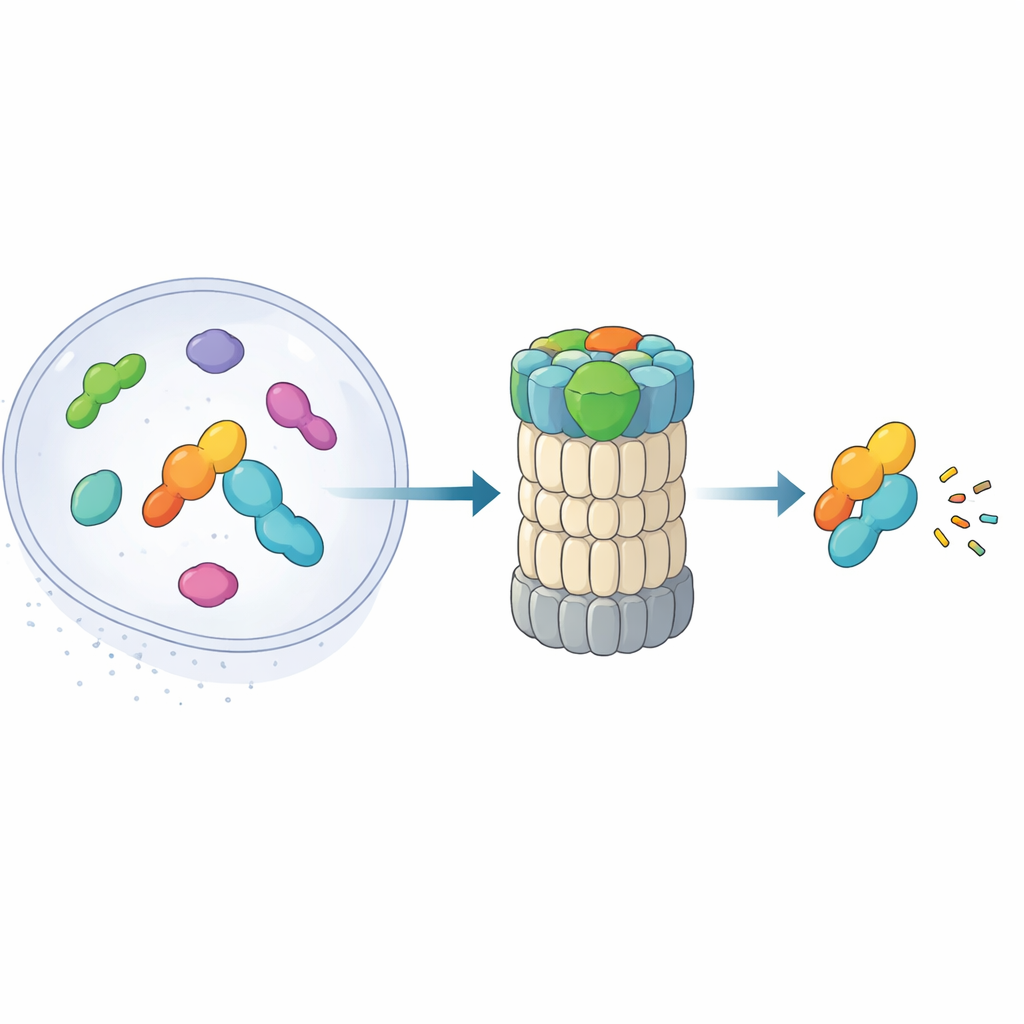
Hedefi Yakalayıp Hedefe Soran Üç Bölümlü Yardımcı
Midnolin üç ana modüle sahip çok amaçlı bir alet gibi çalışır. Bir uçtaki C-terminal heliks, proteazom bileşenlerinden biri olan RPN1 üzerindeki bir bağlantı noktasına girerek midnolini geri dönüşüm makinesine sabitler. Orta kısımdaki “Tut” bölgesi, hedef proteinlerdeki belirli ipliksi bir özelliği (degron) tanır ve kavrar. Karşı uçta ise ubikuitin-benzeri bir domain bulunur. Sürpriz şekilde bu domain, diğer taşıyıcı proteinlerde olduğu gibi esas olarak proteazoma bağlanmak için kullanılmaz. Yazarlar, bunun yerine RPN11 adlı, normalde substratlardan ubikuitini kesen bir enzimle karşı karşıya oturduğunu gösteriyor. Burada RPN11 daha çok bir iskele görevi görür: midnolinin ubikuitin-benzeri segmentini kavrayarak Tut bölgesini ve bağlı yükünü proteazomun dar giriş gözeneklerinin tam üzerinde tutmaya yardımcı olur.
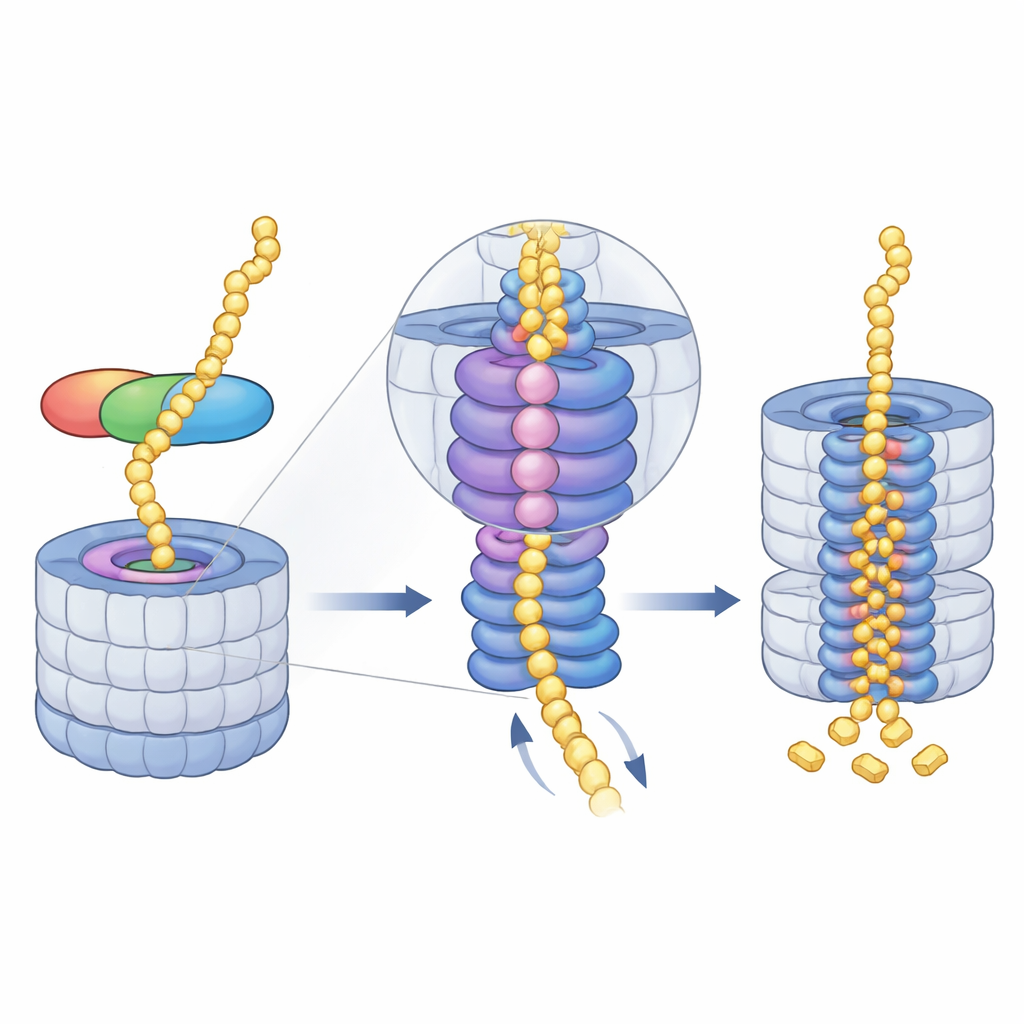
Proteini Öğütücü Çekirdeğe Yönlendirmek
Midnolin bağlandıktan sonra, proteazomun enerji harcayan motoru—bir AAA+ ATPaz halkası—devreye girer. Bu halka giriş gözenekinin hemen altında oturur ve açılmamış protein zincirlerini adım adım çekerek çekirdeğe doğru ilerletir. Kriyo-EM fotoğrafları, motorun altı alt biriminin substratı merkezi kanaldan kavrayıp el değiştirdikçe benimsediği bir dizi “spiral merdiven” konumunu gösteriyor. Yazarlar bu döngünün dört ardışık aşamasını yakaladı; hepsinde midnolin bağlı malzeme gözenekten geçirilmiş haldeydi ve hatta bir alt birimdeki magnezyum iyonunun serbest bırakılmasının tüm halkanın aşağı doğru kaymasıyla eş zamanlı olduğunu gördüler. Bu, koordine ATP kullanımı ve magnezyum salınımının proteini kesim bölgelerinin bulunduğu odaya daha derin bir şekilde ilerletmeye yardımcı olduğunu düşündürüyor.
Neden Konumlandırma ve Eşzamanlı Üretim Önemli
Takım, her midnolin modülünün verimliliğe nasıl katkıda bulunduğunu test etti. Sadece ankraj heliksi RPN1’e bağlanabilir ama proteazom aktivitesini anlamlı şekilde artırmaz. Tut domaininin çıkarılması, midnolin hâlâ tutunabilse bile birçok proteazomun uyarılmamış, substratsız bir durumda takılı kalmasına yol açar; Tut’un yerine kalıcı olarak füze edilmiş bir substrat konması da tam aktiviteyi geri getirmez. Bu bulgular Tut’un sadece hedefi yakalamakla kalmayıp aynı zamanda proteazom girişinde proteini hassas biçimde yönlendirmesi gerektiğini gösterir. Biyokimyasal ve tümör transkriptom veri setleri ayrıca midnolin ile hedef proteinlerin birlikte üretilme eğiliminde olduğunu gösterir. Eşzamanlı ifade edildiğinde midnolin daha iyi katlanır ve stabil kompleksler oluşturur; böylece hücrenin gen ekspresyonunu sıfırlaması gerektiğinde hızlıca proteazoma teslim edilebilecek hazır bir “beni parçala” paketi oluşur.
Öz Temizlik ve Gelecekteki Tıbbi Olanaklar
Hedef protein çekilip parçalandıktan sonra midnolinin kendisi de bağışlanmaz. Kendi düzensiz bölgeleri motor tarafından geçirilip aynı yok etme odasına beslenebilir, böylece yardımcının gereksiz birikimi engellenir. Bu ubikuitinsiz proteazom yolunu aydınlatarak çalışma, hücrelerin protein ömürlerini çok sıkı zaman çizelgelerinde nasıl yönettiğine dair anlayışımızı genişletir. Ayrıca yeni terapötik stratejilere işaret eder: midnolin tabanlı moleküller tasarlanarak hastalığa yol açan nükleer proteinleri doğrudan proteazoma bağlamak mümkün olursa, belirli kanser tetikleyicileri dahil olmak üzere “ilaçlanamaz” hedefleri daha hızlı ve seçici biçimde yok etmek bir gün mümkün olabilir.
Atıf: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Anahtar kelimeler: proteazom, midnolin, protein yıkımı, ubikuitin-bağımsız yol, hemen erken genler