Clear Sky Science · tr
MDSC’lerin ANXA1-FPRs sinyaliyle aracılık ettiği mekânsal heterojenite OSCC ilerlemesinde bağışıklık baskılanmasını tetikliyor
Vücudun Savunmasının Bazı Ağız Kanserleriyle Neden Mücadele Ettiği
Oral skuamöz hücreli karsinom, ağız kanserlerinin yaygın bir türü, sıklıkla vücudun kendi savunmasını serbest bırakan ve günümüzün en umut verici kanser tedavilerinden biri olan immünoterapilere direnç gösterir. Bu çalışma temel ama kritik bir soruyu soruyor: kanseri tanıyıp yok etmesi beklenen güçlü bağışıklık hücreleri bu tümörlerde neden sık sık başarısız oluyor? Araştırmacılar, farklı hücrelerin tümör içinde nerede yer aldığını ve nasıl iletişim kurduklarını haritalayarak, kanser hücreleri, bağışıklık baskılayıcı hücreler ve öldürücü T hücreleri arasında tedavi başarısızlığını açıklamaya yardımcı olan değişken bir “kedi‑fare” oyunu açığa çıkardılar—ve bunu düzeltmenin bir yolunu öneriyorlar. 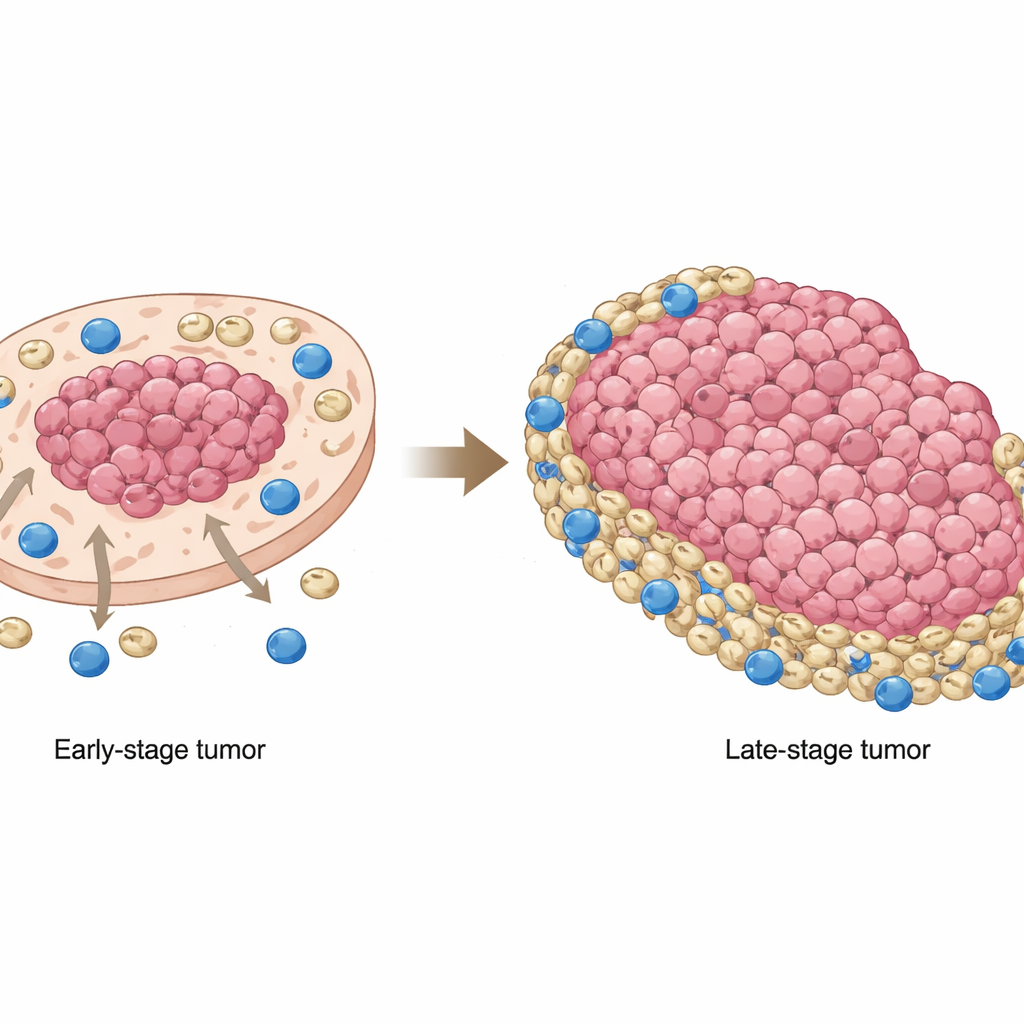
Tümörün İçindeki Gizli Peyzaj
Yazarlar iki ileri teknoloji yaklaşımını birleştirdiler: bireysel hücrelerin etkinliğini okuyan tek hücre RNA dizilemesi ve bu hücrelerin gerçek tümör doku kesitleri içinde nerede bulunduğunu gösteren mekânsal transkriptomik. Erken ve geç evre ağız kanseri olan hastalardan alınan tümörleri analiz ederek başlıca hücre aktörlerini tanımladılar: kanseröz epitelyal hücreler, CD8 “öldürücü” T hücreleri, diğer T ve B hücreleri, yapısal destek sağlayan fibroblastlar ve myeloid kaynaklı baskılayıcı hücreler (MDSC) adı verilen uzmanlaşmış bağışıklık hücreleri. Erken tümörlerde daha aktif CD8 T hücreleri bulunurken, geç evre tümörler zayıf T hücre sinyallemesi ve myeloid hücrelerden güçlü bağışıklık‑söndürücü sinyaller gösteriyordu; bu da anti‑kanser bağışıklık için giderek daha elverişsiz bir ortamı işaret ediyordu.
Hareket Halindeki Baskılayıcı Hücreler
En çarpıcı bulgulardan biri, MDSC’lerin konumunun tümör ilerledikçe nasıl değiştiğiydi. Erken evre kanserlerde bu baskılayıcı hücreler tümör hücresi bakımından zengin bölgelerde, kanser çekirdeğine yakın kümelenme eğilimindeydi. İleri evrelerde ise dışa kaydılar, tümörün fakir olduğu alanlarda ve kenarlarda biriktiler; bu bölgelerde CD8 T hücreleri daha yaygındı. Bu, ileri tümörlerde öldürücü T hücrelerin büyük ölçüde kenarlara itildiği ve orada MDSC’lerin bir kuşak gibi karşılarına çıkıp kanser hücrelerine saldırma yeteneklerini zayıflattığı anlamına geliyordu. Hasta örnekleri ve fare modelleri, bu yeniden dağılımın yalnızca bir merak olmadığını doğruladı: MDSC’lerin kanser hücreleriyle daha az örtüştüğü ve bunun yerine tümör dışı bölgelerde toplandığı durumlarda hastaların genel sağkalımı daha kötüydü. 
Kanser ve Baskılayıcı Hücreler Arasında Bir Sinyalleşme Anahtarı
Çalışma, tümör hücrelerindeki annexin A1 (ANXA1) proteinini ve myeloid hücrelerdeki FPR ailesi reseptörlerini içeren kanser hücreleri ile MDSC’ler arasındaki moleküler “konuşmaya” yakından baktı. Erken hastalıkta, kanser hücrelerindeki ANXA1 özellikle MDSC’ler ve tümör ilişkili makrofajlarda FPR1 ve FPR3 ile güçlü etkileşim kurarak bu baskılayıcı hücreleri tümör çekirdeğine çekmeye ve orada tutmaya yardımcı oluyordu. Kanser ilerledikçe tümör hücrelerindeki ANXA1 seviyeleri düştü ve bu özgün bağlantılar zayıfladı. Aynı zamanda daha fazla MDSC başka bir reseptör olan FPR2’yi ifade etmeye başladı ve ANXA1–FPR2 sinyalleşmesi MDSC’leri bağlı tutmak için telafi edici bir yol olarak ortaya çıktı. Yüksek ANXA1 gösteren ve kök‑benzeri özellikler sergileyen belirli bir tümör hücresi alt kümesi erken dönemde adeta “yem” işlevi görerek MDSC’leri çekiyor görünüyordu; ANXA1 düştüğünde MDSC’ler çekirdekte sabit kalmıyor ve bunun yerine CD8 T hücreleriyle zengin bölgelere doğru kayıyordu.
Kalkanı Kapatıp İmmünoterapinin İşlemesine Yardım Etmek
Bu iletişimi bozmanın tedaviyi iyileştirip iyileştirmeyeceğini test etmek için araştırmacılar, oral kanser fare modelinde FPR2’yi WRW4 adlı küçük moleküllü bir inhibitörle bloke ettiler. Tek başına FPR2 inhibisyonu MDSC varlığını azalttı ve tümör ortamında CD8 T hücrelerini artırdı fakat tümör büyümesini yeterince yavaşlatmadı. Benzer şekilde, tek başına anti–PD‑1 immün kontrol antikoru ile tedavi sınırlı fayda sağladı; çünkü MDSC’ler hâlâ baskılayıcı bir bariyer oluşturuyordu. Ancak her iki ilaç birleştirildiğinde tümör büyümesi güçlü şekilde durduruldu ve farelerin yaşam süresi uzadı. Bu hayvanlarda MDSC infiltrasyonu keskin şekilde azaldı ve CD8 T hücreleri tümör hücresi bakımından zengin bölgelere daha derin nüfuz etti; bu da FPR2’yi bloke etmenin normalde kanser hücrelerini bağışıklık saldırısından koruyan kilit bir kalkanı kaldırdığını gösteriyor.
Geleceğin Kanser Bakımı İçin Ne Anlama Geliyor
Bir araya getirildiğinde, bu çalışma sadece hücre tiplerinin değil aynı zamanda bunların mekânsal düzeninin ve sinyalleşme ortaklarının da oral kanserde immünoterapinin başarı şansını belirlediğini gösteriyor. Tümörler ilerledikçe MDSC’ler merkezden kenarlara göç ediyor, burada öldürücü T hücreleriyle karşılaşıp onları yakalıyor ve ANXA1–FPR2 sinyalleşmesi bu baskılayıcı düzeni sürdürmeye yardımcı oluyor. Bu yolak bozulduğunda—özellikle mevcut kontrol noktası ilaçlarıyla kombinasyon halinde—hekimler tümör ortamını yeniden yapılandırarak vücudun kendi bağışıklık hücrelerinin kanseri yeniden tanıyıp yok etmesini sağlayabilir. Bu, somut bir strateji öneriyor: FPR2 blokerlerini immünoterapi ile eşleştirmek, şu anda en iyi mevcut tedavilere dirençli olan hastaların ağız kanserlerinde sonuçları iyileştirebilir.
Atıf: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
Anahtar kelimeler: oral skuamöz hücreli karsinom, tümör mikroçevresi, myeloid kaynaklı baskılayıcı hücreler, mekânsal transkriptomik, kanser immünoterapisi