Clear Sky Science · tr
Sentez aptamer mekanoreseptörleri, DNA devreleri aracılığıyla hücreye özgü kuvvet algılama ve zamansal kontrol sağlar
Hafif Çekişlerle Hücreleri Dinlemek
Vücudumuz, çevresiyle sürekli itişip çeken hücrelerle doludur; bu küçük kuvvetleri büyüme, hareket veya değişim zamanını belirlemek için kullanırlar. Bu çalışma, belirli hücre tiplerine göre ayarlanabilen ve zaman içinde açılıp kapatılabilen DNA tabanlı aygıtlarla bu kuvvetleri dinlemenin yeni bir yolunu tanımlıyor. Bu teknoloji bir gün mühendislerin doku büyümesini yönlendirmesine, tümörlerin davranışını anlamasına veya canlı hücrelere gerçek zamanlı yanıt veren akıllı malzemeler tasarlamasına yardımcı olabilir.
DNA’yı Minik Bir Mekanik Anahtar Olarak Kullanmak
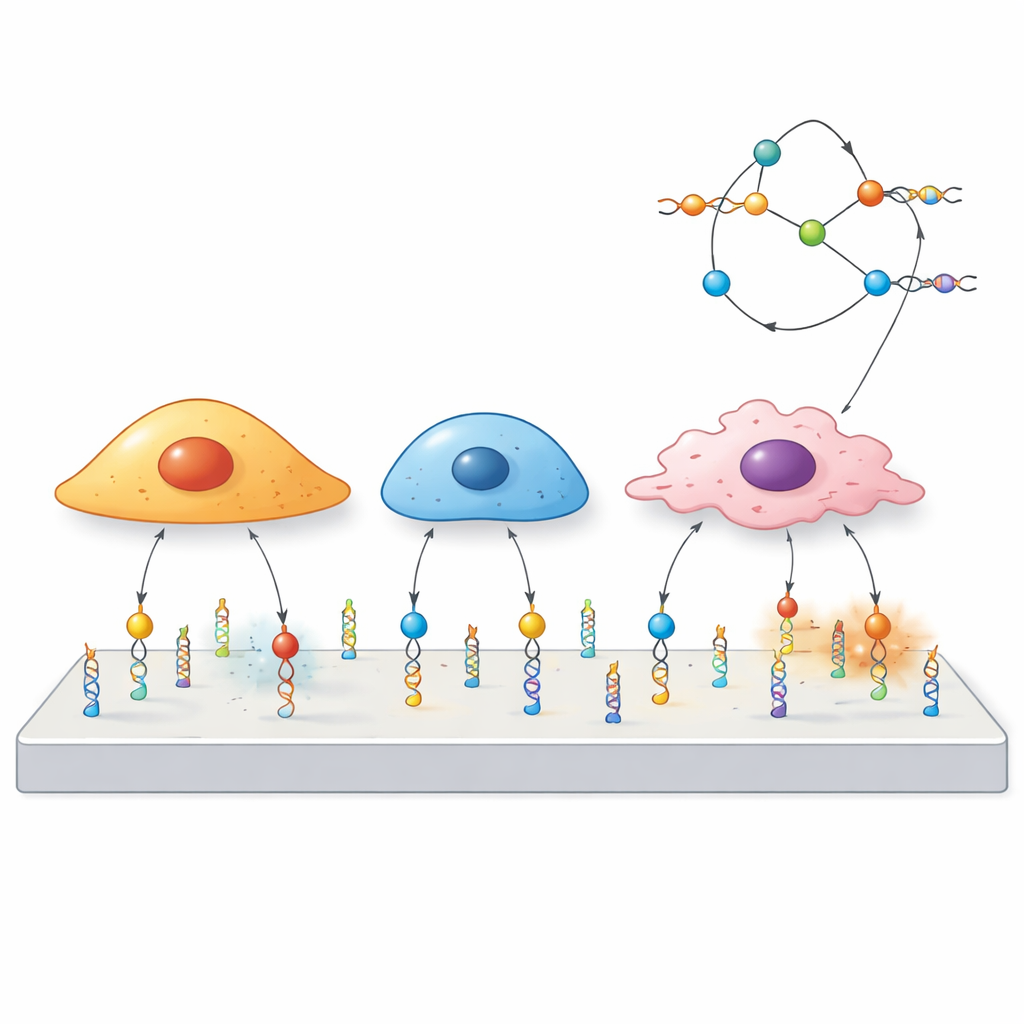
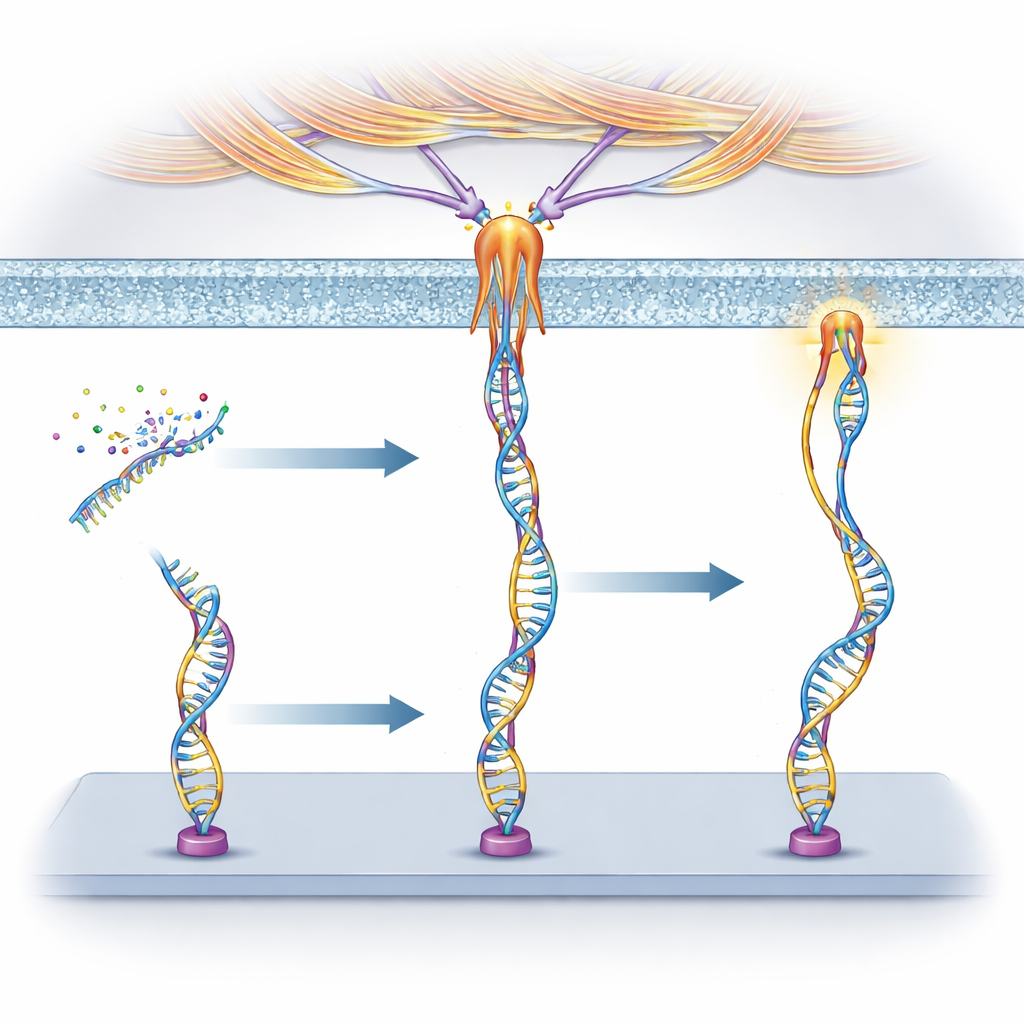
Araştırmacılar, genetik bilgiyi taşıyan aynı molekül olan DNA’dan “mekanoproblar” inşa ettiler. Her prob üç bölümden oluşur: hücre yüzeyindeki seçilmiş bir proteine yapışan aptamer adı verilen kısa bir DNA dizisi, belirli bir kuvvette kopacak şekilde ayarlanmış yay gibi davranan eşleşmiş bir DNA segmenti ve o yay kırıldığında ışık veren bir floresan boya. Bir hücre aptamerle bağlanmış reseptöre yeterince güçlü bir çekiş uyguladığında DNA dubliks açılır ve sinyal aktifleşir. Farklı aptamerler farklı reseptörlere tutunduğundan, ekip hangi hücrelerin veya proteinlerin probu tetikleyebileceğini önceden belirleyebilir.
Hücre Yüzeyinde Gizli Kuvvet Yollarını Bulmak
Mevcut kuvvet sensörlerinin çoğu, hücrelerin çevrelerine tutunmasına yardımcı olan ve birçok hücre tipinde bulunan integrinlere odaklanır; bu da seçiciliği sınırlar. Burada ekip, genellikle mekanik olarak düşünülmeyen “kanonik olmayan” reseptörleri hedef aldı. Kanser hücrelerinde yaygın olan nükleoline bağlanan AS1411 adlı bir aptamerin, hedefini özgün şekilde tanıyabildiğinde sinyal ürettiğini gösterdiler. Açılması için ya daha zayıf ya da daha güçlü kuvvetler gerektiren problar tasarlayarak nükleolinin integrinlere kıyasla ılımlı kuvvetler ilettiğini ve tek başına hücrelerin yüzeyde yayılmasına yardım etmediğini keşfettiler. Buna karşılık, reseptör PTK7’yi tanıyan Sgc8 adlı başka bir aptamer, hücreler zar zor yapışmış olsa bile kuvvetleri rapor edebildi; halka benzeri desenler oluştu ve bu farklı bir hareket kaynağına işaret etti.
Kuvvetlerin Nereden Geldiğini İzlemek
Bu DNA aygıtlarına neyin çekiş uyguladığını anlamak için araştırmacılar farklı hücresel süreçleri seçici olarak engelleyen ilaçlar kullandılar. Nükleolin için kuvvetlerin güçlü bir şekilde miyozine bağımlı olduğunu buldular; miyozin, kasların kasılmasına yardımcı olan motor proteindir ve sinyaller hücrenin odak yapışma–sertlik algılama için kullandığı özel temas noktalarında ortaya çıktı. Bu, nükleolinin hücrenin iç aktin–miyozin makinelemesine dolaylı olarak bağlı olduğunu ve kasılma kuvvetlerini paylaşabileceğini öne sürer. Öte yandan PTK7 için, hücrelerin zarlarını dalgalandırıp sıvı yuvarladığı makropinositoz adı verilen sürecin bloke edilmesi sinyalleri büyük ölçüde azalttı. Kuvvetler esas olarak vezikül kapatmanın sonraki aşamalarından ziyade aktin büyümesiyle yönlendirilen erken zar dalgalanmalarından kaynaklandı ve bu da ayrı bir mekanik yol ortaya koydu.
Moleküler Hassasiyetle Hücre Seçiciliğini Ayarlamak
Her aptamer belirli bir yüzey reseptörünü tanıdığından aynı DNA iskeleti sadece bir aptameri başka bir aptamerle değiştirerek yeniden programlanabilir. Ekip bunu PTK7, mucin-1 ve EpCAM için problarla ve her proteinin yüksek veya düşük düzeyde olduğu bir panel kanser hücre hattında gösterdi. Belirli bir reseptörde zengin olan hücreler güçlü sinyaller üretirken, az reseptör içerenler aynı kap içinde birlikte olduklarında bile neredeyse yanıt vermedi. Çarpıcı şekilde, aynı reseptörü paylaşan hücreler hâlâ farklı mekansal kuvvet desenleri gösterebildi; bu da bir reseptör üzerinden akan kuvvetin yalnızca varlığına değil, her hücre tipinin içsel bağlantılarına da bağlı olduğunu vurguluyor.
Hücrelerin Ne Zaman Çekmesine İzin Verileceğini Programlamak
Aptamerlerin DNA’dan yapılmış olmasının avantajından yararlanarak araştırmacılar problarını aptamerin bağlanıp bağlanamayacağını kontrol eden DNA reaksiyon ağlarına bağladılar. Tamamlayıcı “engelleyici” diziler aptameri geçici olarak gizleyebilir ve daha sonra “aktive edici” diziler şerit değişimi reaksiyonu yoluyla engelleyicileri çıkararak kuvvet duyarlılığını geri getirebilir. Ayrıca RNase H adlı bir enzim tarafından kesilebilen RNA tabanlı bir engelleyici tasarladılar ve bu kesimi enzime rakip olan yanıltıcı moleküllerle yavaşlattılar. Bu yolla mekanosensörü zamanlı bir programa dönüştürdüler: hücreler yerleşik bir gecikmeden sonra veya seçilen zaman pencereleri içinde yalnızca o zamanlarda sinyal üretebiliyordu.
Geleceğin Yaşayan Malzemeleri İçin Neden Önemli
Günlük terimlerle, bu çalışma DNA’yı yalnızca belirli hücreler, yalnızca belirli kuvvetler ve yalnızca seçilmiş zamanlarda açılan akıllı bir mekanik kilide dönüştürüyor. Nükleolin ve PTK7 gibi daha az belirgin reseptörlerin hücre içinde çok farklı yollarla mekanik bilgi taşıyabileceğini ortaya koyarak hücrelerin çevrelerini “nasıl hissettiklerine” dair resmimizi genişletiyor. Tüm sistem nükleik asitlerden inşa edildiği için DNA devreleri ve nanoyapıların hızla büyüyen araç kutusuna doğrudan bağlanabiliyor. Bu, hücrelerin ne zaman itip çektiğini algılamakla kalmayıp, dikkatle zamanlanmış biyokimyasal eylemlerle yanıt veren malzemeler ve mühendislikleştirilmiş dokular için bir temel oluşturuyor; bu da iyileşmeyi, büyümeyi veya kanser tedavisini yüksek düzeyde programlanabilir şekilde yönlendirme potansiyeli taşıyor.
Atıf: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Anahtar kelimeler: mekanotransdüksiyon, DNA aptamerleri, hücre mekaniği, sentetik biyoloji, DNA reaksiyon ağları