Clear Sky Science · tr
Patojenik bir Tau mutasyonu, frontotemporal demans modelinde Tau yıkımını sınırlayan otofaji-lizozom işlev bozukluğunu tetikliyor
Beynin Temizlik Ekipleri Geri Kaldığında
Bazı kişiler yaşlılıktan çok önce neden yıkıcı hafıza ve davranış sorunları geliştirir? Bu çalışma, tek bir beyin proteini olan Tau ve normalde onu kontrol altında tutan küçük hücresel “geri dönüşüm merkezleri” üzerine odaklanarak bu soruyu ele alıyor. Canlı insan nöronlarını son derece net mikroskoplarla izleyerek, araştırmacılar hastalık yapıcı bir Tau mutasyonunun hücrenin atık imha sistemini nasıl tıkadığını ve bu sistemi küçük bir molekülle hızlandırmanın dağınıklığı nasıl temizleyebileceğini gösteriyor. Bulguları, bazı demans türleri için yeni tedavi stratejilerine işaret edebilir.
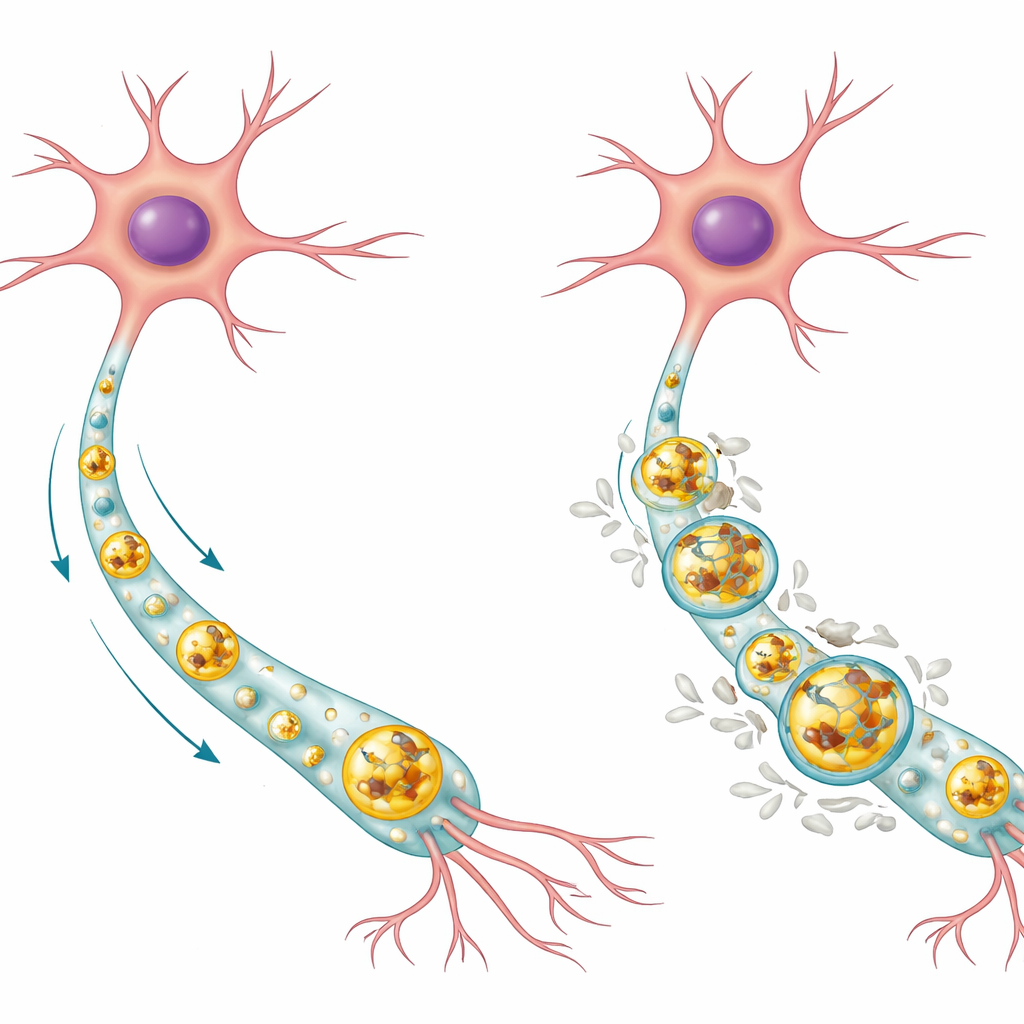
Beyin Hücreleri Genellikle Çöpü Nasıl Dışarı Atar
Nöronlar uzun ömürlü hücrelerdir ve hasarlı maddeleri seyreltemek için bölünemezler, bu yüzden içsel temizlik sistemlerine büyük ölçüde güvenirler. Ana yollardan biri otofaji-lizozom yoludur. Bu süreçte istenmeyen proteinler ve eskimiş parçalar, otofagosom adı verilen zar keseciklerine sarılır; sonra bu kesecikler enzim dolu lizozomlarla kaynaşır ve içlerindeki yük parçalanıp geri dönüştürülür. Sağlıklı insan nöronlarında, yazarlar normal Tau proteininin lizozomların asidik merkezinde birikme eğiliminde olduğunu buldular; burada Tau parçalanabilirken, hastalıkla ilişkili kimyasal bir değişiklik olan fosforile Tau ise daha çok lizozomun dış zarında yer alıyordu. Sağlıklı hücrelerdeki çoğu lizozomun tamamen Tau’dan arınmış olması, bu sistemin genellikle Tau düzeylerini düşük ve iyi kontrol altında tuttuğunu düşündürüyor.
Genetik Bir Demansta Neler Yanlış Gidiyor
Takım, kalıtsal bir frontotemporal demansa yol açan ve Alzheimer benzeri hafıza kaybını taklit edebilen MAPT genindeki p.R406W adlı mutasyona odaklandı. Kök hücre teknolojisi kullanarak hasta deri hücrelerini indüklenmiş pluripotent kök hücrelere ve ardından ya mutasyonu taşıyan ya da gen düzenlemesiyle normale çevrilmiş geniş sayıda insan nöronuna dönüştürdüler. Mutant nöronlarda toplam Tau ve fosforile Tau belirgin şekilde daha yüksekti; bunun nedeni hücrelerin daha fazla Tau üretmesi değil, onu daha az verimli temizlemesiydi. Süper-çözünürlüklü görüntüleme, mutant hücrelerdeki neredeyse tüm lizozomların Tau ile dolu olduğunu ve özellikle fosforile Tau’nun lizozom zarını kapladığını ortaya koydu. Bu birikim, hücrenin ana protein imha yolunun tıkandığını işaret ediyordu.
Tıkanmış Geri Dönüşüm Merkezleri ve Yavaşlayan Trafik
Geri dönüşüm mekanizmasını daha yakından incelediklerinde, araştırmacılar mutant nöronlardaki lizozomların daha fazla sayıda, daha büyük ve hücre gövdesinden daha uzakta yer alma eğiliminde olduğunu gördü. Floresan boyalarla canlı görüntüleme, bu lizozomların daha yavaş hareket ettiğini ve sinir lifleri boyunca daha kısa mesafeler kat ettiğini gösterdi; oysa altta yatan mikrotübül yollar normal görünüyordu. Mutant nöronlar ayrıca daha fazla otofagosom, daha fazla yük-adaptör proteini p62 ve ekstra lipid damlacıkları içeriyordu—bu, materyalin imha için etiketlendiğini ama tam olarak parçalanmadığını gösteren işaretlerdi. pH duyarlı bir raporlayıcı kullanıldığında, mutant hücrelerdeki otofagosomların sıklıkla lizozomlarla düzgün şekilde kaynaşamadığı bulundu; bu da yarım kalmış geri dönüşüm veziküllerinin yığılmasına ve yalnızca Tau için değil, diğer yükler için de geniş çaplı hücresel temizlik kusurlarına yol açıyordu.
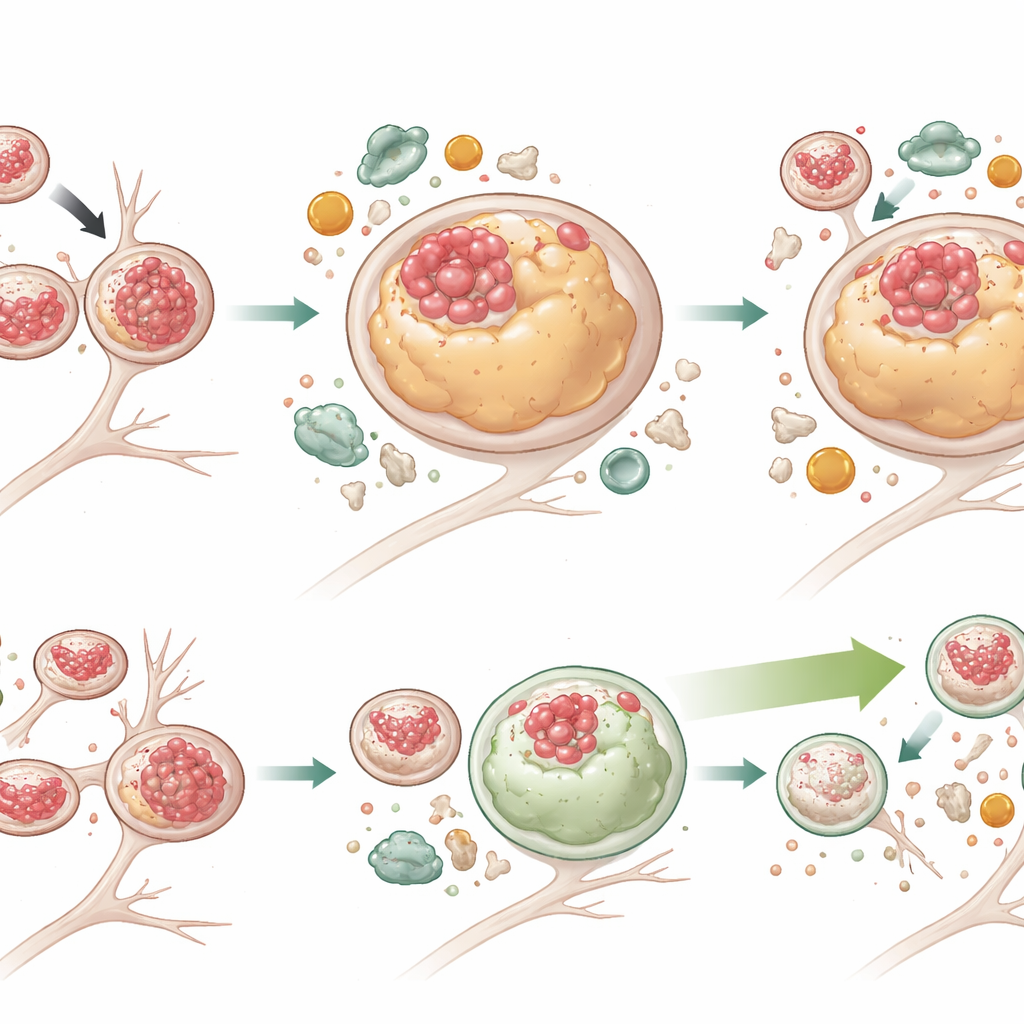
Trafik Sıkışmasını Düzeltmeden Hücresel Temizliği Güçlendirmek
Otofajiyi güçlendirmenin bu sorunları aşmaya yetip yetmeyeceğini test etmek için ekip, otofaji-lizozom sistemini uyarması daha önce gösterilmiş küçük bir molekül olan G2-567 ile nöronları tedavi etti. İki haftalık tedaviden sonra, mutant nöronlarda hem toplam Tau hem de fosforile Tau seviyeleri önemli ölçüde düştü ve birçok lizozom yeniden Tau’dan arınmış hâle geldi. Lizozomlar ayrıca normale daha yakın bir boyuta küçüldü. Aktif otofajinin belirteçleri artarken, bozuk yıkımı gösteren p62 mutant hücrelerde azaldı; bu, yükün daha etkili parçalanmasını gösteriyordu. İlginç şekilde, G2-567 tüm kusurları düzeltmedi: mutant nöronlardaki lizozomlar hâlâ hücre gövdesinden daha uzakta olma ve yavaş hareket etme eğilimindeydi ve lizozom taşınmasıyla ilişkili bir adaptör protein (JIP3) yüksek kaldı. Bu, lizozomların hareket ve yıkım işlevlerinin kısmen ayrıştırılabileceğini ve yalnızca parçalanmanın iyileştirilmesinin bile toksik Tau birikimini azaltmak için yeterli olabileceğini düşündürüyor.
Gelecekteki Demans Tedavileri İçin Bunun Anlamı
Uzman olmayan bir kişi için ana çıkarım şu: bu genetik frontotemporal demans modelinde sorun yalnızca Tau’nun anormal hâle gelmesi değil; asıl sorun nöronun geri dönüşüm sisteminin yetişememesi. p.R406W Tau mutasyonu otofaji-lizozom yolunun birkaç adımını doğrudan bozuyor ve Tau—özellikle fosforile formu—başka parçalanmamış materyallerle birlikte lizozomların üzerinde ve içinde birikiyor. Hücrenin temizlik mekanizmasını farmakolojik olarak biraz daha çalıştırarak araştırmacılar Tau düzeylerini düşürebilmiş ve lizozom boyutunu normalleştirebilmişler; taşınma kusurları devam etse bile. Bu bulgular, otofaji ve lizozomal fonksiyonu güvenli biçimde artırmayı hedefleyen ilaçların, tau ile ilişkili demanslarda ve belki Alzheimer gibi daha yaygın durumlarda protein dengesini yeniden sağlamakta yardımcı olabileceği fikrini güçlendiriyor.
Atıf: Mirfakhar, F.S., Marsh, J.A., Sato, C. et al. A pathogenic Tau mutation drives autophagy-lysosome dysfunction that limits Tau degradation in a model of frontotemporal dementia. Nat Commun 17, 2699 (2026). https://doi.org/10.1038/s41467-026-70473-5
Anahtar kelimeler: tau proteini, otofaji, lizozom işlev bozukluğu, frontotemporal demans, nörodejenerasyon