Clear Sky Science · tr
Yüzey hidrofobikliği ve sertliği, kolit tedavisi için ağız yoluyla verilen nanoparçacıklarda protein koronası belirler
Hapları Daha Akıllı Tedavilere Dönüştürmek
Kolit gibi inflamatuvar bağırsak hastalıklarıyla yaşayan kişiler genellikle güçlü anti-inflamatuar ilaçlar alır; ancak her dozun büyük kısmı boşa gider veya vücudun başka yerlerinde yan etkilere yol açar. Bu çalışma, ağız yoluyla verilen ilaçları daha çok hedefe yönelik füze gibi davranmaya yaklaştırmanın yeni bir yolunu araştırıyor: vücudun kendi bağırsak proteinlerini doğal bir hedefleme sistemi olarak kullanacak şekilde tasarlanmış küçük ilaç taşıyıcı partiküller oluşturmak; böylece ilaçların bağırsak iltihabını yönlendiren bağışıklık hücrelerine odaklanması sağlanıyor.
Bağırsak Nanoparçacıkları Nasıl Giydirir
Herhangi bir nanoparçacık vücuda girdiğinde, hızla ince bir protein tabakasıyla kaplanır; bilim insanlarının “protein koronası” dediği şey budur. Hastalıklı bağırsakta bu korona, yerel protein karışımı değiştiği için sağlıklı dokudakinden çok farklı görünür. Yazarlar daha önce kolitin, parçacıkları hem iltihabı körükleyen hem de çözümleyen makrofaj adı verilen bağışıklık hücrelerine kısmen yönlendiren özel bir bağırsak koronası oluşturduğunu bulmuştu. Burada amaç, ilaç taşıyıcı parçacıkların iki temel özelliğini—su iticilikleri (hidrofobiklik) ve sertlikleri (rijidite)—ayarlayarak bu koronayı kasıtlı şekilde şekillendirmek ve hastalık kaynaklı mütevazı bir etkiyi güçlü bir hedefleme stratejisine dönüştürmektir.
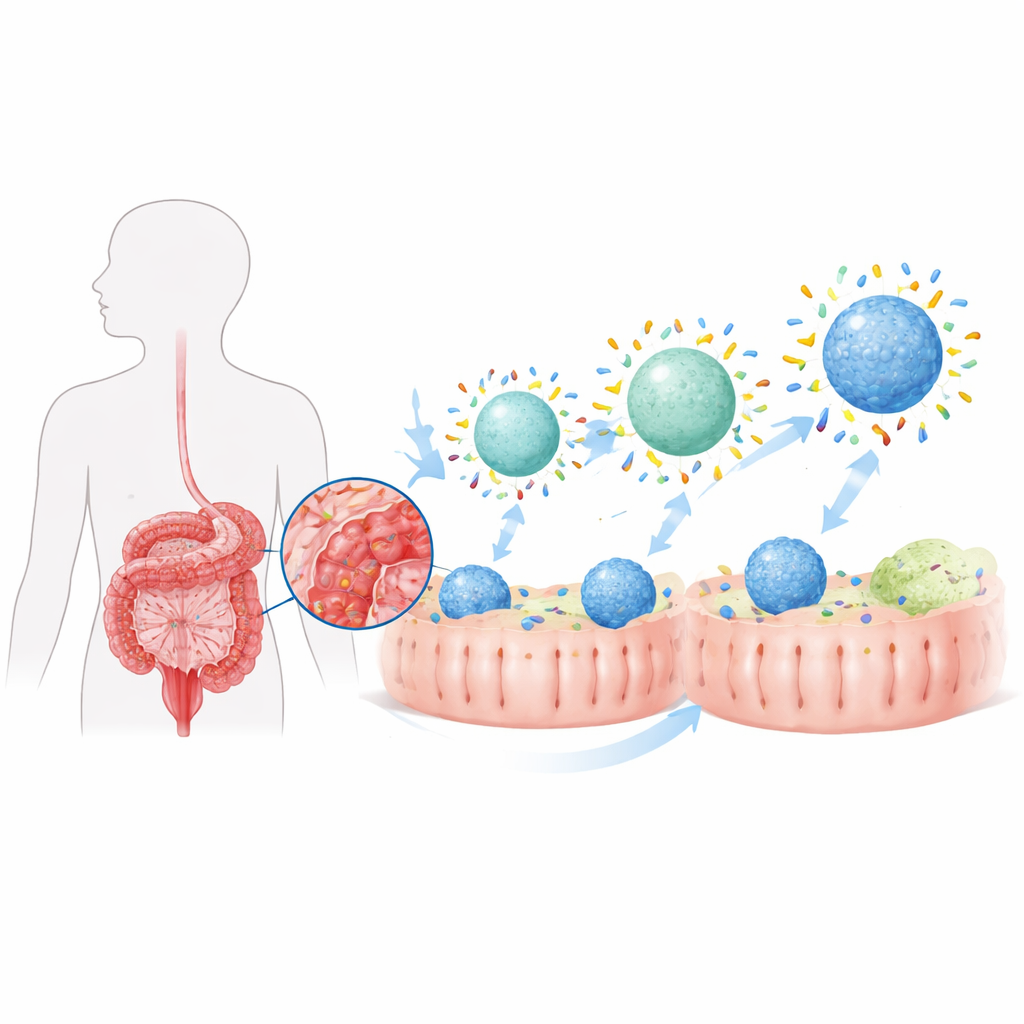
Parçacıkları Proteinlere Daha Cazip Kılmak
Araştırma ekibi, küçük yağ kabarcıklarına benzeyen lipit bazlı nanoparçacıklar inşa etti ve yüzeylerinin suyu seven veya sudan kaçan doğasını ortak bir polimer kaplama miktarını değiştirerek ayarladı. Daha hydrofobik yüzeylere sahip parçacıklar, kolit sıvılarına maruz kaldıklarında hem hayvanlarda hem de tüp testlerinde çok daha fazla bağırsak proteini bağladı. Bu “fobik” parçacıklar steroid budesonid ile yüklendiğinde ve kolitli sıçanlara ağızdan verildiğinde, kolon makrofajlarına daha su-sevici versiyonlara göre çok daha fazla ilaç ulaştırdılar. Sonuç olarak tedavi edilen hayvanlar daha fazla vücut ağırlığı geri kazandı, kolon kısalması ve doku hasarı azaldı ve bağırsaktaki inflamatuvar molekül düzeyleri düştü. Ancak iltihap iyileşse de tamamen sağlıklı duruma dönmedi; bu da yalnızca korona proteinlerinin toplam miktarını artırmanın yeterli olmadığını gösteriyor.
Daha İyi Ortaklar Seçmek İçin Parçacıkları Sertleştirmek
Konsepti daha ileri taşımak için araştırmacılar yüzeyleri hidrofobik tutarken iç yapıyı farklı boyutlardaki plastik kürelerle doldurarak parçacıkları yumuşak, orta veya sert hale getirdiler. Üçü de benzer toplam bağırsak proteini miktarını yakalasa da protein karışımı değişti. En sert parçacıklar özellikle makrofajlardaki reseptörlere tutunabilen veya bu hücrelerin aldıkları küçük besinleri taşıyabilen proteinler açısından zengin koronalar oluşturdu. Bu proteinlerden biri olan S100A8, iltihaplı bağırsaklarda bol bulunur ve belirli makrofaj reseptörleriyle etkileşime girebilir. Koronadaki S100A8 bloke edildiğinde sert parçacıkların makrofajlar tarafından alınması keskin biçimde azaldı; bu da parçacığın sertliği tarafından seçilen önemli bir hedefleme bileşeni olarak S100A8’i ortaya koyuyor.
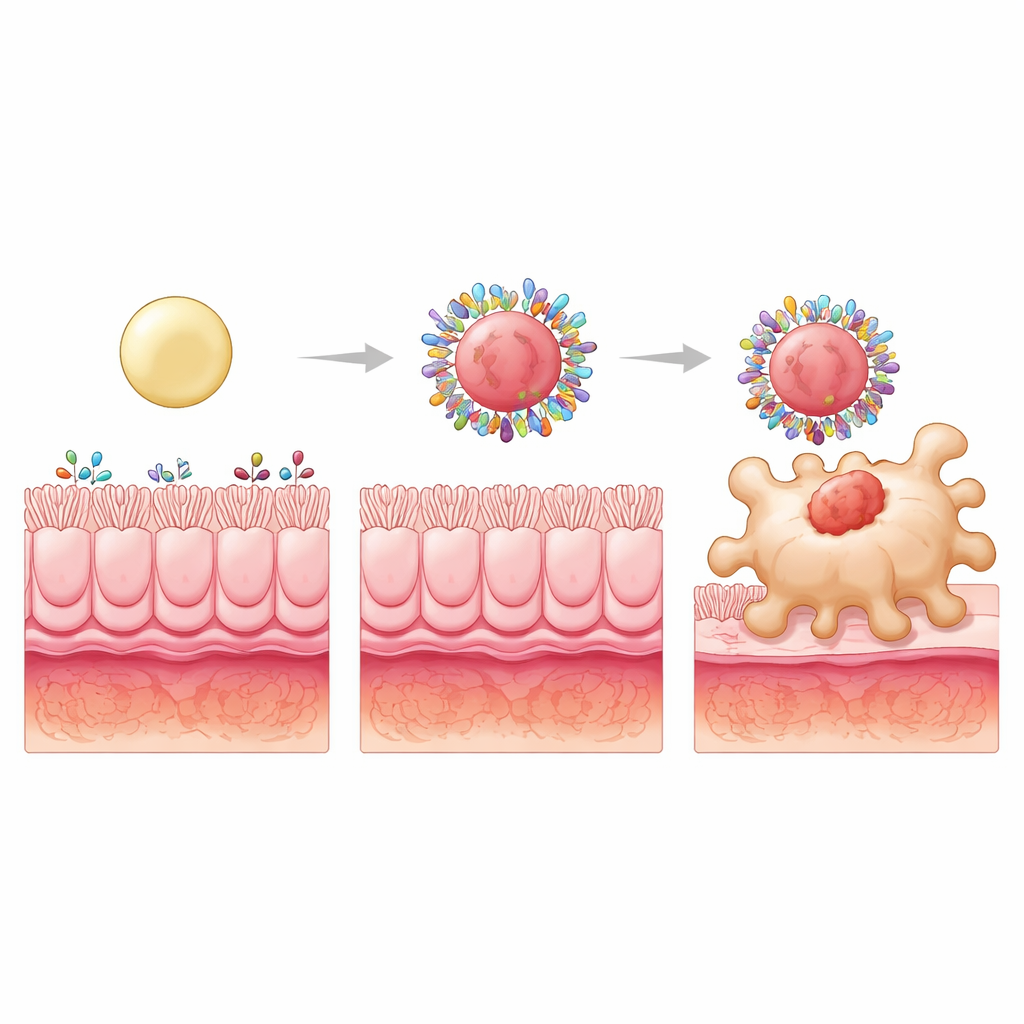
Daha İyi Hedeflemeden Daha İyi İyileşmeye
Budesonid bu yüksek hidrofobikliğe ve yüksek rijiditeye sahip parçacıklara paketlenip kolitli sıçanlara ağızdan verildiğinde yararlar çarpıcıydı. Sert formülasyon yalnızca bağırsak hasarını ve oksidatif stresi azaltmakla kalmadı, aynı zamanda bir dizi inflamatuvar sinyali sağlıklı hayvanlarda görülen seviyelere normalize etti. “Saldırgan” ve “sakin” makrofaj tipleri arasındaki daha sağlıklı dengeyi geri kazandırdı ve bağışıklık yanıtlarını kontrol altında tutmaya yardımcı olan düzenleyici T hücrelerini artırdı. Önemli olarak, bu kazanımlar kolitte hastalıkla değişmiş protein ortamına bağlıydı; aynı tasarım sağlıklı sıçanlarda özel bir hedefleme göstermedi ve bunun koronanının dinamik, hastalığa özgü bir müttefik olduğunu vurguladı.
Geleceğin İlaçları İçin Neden Önemli
Bu çalışma, taşıyıcıların yüzey ve mekanik özelliklerini ayarlayarak vücudun kendi proteinlerini ağızdan verilen ilaç taşıyıcıları üzerinde akıllı, kendini yenileyen “etiketler” gibi davranmaya yönlendirebileceğimizi gösteriyor. Önce hidrofobik yüzeyler aracılığıyla protein yakalamayı artırıp ardından rijiditeyi S100A8 gibi makrofaj yönelimli proteinleri destekleyecek şekilde kullanarak, araştırmacılar koliti yönlendiren bağışıklık hücrelerini doğal olarak arayan ve tedaviyi en çok ihtiyaç duyulan yere ulaştıran nanoparçacıklar yarattılar. Aynı tasarım mantığı—parçacıkların bağırsak yüzeyinde nasıl hissettikleri ve davrandıklarını manipüle etmek—birçok nanoterapi ve hastalığa uyarlanabilir; yapay hedefleme molekülleri eklemeden hedefe yönelik tedaviye daha ince bir yol sunar.
Atıf: Wu, J., Ni, M., Xing, L. et al. Surface hydrophobicity and rigidity determines protein corona on orally delivered nanoparticles treating colitis. Nat Commun 17, 2497 (2026). https://doi.org/10.1038/s41467-026-70453-9
Anahtar kelimeler: nanoparçacık ilaç taşıma, inflamatuvar bağırsak hastalığı, protein koronası, ağız yoluyla nanoterapi, makrofaj hedefleme