Clear Sky Science · tr
GTPaz aktive edici protein TBC1D9B ve bağlayıcı ortağı TMEM55B tarafından lizozom işlevinin kontrolü
Hücre Geri Dönüşüm Merkezleri Dengesi Nasıl Korur
Her hücremizin içinde geri dönüşüm merkezleri ve büyüme kontrol düğümcüleri gibi davranan lizozom adı verilen küçük kesecikler bulunur. İyi çalıştıklarında yıpranmış parçalar parçalanır ve bileşenleri yeniden kullanılır; başarısız olduklarında atıklar birikir ve nörodejenerasyon ile kanser de dahil hastalıklar ortaya çıkabilir. Bu çalışma, iki az bilinen proteinin lizozomları dolaşan, büyümeyi destekleyen bir durumla kümelenmiş, atıkları temizleyen bir mod arasında nasıl anahtar gibi geçiş yaptırdığını ortaya koyuyor ve hücrelerin bolluk ve kıtlık koşullarına nasıl uyum sağladığını aydınlatıyor.
Geri Dönüşüm Merkezlerini Hücre İçinde Hareket Ettirmek
Lizozomlar sabit değildir. İç hatlar boyunca hareket ederler; bir grup moleküler motor onları dışa doğru çekerken başka bir grup içe doğru çeker. Hücre içindeki konumları önemlidir: besinler bol olduğunda lizozomlar hücrenin dış bölgelerine yayılır ve büyüme sinyallerini destekler; yiyecek kıt olduğunda merkeze çekilir, daha asidik hale gelir ve hücresel materyalin parçalanmasını artırırlar. ARL8 adındaki küçük anahtar‑gibi bir protein lizozomları dışa itmesiyle biliniyor, ancak şimdiye dek bunu frenleyecek özel bir sistem tanımlanmamıştı. Yazarlar, böyle bir frenin açlık sırasında hücrelerin hızla tasarruf moduna geçmesine izin vermede kritik olacağını düşündüler.
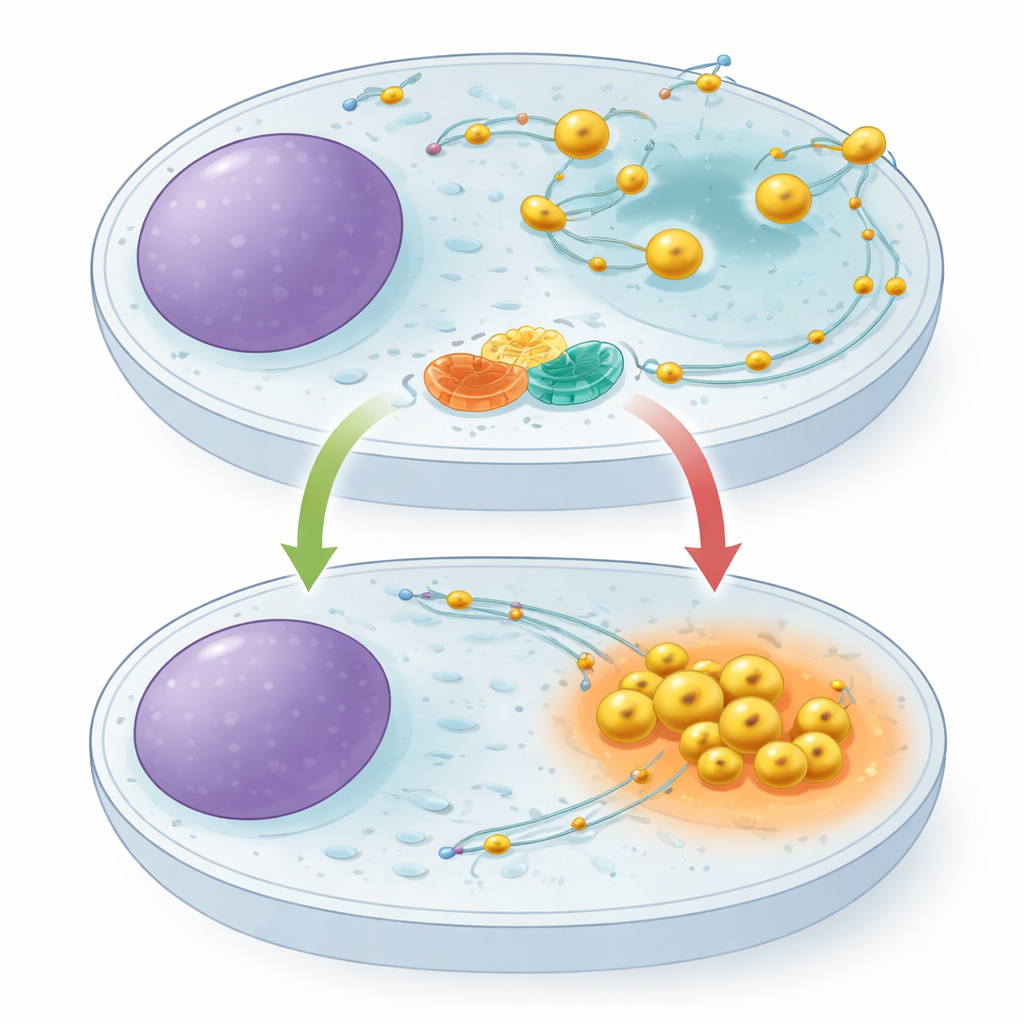
Lizozom Yüzeyinde Moleküler Bir Ortaklık
Protein avlama teknikleri ve kütle spektrometrisi kullanarak araştırmacılar TBC1D9B adlı bir proteinin TMEM55B adındaki bir lizozomal zar proteinine bağlandığını keşfettiler. TMEM55B lizozomun dış kabuğu boyunca yer alırken, TBC1D9B büyük ölçüde çözünürdür ve zara tutunabilir. Ekip, bu ikilisinin doğrudan bir kompleks oluşturduğunu gösterdi: saflaştırılmış TBC1D9B tüpler içinde TMEM55B’nin maruz kalan kısmına yapışıyor ve etiketli protein versiyonları hücre ekstraktlarından birbirlerini çekiyordu. Protein parçalarının dikkatli haritalanması, TBC1D9B’nin TMEM55B ile temas eden birkaç bölgesinin olduğunu ve TBC1D9B’yi lizozom yüzeyine konumlandırdığını, bununla birlikte katalitik aktiviteden sorumlu bölgeyi engellemediğini ortaya koydu.
Fren Bozulduğunda Lizozomlar Kontrolden Çıkar
Bu ortaklığın ne işe yaradığını görmek için yazarlar insan hücrelerinde TMEM55B veya TBC1D9B’yi CRISPR ile sildiler. Her iki durumda da lizozomlar artık çekirdeğin yakınında kümelenmiyor, bunun yerine hücre kenarına doğru dağılıyor ve hatları boyunca daha hızlı hareket ediyordu; bu, sürekli beslenmiş bir durumdaki hücreleri taklit ediyordu. Normal TBC1D9B’nin yeniden verilmesi doğru konumlanmayı geri getirirken, katalitik gücü olmayan bir versiyon getirmedi; bu da enzimatik aktivitenin gerekli olduğunu gösterdi. Hücreler aç bırakıldığında kontrol hücreleri lizozomlarını içeri çekti ve anahtar enzimlerin aktivitesindeki artış ve deney parçasının daha güçlü parçalanmasıyla sindirim güçlerini artırdı. TMEM55B veya TBC1D9B eksik hücreler bunu yapamadı: lizozomları periferide kaldı ve açlığa yanıt olarak degradatif tepkileri zayıfladı. Hücrelerin hasarlı bileşenleri kendi kendine sindirdiği süreç olan otofaji de bozuldu; otofaji raporlama cihazının işlenmesi daha az verimliydi ve adaptör proteini p62 birikti.
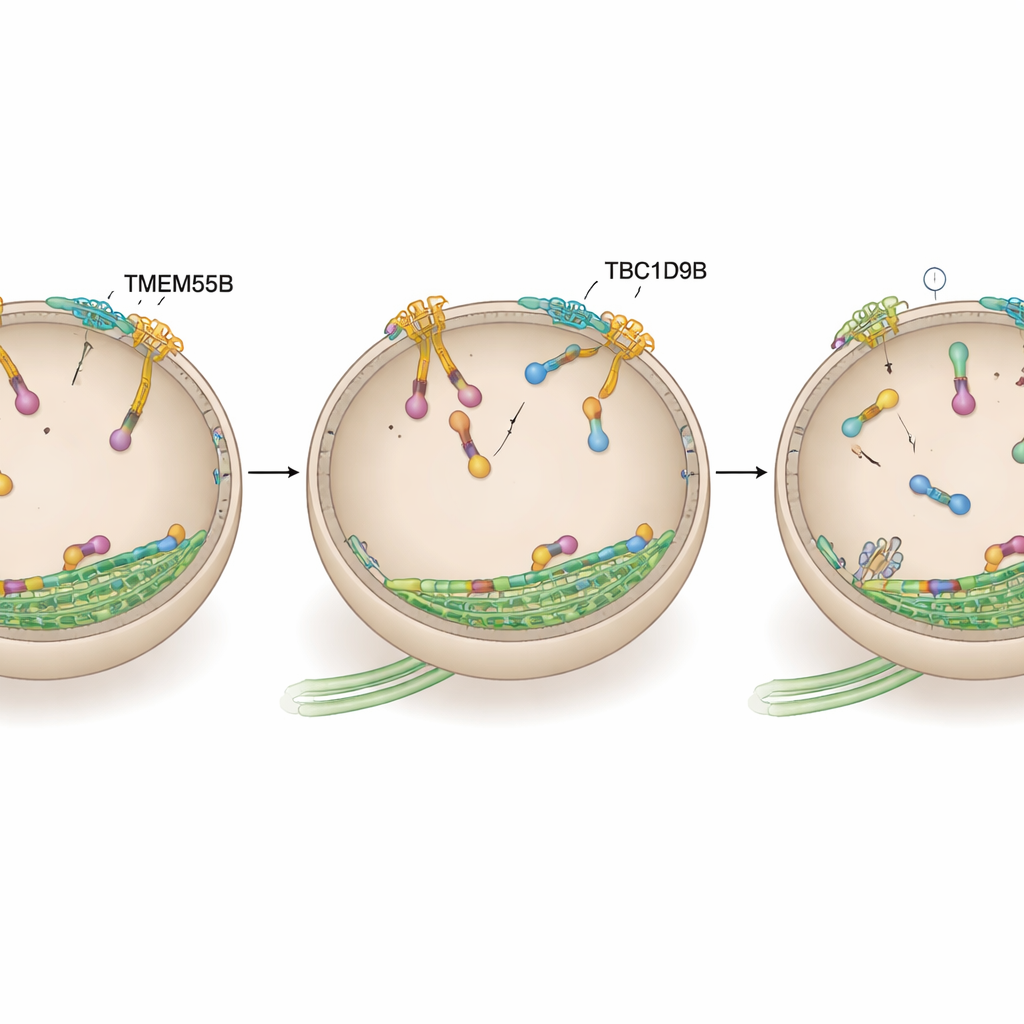
Lizozom Motorunu Kapatmak
Ekip daha sonra TBC1D9B’nin etkilerini ARL8 üzerinde doğrudan mı uyguladığını sordu, yani dışa doğru sürükleyen motor anahtarını kapatıp kapatmadığını. İnsan nöronlarında yakınlık etiketleme ve hücre hatlarında ile saflaştırılmış proteinlerde bağlanma testleri kullanarak TBC1D9B’nin ARL8B varyantının etkin, GTP‑yüklü formuna seçici olarak bağlandığını, inaktif formuna veya yakından ilişkili ARL8A’ya bağlanmadığını gösterdiler. Yapısal modelleme, TBC1D9B’deki kritik kalıntıların ARL8B’nin GTP cebine temas ettiğini öngördü. Biyokimyasal testlerde TBC1D9B, ARL8B’ye bağlı GTP’nin hidrolizini hızlandırdı ve böylece proteini “açık” durumdan “kapalı” duruma etkili biçimde çevirdi; bu kalıntılardan yoksun mutant bir TBC1D9B artık bunu yapamadı. Tutarlı olarak, TMEM55B veya TBC1D9B eksik hücrelerde lizozomlarda artmış ARL8B görüldü, oysa TBC1D9B’nin aşırı eksprese edilmesi lizozomları merkeze doğru çekti ve ARL8B aktivitesini düşürmeye benzer bir etki yarattı.
Hücresel Temizlik İçin Yeni Bir Kontrol Düğmesi
Son olarak yazarlar, ARL8B freninin TBC1D9B eksikliğinde görülen hücresel değişiklikleri açıklayıp açıklamadığını test ettiler. ARL8B tükenmişken lizozomlar TMEM55B veya TBC1D9B varlığına bakılmaksızın çekirdek yakınında kümelenmeye devam etti ve TBC1D9B kaybının neden olduğu otofaji kusurları büyük ölçüde baskılandı. Birlikte veriler, TMEM55B’nin TBC1D9B’yi lizozomlara getirdiği, burada ARL8B’yi inaktive ederek lizozomların dağılan, büyümeyi destekleyen bir durumdan merkezileşmiş, sindirim odaklı bir duruma geçmesine izin verdiği modelini destekliyor. Uzman olmayanlar için bunun anlamı, çalışmanın hücrelerin daha agresif biçimde geri dönüşüm yapmaya ne zaman karar vereceğini belirlemek için kullandıkları önemli bir düğmeyi ortaya çıkarmış olmasıdır; bu süreç beyin atık birikimi bozuklukları, metabolizma ve kanserle ilgili sonuçlar taşır.
Atıf: Duhay, V., Tian, M., Kosieradzka, K. et al. Control of lysosome function by the GTPase-activating protein TBC1D9B and its binding partner TMEM55B. Nat Commun 17, 2487 (2026). https://doi.org/10.1038/s41467-026-70345-y
Anahtar kelimeler: lizozomlar, otofaji, hücre sinyalleşmesi, organel taşınması, nörodejenerasyon