Clear Sky Science · tr
NAA40 ve NAC, insanlarda ortak-çevirimsel histon asetilasyonunda iş birliği yapar
Hücrelerin gen anahtarlarını nasıl ince ayarladığı
Her insan hücresinin içinde, yeni sentezlenen proteinler ribozom adı verilen protein üretim makinelerinden çıktıkça kimyasal olarak düzeltilir. Bu küçük değişiklikler bir proteinin nereye gideceğini, ne kadar süre dayanacağını ve hatta genlerimizin nasıl açılıp kapatılacağını belirleyebilir. Bu makale, NAA40 adlı çok özel bir protein ile NAC adlı bir yardımcı kompleksin ribozom üzerinde nasıl birlikte çalıştığını, histon proteinlerini—DNA’nın sarıldığı makara benzeri yapıları—nasıl modifiye ettiklerini ve bunun gen aktivitesini ve potansiyel olarak kanser gelişimini nasıl etkileyebileceğini ortaya koyuyor.
Histon davranışını değiştiren küçük bir kapak
Birçok insan proteini, başlangıç ucunda küçük bir kimyasal kap alır; buna N-terminal asetilasyon denir. DNA’yı kromatin halinde paketlemeye yardımcı olan histonlar H2A ve H4 neredeyse her zaman bu şekilde kaplanır. NAA40, bu histonlara üretim sırasında bu kapağı ekleme konusunda neredeyse tamamen uzmanlaşmış olmasıyla diğer enzimlerden ayrılır. Bu asetil işareti, aynı histon bölgesindeki fosforilasyon ve metilasyon gibi diğer kimyasal etiketlerle yarışır; dolayısıyla NAA40’un etkide bulunup bulunmaması DNA’nın ne kadar sık paketlendiğini ve genlerin nasıl düzenlendiğini değiştirebilir. Önemli olarak, NAA40 düzeylerindeki değişimler birkaç kanser ile ilişkilendirilmiştir ve bu da onu yeni tedavilere yönelik umut verici bir hedef yapar.
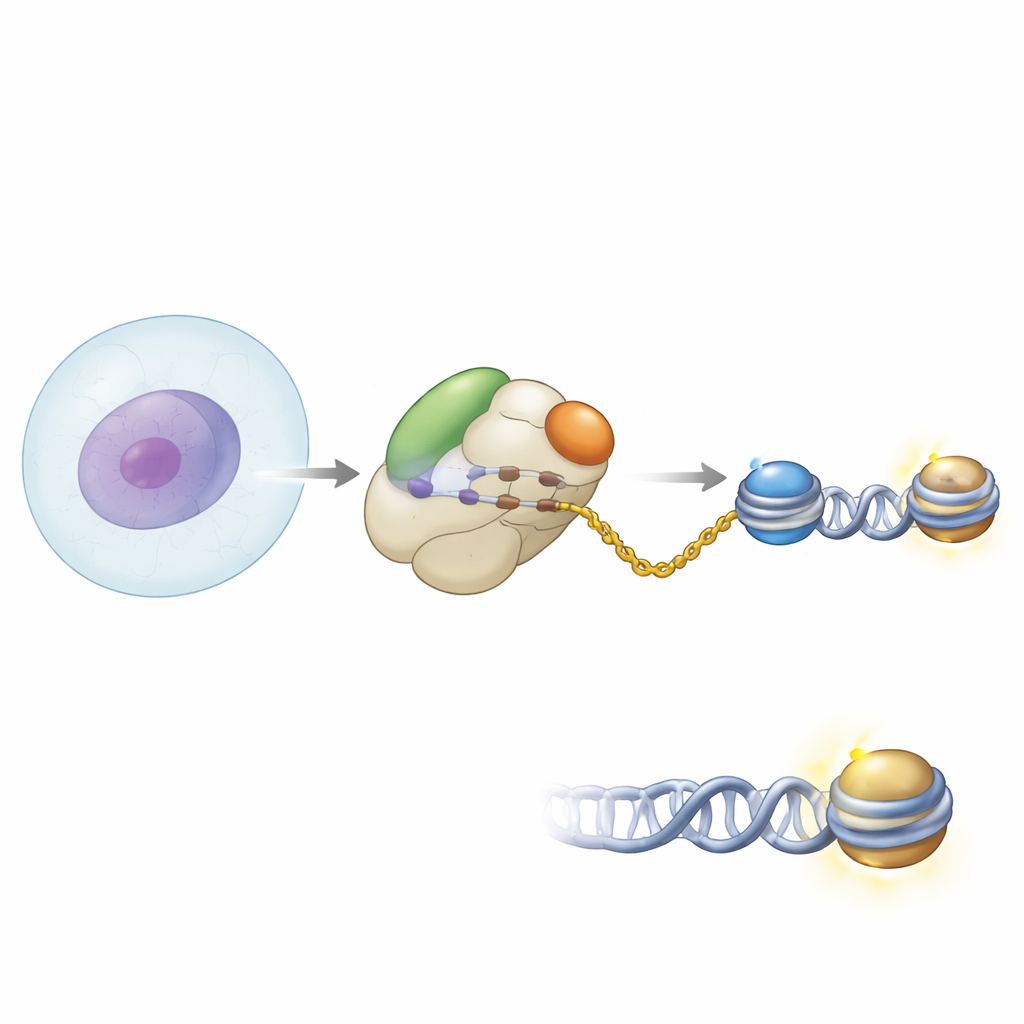
Protein fabrikasının kapısında ortaklık
Yazarlar, NAA40’ın insan ribozomu üzerindeki konumunu görmek için biyokimyasal yöntemler ve yüksek çözünürlüklü kriyo-elektron mikroskopisi kullandılar. NAA40’ın yeni doğan protein zincirlerinin çıktığı tünel çıkışının hemen üzerinde oturduğunu buldular. Orada tek başına çalışmıyor: yeni proteinler çıktıkça onlara gözetim yapan yaygın bir ribozom-bağlı yardımcı olan yenidoğan polipeptid–ilişkili kompleks (NAC) ile birlikte bağlanıyor. Yapısal anlık görüntüler, NAA40’ın kendisinin başlangıcında bulunan benzersiz pozitif yüklü bir helikal segment tarafından ribozoma ankrajlandığını, NAC’ın ise alt birimlerinden biri aracılığıyla ribozom yüzeyine bağlandığını gösterdi. NAC’ın esnek bir alanı NAA40 ile temas etmek için uzanıyor ve böylece enzimi ribozoma köprüleyerek yerleştiriyor.
NAC’ın histon ayarlaması için neden gerekli olduğu
Bu ortaklığın ne kadar önemli olduğunu test etmek için araştırmacılar bu etkileşimleri saflaştırılmış bileşenlerle deney tüplerinde yeniden kurdular. NAA40’ın tek başına ribozomlara yalnızca zayıf bağlandığını, ancak NAC varlığında ribozom bağlanmasının çok daha güçlü hale geldiğini gözlemlediler. NAA40 ile temas eden belirli bir “UBA” bölgesini NAC’tan çıkardıklarında bu güçlenmiş bağlanma ortadan kalktı. İnsan hücrelerinde NAC’ı azaltmak, NAA40’a bağımlı histon H4 asetilasyonunun azalmasına ve aynı histon kuyruğunda rakip bir fosforilasyon işaretinin artmasına yol açtı. Bu değişiklik NAA40 miktarını veya yerini değiştirmedi; bu da NAC’ın temel rolünün, histonlar üretilirken onların verimli bir şekilde modifiye edilebilmesi için NAA40’ı çeviren ribozomlara doğru şekilde işe alıp konumlandırmak olduğunu gösteriyor.
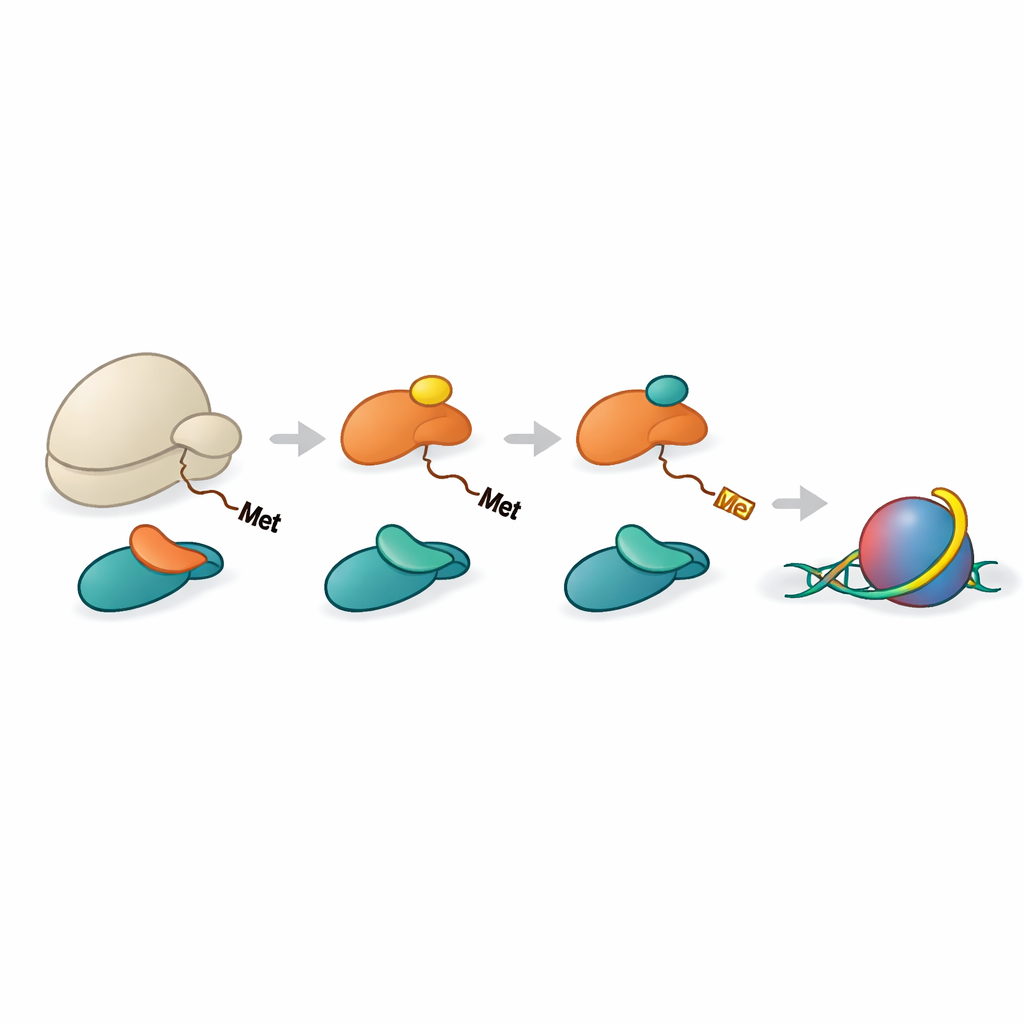
Histon işleme için koordineli bir montaj hattı
Histonlar H2A ve H4’ün NAA40 tarafından tanınabilmesi için önce başlangıçtaki metiyonin aminoasitini kaybetmeleri gerekir. Başka bir enzim olan METAP1 bu kesmeyi gerçekleştirir. Ekip, NAC’ın METAP1 ve NAA40’ı ribozomla birlikte getirmeye yardımcı olabileceğini ve peptid çıkışında çoklu-enzim bir montaj oluşturabileceğini gösterdi. Yeniden oluşturulmuş komplekslerin yüksek çözünürlüklü yapıları, METAP1 ve NAA40’ın ribozom üzerinde yan yana bağlandığını ve aktif bölgelerinin çıkış tünelinden neredeyse eşit mesafelerde konumlandığını ortaya koydu. Bu geometri, bir histon kuyruğu ribozomdan on iki veya daha fazla aminoasit uzadığında METAP1’in başlangıç metiyoninini çıkarabileceği ve NAA40’ın hemen ardından asetil kapağı ekleyebileceği anlamına gelir; böylece iki adım arasındaki gecikme en aza indirilir.
Gen kontrolü ve kanser için çıkarımlar
Genel olarak çalışma, NAA40’ın hücre içinde yalnızca histon arayıp bulup rastgele hareket etmediğini gösterir. Bunun yerine NAC tarafından ribozoma demirlenir ve sentezlendikleri anda histonları hazırlayan düzenli bir işlem istasyonunun parçası olur. Metiyonin uzaklaştırma ve asetil ekleme işlemlerini sıkı şekilde birbirine bağlayarak hücre, histon H2A, H4 ve DNA hasarıyla ilişkilendirilen varyant H2A.X’in hızla asetil işareti almasını sağlar; bu işaret kromatin yapısını ve gen ifadesini şekillendirebilir. Bu erken histon işaretleme adımındaki bozulmalar kanseröz büyümeyi destekleyebileceğinden, ribozom üzerindeki NAA40, NAC ve METAP1’in tam düzeninin anlaşılması, bu kritik epigenetik kontrol noktasını ince ayarlamaya yönelik ilaç tasarımına rehberlik edebilecek yapısal bir plan sunar.
Atıf: Guan, D., Denk, T., Klavaris, A. et al. NAA40 and NAC cooperate in co-translational histone acetylation in humans. Nat Commun 17, 2486 (2026). https://doi.org/10.1038/s41467-026-70279-5
Anahtar kelimeler: histon asetilasyonu, NAA40, ribozom, yenidoğan polipeptid ilişkili kompleks, epigenetik düzenleme