Clear Sky Science · tr
Asetilasyondan fosforilasyona hücre döngüsüne bağlı geçiş, zamanında merkezsoma olgunlaşmasını düzenler
Genetik Yükümüzü Doğru Yerde Tutmak
Vücudumuzdaki her hücre bölünmesi sırasında, DNA’sını son derece hassas bir şekilde paylaştırmak zorundadır. Bu süreç bozulduğunda hücreler kromozom kazanabilir veya kaybedebilir; bu, kanser ve diğer hastalıklarla ilişkilendirilen tehlikeli bir durumdur. Bu çalışma, hücrelerin kromozomları doğru ayırmak için gereken küçük yapıları zamanında oluşturmasına yardımcı olan moleküler bir zamanlayıcıyı ortaya koyuyor ve gelecekteki kanser karşıtı terapilerin hedefleyebileceği potansiyel bir zayıf noktayı açığa çıkarıyor.
Hücrenin Küçük Trafik Merkezleri
Her bölünen hücrenin merkezinde, kromozomları çeken lifler için trafik merkezi gibi davranan küçük yapılar olan merkezsomalar bulunur. Bir hücre bölünmeye girmeden önce, bu merkezsomaların “olgunlaşması” gerekir: yardımcı proteinlerle güçlenirler ve bölünme iğini oluşturan dinamik mikrotübüllerin güçlü organize edicileri haline gelirler. Bu olgunlaşma çok erken, çok geç veya hiç gerçekleşmezse, kromozomlar yanlış dağıtılır ve anormal kromozom sayısına sahip hücreler ortaya çıkar. Merkezsomaların tam doğru anda nasıl aktif hâle geldiğini anlamak hücre biyolojisinde uzun süredir süregelen bir sorundu.
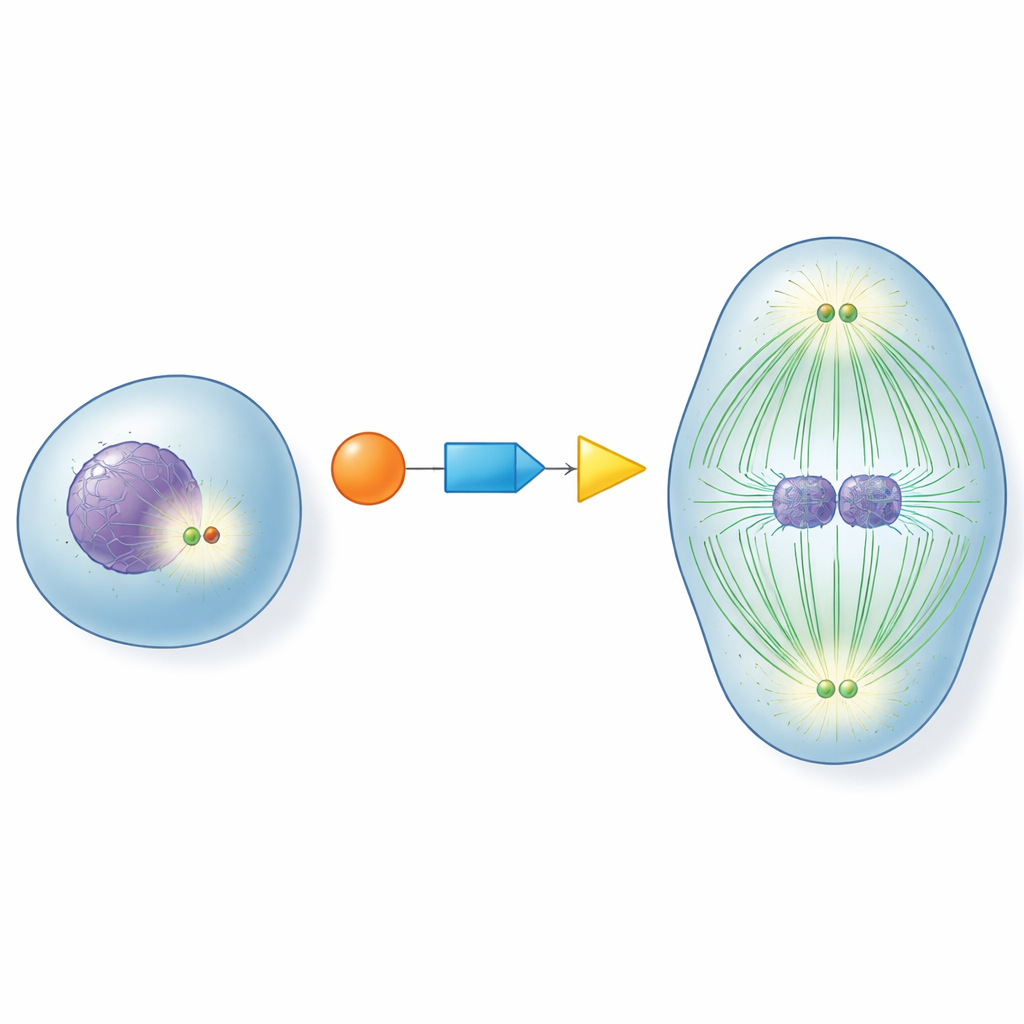
Mükemmel Zamanlama İçin Bir Moleküler Röle
Yazarlar zamanlayıcı olarak birlikte çalışan üç ana proteine odaklandı: hücre döngüsünün başlıca düzenleyicisi CDK1; daha çok DNA paketleyen proteinleri modifiye etmesiyle bilinen RNF40; ve hücre bölünmesinin ana itici gücü PLK1. RNF40’ın hücre döngüsü boyunca fiziksel olarak merkezsomalarda bulunduğunu ve doğrudan PLK1 ile bağlandığını keşfettiler. Hücreler bölünmeye yaklaşınca CDK1, RNF40’ı iki belirli noktada kimyasal olarak işaretliyor ve bu da RNF40’ın PLK1 için daha iyi bir tutunma alanı haline gelmesini sağlıyor. Bu CDK1–RNF40–PLK1 zinciri, PLK1’in merkezsomalara tam olarak bölünmenin geç hazırlık aşamasında ulaşmasını sağlayarak güçlü merkezsoma olgunlaşmasını, mikrotübül büyümesini ve iyi oluşmuş bipolar bir iğ oluşumunu tetikliyor.
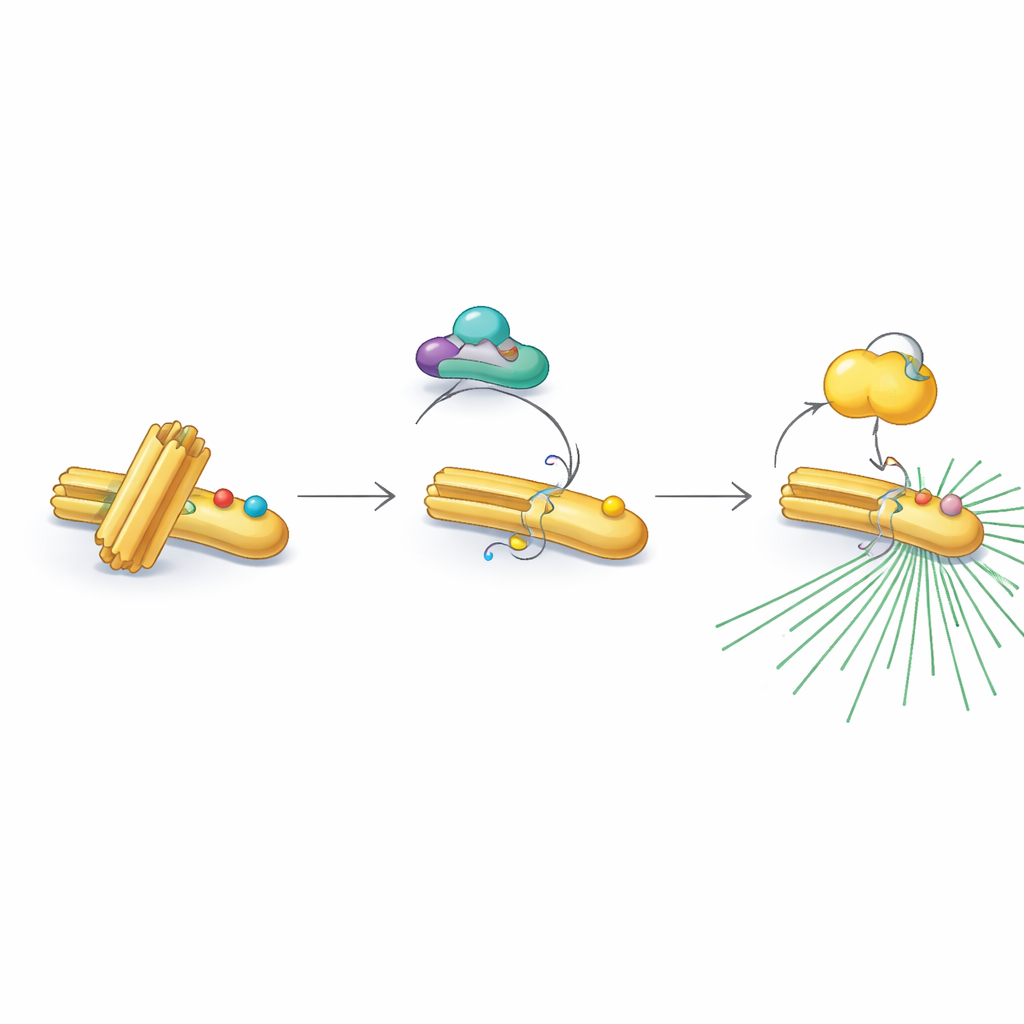
Şekil Değiştiren Bir Protein Anahtarı
İlginç bir şekilde, RNF40 her zaman bu etkinleştirici işaretleri kabul etmiyor. Bölünmeyen ve DNA kopyalama evrelerinde RNF40, iki yakın pozisyonda farklı bir kimyasal süs—asetil grupları—taşıyor. Bu asetil işaretleri PCAF adlı bir enzim tarafından ekleniyor ve daha sonra deasetilaz ortak HDAC1 tarafından siliniyor. Asetillenmiş RNF40, CDK1 tarafından modifikasyona direnç gösteriyor ve rölenin bir sonraki adımını etkili biçimde engelliyor. Hücreler son ön-bölünme aşamasına ilerledikçe HDAC1 asetil işaretlerini kademeli olarak siliyor ve CDK1’in bunun yerine fosfat grupları eklemesine izin veriyor. Bu asetilasyondan fosforilasyona dikkatle zamanlanmış geçiş, RNF40’ı “bekleme” durumundan PLK1’i çekmeye ve merkezsomayı çalıştırmaya hazır bir “aktif” duruma dönüştürüyor.
Zamanlama Bozulduğunda Ne Olur
Araştırmacılar bu anahtarın ne kadar hayati olduğunu incelemek için RNF40’ın artık fosforilasyon yapamayacağı veya asetilasyon-mimik hâlinde kalmaya zorlandığı hücreleri mühendisliklediler. Her iki durumda da PLK1 merkezsomalarda düzgün bir şekilde birikemedi. Bu hücrelerde merkezsomalardan mikrotübül büyümesinde zayıflama, kötü şekillenmiş iğler ve hizalanmamış kromozomlar görüldü. Birçoğu ekstra veya eksik kromozomla—aneuploidite olarak bilinen anormal bir durum—sonuçlandı ve bazıları binükleer hale geldi; bu, yıkıcı bölünme hatalarının işaretleriydi. Kanser modellerinde, “asetillenmiş” RNF40 durumunda kilitlenmiş hücreler farelerde daha küçük tümörler oluşturdu ve kolorektal kanser tedavisinde kullanılan yaygın kemoterapi ilaçlarına karşı daha duyarlıydı; bu da bu anahtarın bozulmasının tümör büyümesini yavaşlatabileceğini düşündürüyor.
İnsan Kanseriyle Bağlantılar ve Gelecek Olanaklar
Ekip hasta verilerini ve tümör örneklerini de inceledi. RNF40’ın kolorektal kanserlerde sıklıkla anormal derecede fazla olduğunu ve modifikasyon bölgelerine yakın bazı kanserle ilişkili mutasyonların onun fosforilasyonunu bozduğunu, dolayısıyla düzgün merkezsoma işlevini zayıflattığını buldular. Bu gözlemler yeni tanımlanan zamanlama mekanizmasını doğrudan insan hastalığına bağlıyor. Merkezsomaların ne zaman olgunlaşacağını ve kromozomların nasıl ayrılacağını koordine eden belirli bir proteini belirleyerek çalışma, hızlı bölünen kanser hücrelerini sağlıklı hücreleri daha az etkileyerek öldürücü bölünme hatalarına itebilecek hedeflenebilecek bir sinyal “düğümünü” öne çıkarıyor.
Güvenilir Hücre Bölünmesine Yeni Bir Kavrama
Uzman olmayanlar için temel mesaj, hücrelerin kromozomları ayıran makineyi tam olarak ne zaman etkinleştireceklerine tek bir protein olan RNF40 üzerindeki hassas ayarlı bir kimyasal anahtara güvenerek karar verdiğidir. Bu asetilasyondan fosforilasyona geçiş, yoğun bir kavşaktaki trafik lambası gibi davranır ve hücre gerçekten bölünmeye hazır olduğunda yalnızca yeşile döner. Lamba arızalandığında, hücreler bölünmede tökezler, genetik hatalar birikir ve kansere dönüşebilir. Bu anahtarı anlamak ve kontrol etmek, kanser hücrelerinin temiz bir şekilde bölünme yetisini sabote ederek seçici olarak kararsızlaştırılmasını sağlayacak yeni tedavi yolları açabilir.
Atıf: Li, J., Liang, J., Chen, G. et al. A cell cycle-dependent transition of acetylation to phosphorylation regulates timely centrosome maturation. Nat Commun 17, 2583 (2026). https://doi.org/10.1038/s41467-026-70271-z
Anahtar kelimeler: merkezsoma olgunlaşması, hücre bölünmesi, kromozom kararsızlığı, PLK1 sinyalleşmesi, kolorektal kanser