Clear Sky Science · tr
Fostriecin biyosentezinde kovalent savaş başlığı montajı, bifonksiyonel bir tioesteraz tarafından malonilasyon-laktonlaşma ve enzimatik demalonilasyonu içerir
Doğa küçük bir kimyasal savaş başlığını nasıl inşa ediyor
Kanser ilaçları ve antibiyotikler sıklıkla birkaç atomun özel bir düzenine dayanır—bir proteine tutunan ve onu devre dışı bırakan küçük bir “savaş başlığı”. Doğal bir bileşik olan fostriecin, hücre büyümesinde rol oynayan enzimlere karşı güçlü aktivite gösteren böyle bir moleküldür. Ancak karmaşık yapısı laboratuvarda üretimini veya modifikasyonunu zorlaştırır. Bu çalışma, bakterilerin fostriecin’in kritik savaş başlığını adım adım nasıl bir araya getirdiğini ortaya koyarak, kimyagerlerin yeni ilaçlar tasarlamak için ödünç alabileceği enzimsel hileleri açığa çıkarıyor.
Güçlü doğal ilaçlardaki özel kanca
Toprak bakterilerinden gelen birçok umut verici ilaç poliketidler adı verilen bir aileye aittir. Bu aile içinde bir alt grup, kimyagerlerin α,β-doymamış δ-lakton olarak adlandırdığı reaktif bir halka taşır; bu halka moleküler bir balık kancası gibi davranır. Belirli protein aminoasitleriyle kalıcı bağ oluşturabilir ve böylece önemli biyolojik anahtarları kapatabilir. Fostriecin ve ilgili moleküllerde bu kanca, hücre bölünmesini kontrol eden belirli enzimlere yönelmelerine yardımcı olan bir fosfat grubu ile eşleştirilmiştir. Bu özellikler onları çekici birer antikanser adayına çevirir, ancak aynı reaktivite ve yapısal karmaşıklık sentezlerini zorlaştırır ve depolama sırasında kararsız olmalarına neden olur.
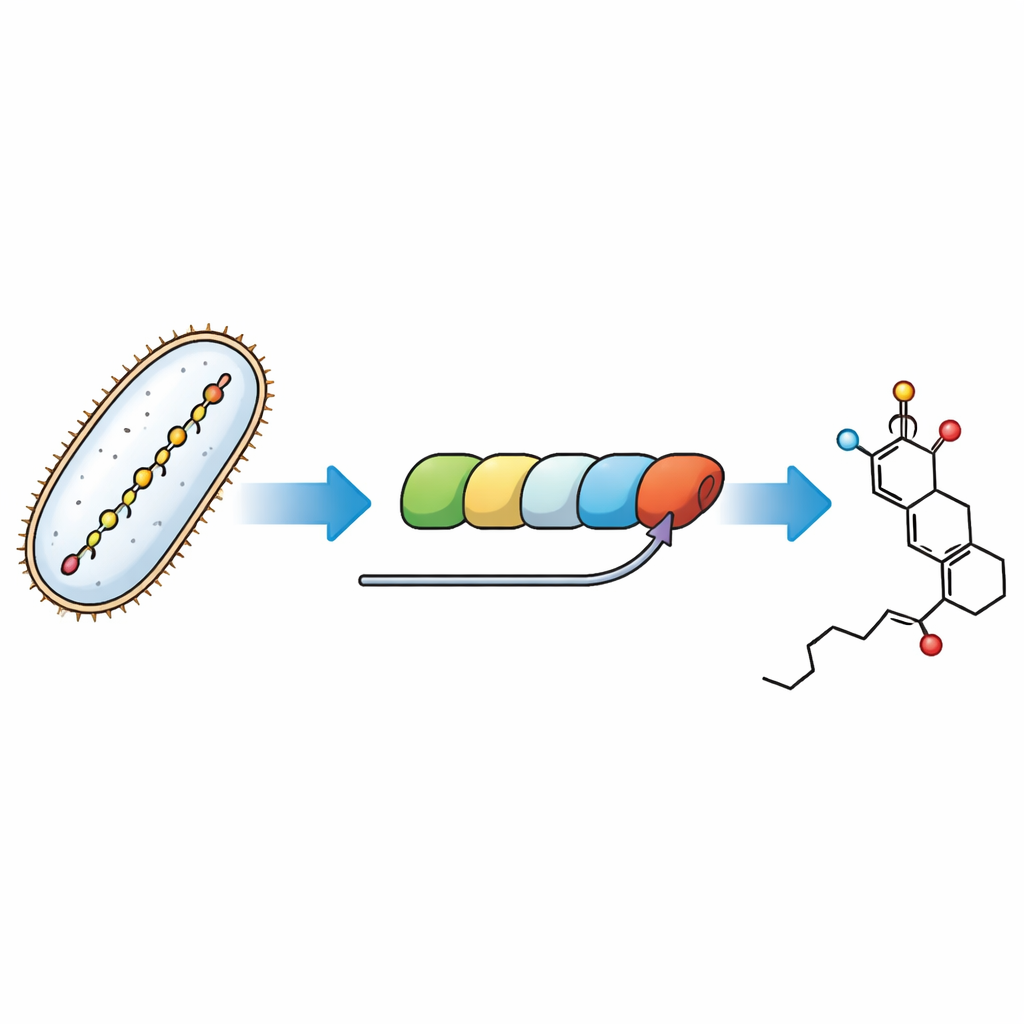
Moleküler montaj hattının son adımlarını izlemek
Bakteriler fostriecini, her istasyonun büyüyen karbon zincirini uzattığı ve şekillendirdiği modüler devasa bir protein makinesi olan bir poliketid sentaz kullanarak inşa eder. Burada ele alınan bulmaca, bu makinenin son modülünün savaş başlığı halkasını nasıl oluşturduğu ve daha sonra çıkarılması gereken geçici bir “tutacak” olan malonil grubunu nasıl yerleştirdiğidir. Yolu saflaştırılmış enzimlerle ve doğal ara maddelerin dikkatle tasarlanmış küçük moleküllü taklitleriyle test tüplerinde yeniden kurarak, araştırmacılar bireysel adımları izleyebildi ve bunları montaj hattının belirli kısımlarına atayabildi.
Beklenmedik bir yeteneğe sahip çok görevli bir enzim
Araştırma ekibi, montaj hattının son istasyonunun FosTE adlı bir domainin daha önce görülmemiş bir şekilde davrandığını keşfetti. Bu domainlerin tipik versiyonları bitmiş ürünleri sadece hattan keser. Buna karşılık FosTE, önce ortak bir hücresel yapı taşından bir malonil parçasını alıp büyüyen zincirdeki belirli bir oksijen yerine aktarır, sonra zincirin halkayı kapatacak şekilde kıvrılmasına yardımcı olur. FosTE’deki tek bir reaktif serin amino asidin mutasyonu her iki aktiviteyi de durdurur. Yapısal modelleme, aktif bölgede malonil parçasını kavrayan ve transfer için konumlandıran iki pozitif yüklü arginin kalıntısına işaret ediyor—normalde farklı bir enzim türü tarafından yürütülen işlevler. Bu argininlerin nötr residülere değiştirilmesi malonil transfer adımını ortadan kaldırırken temel halka oluşumunu büyük ölçüde etkilemez; bu da onların kritik rollerini doğrular.
Savaş başlığını kilitlemek ve israfı önlemek
Halka oluşturulduktan ve geçici malonil grubunu taşıdıktan sonra, bu grubu çıkarıp tamamen silahlanmış savaş başlığını ortaya çıkarmak için başka bir enzim, FosM, gereklidir. Çalışma, FosM’nin yalnızca bir başka enzim olan geniş özgüllüklü bir kinaz olan FosH, molekülün yakın bir konumuna fosfat ekledikten sonra verimli çalıştığını gösteriyor. Araştırmacılar malonillanmış halkayı yalnızca FosM’ye sunduklarında, sadece mütevazı bir dönüşüm gerçekleşti. Önce FosH eklendiğinde ise malonil grubunun neredeyse tamamen çıkarılması ve son reaktif birimin oluşumu sağlandı. Önemli olarak, FosH yan reaksiyonlardan kaynaklanan ilgili “sapma” ara maddelere de fosfat ekleyebilir; böylece bunları işlemeye kazanıp ölü uç ürünler olarak kaybolmalarını engeller.
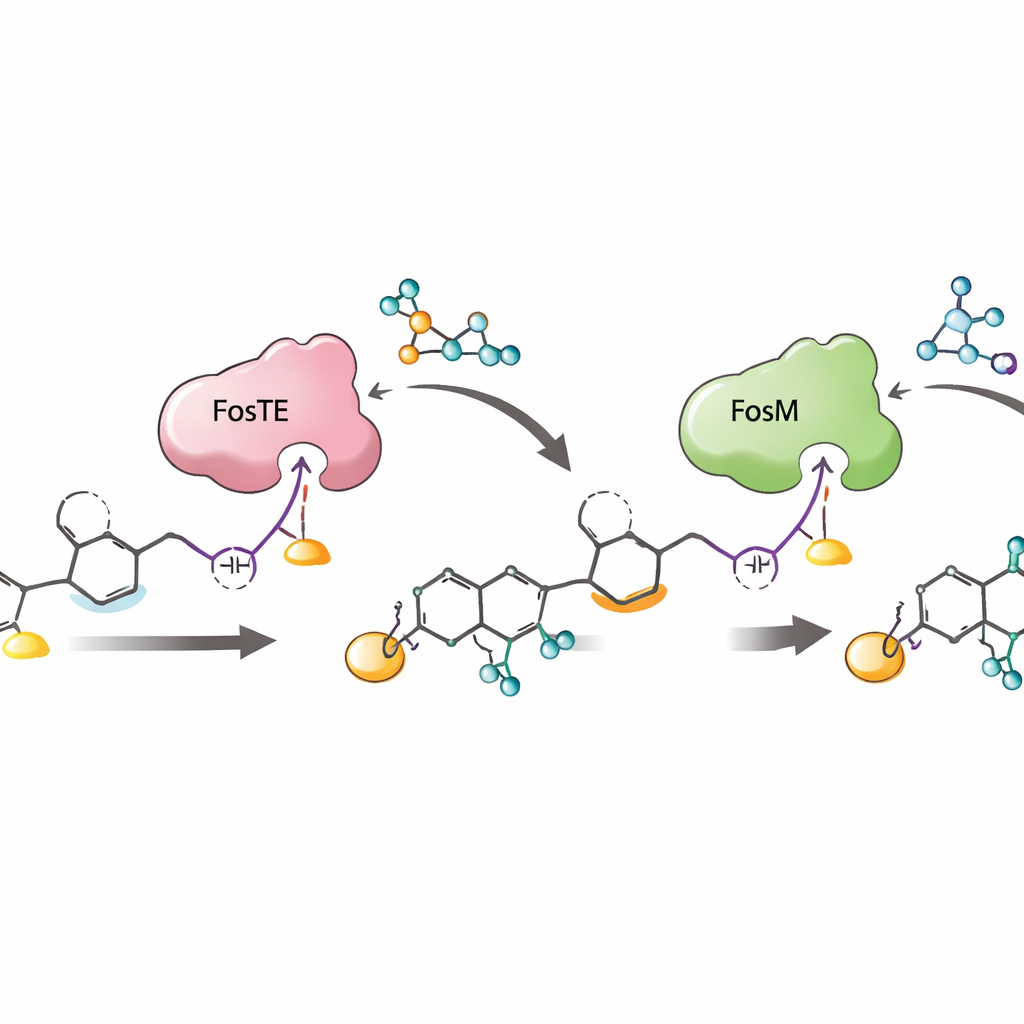
Bu enzimatik koreografinin önemi
Bir arada alındığında, çalışma sıkı bir şekilde düzenlenmiş bir sırayı ortaya koyuyor: montaj hattında zincir uzaması, FosTE kaynaklı malonil eklenmesi ve halka kapanması, FosH tarafından fosforilasyon ve son olarak FosM tarafından tetiklenen malonil çıkarılması. Bu sıra sadece hassas savaş başlığını verimli bir şekilde inşa etmekle kalmaz, aynı zamanda kararsız ara maddelerin parçalanmasını önler ve en etkili ilaç adayı formu olan fosforillı versiyonun üretimini maksimize eder. Tek bir enzim domaininin hem büyüyen bir molekülü süsleyip hem serbest bırakabilmesini ve partner enzimlerin reaktif ara maddeleri nasıl ince ayarlayıp kurtardığını ortaya koyarak, çalışma savaş başlığı taşıyan yeni poliketidlerin mühendisliği ve fostriecin benzeri karmaşık antikanser ajanlara daha kısa, daha verimli sentetik yollar kurmak için bir yol haritası sunuyor.
Atıf: Nguyen, L.N.K.T., Schlotte, L., Hoffmann, J. et al. Covalent warhead assembly in fostriecin biosynthesis involves malonylation-lactonisation by a bifunctional thioesterase and enzymatic demalonylation. Nat Commun 17, 2365 (2026). https://doi.org/10.1038/s41467-026-70144-5
Anahtar kelimeler: fostriecin, poliketid biyosentezi, enzim mühendisliği, doğal ürün savaş başlıkları, kemoişlemsel sentez