Clear Sky Science · tr
tRNA modifikasyonlarının oksidatif desülfürasyonu ile translasyonel düzenleme
Hücreler Stres Altındayken Protein Üretimini Nasıl Ayarlar
Her hücre hangi proteinlerin üretileceğine, hangi hızla üretileceğine ve üretimin ne zaman yavaşlatılacağına karar vermek zorundadır. Bu çalışma, transfer RNA (tRNA) moleküllerinde hücre ortamı iltihap veya metabolik stres gibi durumlarda daha oksitleyici hale geldiğinde protein üretimini geri çeken ince bir kimyasal anahtarı ortaya koyuyor. Araştırmacılar bu anahtarın memeli hücrelerinde ve tüp içi sistemlerde nasıl davrandığını izleyerek, RNA’daki hasar benzeri değişikliklerin aslında düzenleyici bir sinyal olarak işlev görebileceği yeni bir yol keşfediyor.
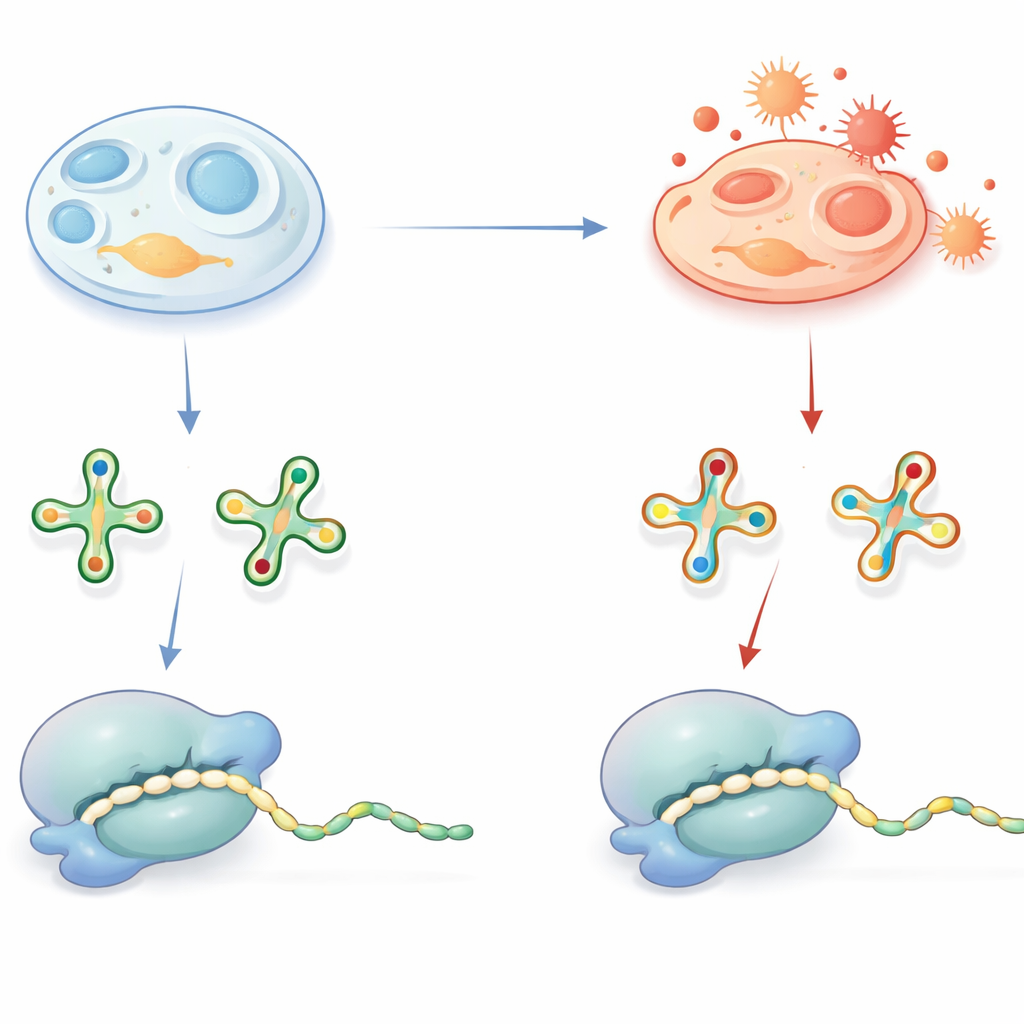
tRNA Üzerindeki Küçük İşaretlerin Büyük Sonuçları
tRNA’lar, haberci RNA’daki üç harfli “kelimeleri” okuyan ve protein sentezi sırasında eşleşen aminoasitleri getiren adaptörler olarak görev yapar. Bu işi doğru ve verimli yapmak için birçok tRNA, özellikle her kodonun üçüncü harfiyle temas eden kilit konumda özel kimyasal süslemeler taşır. Yaygın süslemelerden biri, uridin bazı üzerindeki kükürt içeren bir grup olup genellikle 2-tiouridin türevi olarak yazılır. Sağlıklı koşullarda bu kükürt grubu, tRNA’nın A veya G ile biten doğru kodonları tanımasına yardımcı olur ve hızlı, hatasız translasyonu destekler. Bu süslemelerdeki kusurların insan hastalıklarına yol açtığı zaten bilinmekte olup önemlerini vurgular.
Oksidatif Stres tRNA’yı Yeniden Yazdığında
Çözümlemeyi artıran kükürt grubunun bir dezavantajı vardır: oksidasyona karşı kimyasal olarak savunmasızdır. Ekip, hücre içinde bu grubun gerçekten oksidatif koşullar altında çıkarılıp çıkarılmadığını ve bunun protein sentezi için ne anlama geldiğini sorguladı. Hassas kütle spektrometrisi kullanarak, fare dokularında, domuz mitokondrilerinde, bakterilerde, mayada ve çeşitli insan hücre hatlarında oksitlenmiş, kükürtsüz tRNA bazı versiyonlarını — h2U türevleri olarak adlandırılan — tanımladılar. Bir bakteriyel tRNA izleyicisi ile yapılan zekice bir spike-in deneyi, bu h2U işaretlerinin örnek hazırlığı sırasında oluşan artefaktlar olmadığını, canlı hücrelerde meydana geldiklerini gösterdi. Oksitlenmiş versiyonlar yalnızca bir tRNA fraksiyonunda bulunmasına rağmen, bollukları doku ve hücre tiplerine göre değişiyordu; bu da hücresel redoks durumunun ve antioksidan kapasitenin bu dönüşümün ne sıklıkta gerçekleştiğini etkilediğini düşündürüyor.
Oksitlenmiş tRNA’lar Montaj Hattını Nasıl Yavaşlatır
Araştırmacılar daha sonra bu değiştirilmiş tRNA’ların protein sentezi sırasında nasıl performans gösterdiğini test ettiler. Kükürt içeren formu toplu tRNA’da kimyasal olarak oksitlenmiş h2U formuna dönüştürdüler ve tam olarak yeniden oluşturulmuş bir insan translasyon sistemini in vitro kullandılar. Üretimi bu modifiye tRNA’lara güçlü şekilde bağımlı bir raporör protein, tRNA’lar desülfürize edildiğinde belirgin şekilde azalmış çıktı gösterirken, etkilenen kodonlardan kaçınan kontrol raporörü normal şekilde çevrildi. Biyokimyasal testler bunun nedenini ortaya koydu: lizine, glutamine ve glutamete ait oksitlenmiş tRNA’lar aminoasitleriyle çok daha az verimli şarj edilirken, karşılık gelen arginin tRNA’ları büyük ölçüde korundu. Önemli olarak, h2U taşıyan tRNA’lar hâlâ hücrelerden elde edilen ribozom-bağlı (polizomal) fraksiyonlarda görünüyordu; bu da onların translasyona katıldığını ama düşük verimle yaptıklarını gösteriyor.
Zayıflamış Kodon Okumanın Yapısal Görünümü
Oksidasyonun kodon okumayı tam olarak nasıl değiştirdiğini görmek için ekip, insan lizine tRNA’sı ve belirli kodonlarla programlanmış bakteriyel ribozomları yüksek çözünürlüklü kriyo-elektron mikroskopisi ile görüntüledi. Normal, kükürt içeren durumda, tRNA’nın “wobble” pozisyonundaki modifiye baz ya A ile biten bir kodonla standart bir baz eşleşmesi ya da G ile biten kodonla özel bir wobble eşleşmesi oluşturuyor ve her ikisi de ribozomun kodlama merkezinde sıkıca yerleşiyordu. Desülfürasyon sonrasında aynı baz yalnızca A ile biten kodonla zayıf tek bir temas kurabiliyor ve G ile biten kodonla daha az stabil bir wobble çifti oluşturuyordu. Bağlanma deneyleri bu yapılarla örtüştü: oksitlenmiş lizine tRNA temelde AAA kodonunu tanıma yeteneğini kaybetmiş ve AAG kodonunu çok daha az verimli tanımıştı. Birlikte, bu bulgular küçük görünen bir kimyasal değişikliğin kodon-spesifik translasyon yavaşlamalarına dönüşebileceğini gösteriyor.
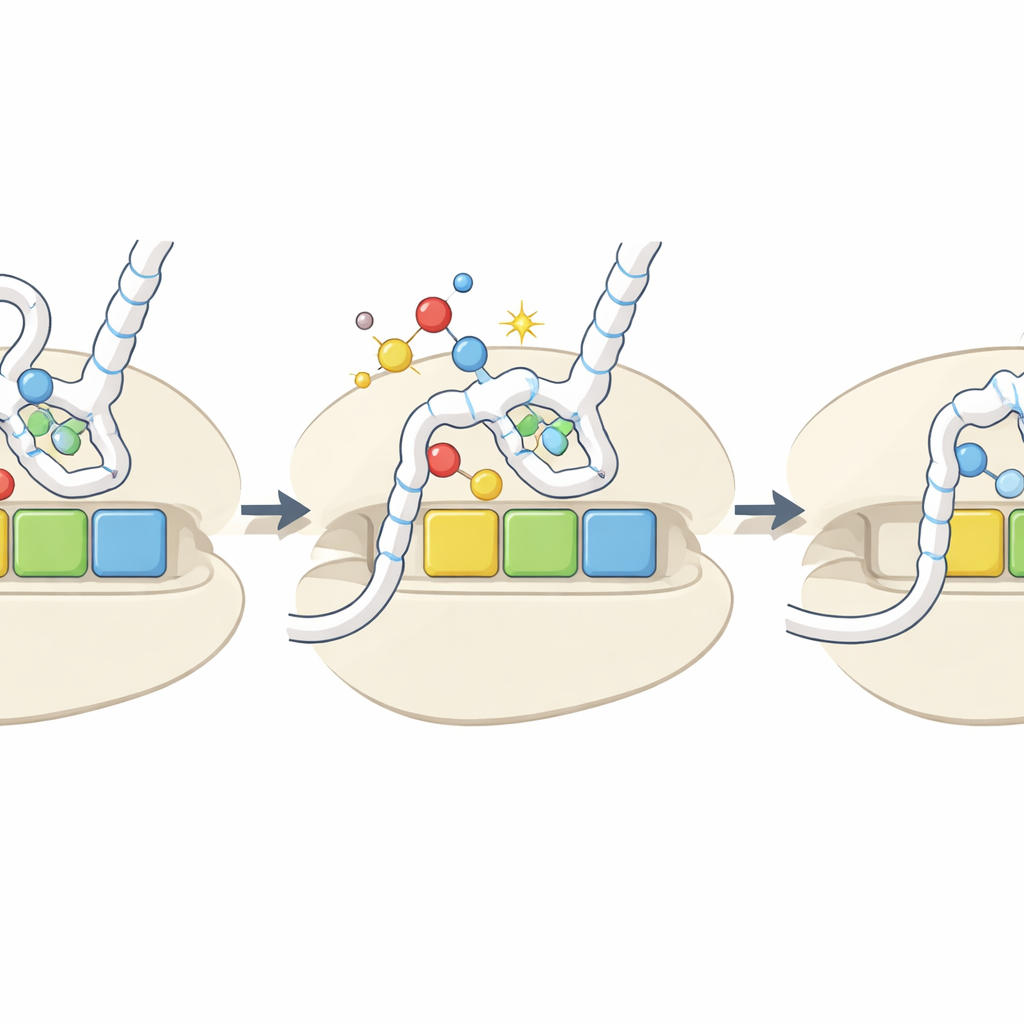
Hasar Sinyali Olarak İşleyen Düzenleyici Bir Düğme
Genel olarak çalışma, önemli tRNA bazlarından kükürdün oksidatif olarak uzaklaştırılmasının hücrenin redoks ortamı için yerleşik bir sensör görevi gördüğünü öne sürüyor. Oksidatif stres altında daha fazla tRNA h2U formuna dönüştürülür; bu formlar zayıf şarj edilir ve belirli kodonlara zayıf bağlanır. Bu, bu kodonlardaki translasyonu seçici olarak yavaşlatır, etkilenen mRNA’ların kararlılığını değiştirebilir, proteinlerin katlanmasını etkileyebilir ve ribozomlar takıldığında stres yanıtı yollarını tetikleyebilir. Oksitlenmiş işaretler nispeten nadir olsa da ve düzeyleri deneysel streste her zaman keskin şekilde artmasa da, kodon- ve amino asit-spesifik etkileri, mütevazı değişikliklerin bile zorlu koşullarda hangi proteinlerin üretileceğini ve ne hızda üretileceğini yeniden şekillendirebileceği anlamına gelir.
Atıf: Mo, Y., Ishiguro, K., Miyauchi, K. et al. Translational regulation by oxidative desulfuration of tRNA modifications. Nat Commun 17, 2125 (2026). https://doi.org/10.1038/s41467-026-70126-7
Anahtar kelimeler: tRNA modifikasyonu, oksidatif stres, protein sentezi, translasyon düzenlemesi, RNA hasarı