Clear Sky Science · tr
tRNA'ya Bağımlı Tirozin Kullanımını Hedeflemek, Hepatosellüler Karsinomda Metabolik Bir Açığı Ortaya Çıkarıyor
Kanser Hücrelerini Yaygın Bir Yapı Taşından Yoksun Bırakmak
Tüm hızlı bölünen hücrelerde olduğu gibi karaciğer kanseri hücreleri de proteinlerin küçük yapı taşları olan amino asitlere sürekli erişim ister. Bu çalışma, en yaygın karaciğer kanseri türü olan hepatosellüler karsinomun beklenmedik bir zayıflığı olduğunu gösteriyor: enerji üretimi ve hayatta kalma için tirozin amino asidine güçlü biçimde bağımlı olması. Kanser hücrelerinin tirozin kullanımını seçici olarak sınırlayarak araştırmacılar tümör büyümesini yavaşlatabildiler, kanser hücrelerinin enerji santrallerine zarar verdiler ve yeni tedavilerde kullanılabilecek bir hücre ölümü biçimini tetiklediler.
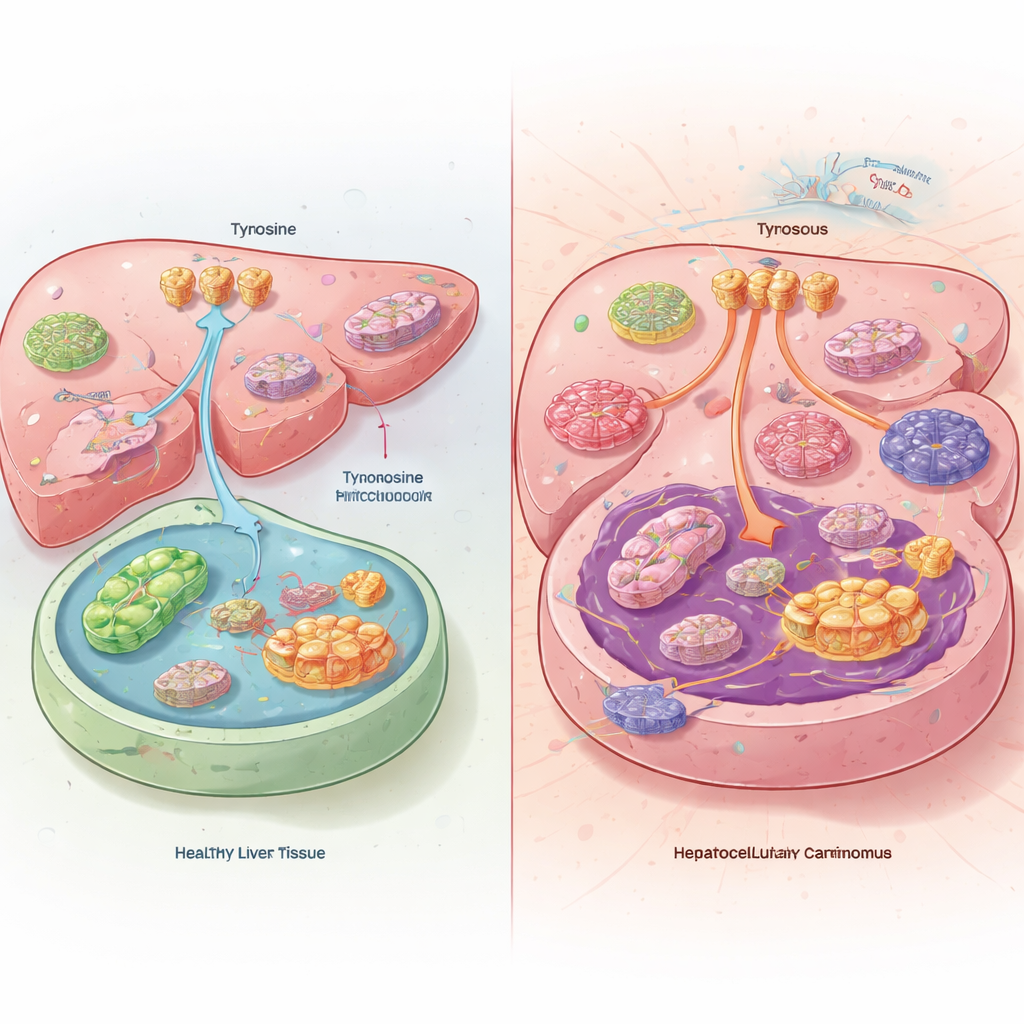
Karaciğer Tümörlerinde Gizli Bir Dengesizlik
Araştırma ekibi, hastalardan ve farelerden alınan karaciğer tümörlerini sağlıklı karaciğer dokusuyla karşılaştırdığında şaşırtıcı bir durum buldu. Kanser hücrelerinin içinde tirozin düzeyleri aslında düşüktü, oysa tümörler kan dolaşımından daha fazla tirozin çekiyor ve bunun daha azını parçalıyordu. Tirozini yakıt olarak yakmak yerine karaciğer tümörleri onu protein üretimine yönlendiriyordu. Kanserler bunu hücre yüzeyindeki tirozin taşıyıcılarının aktivitesini artırıp karaciğerde tirozini normalde parçalayan enzimlerin etkinliğini azaltarak başardı. Tirozinsiz diyetle beslenen farelerde tümörler daha küçük gelişti ve yaşam süreleri uzadı; diyete ekstra tirozin eklenmesi ise kanserlerin daha hızlı büyümesine yol açtı.
Kanserin Protein Üretimini Yeniden Devreye Sokma Yolu
Araştırmacılar bu tirozin açlığını güçlü bir kanser sürükleyici gen olan MYC’e kadar izledi. Karaciğer tümörlerinde MYC, tirozini belirli bir transfer RNA’sına (tRNA-TyrGUA) bağlayan YARS1 adlı proteini açığa çıkarıyor. Bu yüklü tRNA, ribozomların tirozin açısından zengin proteinler inşa etmesi için gerekli. Çalışma, karaciğer kanserlerinin hem YARS1’i hem de ona karşılık gelen tRNA’yı artırarak tirozinin protein sentezine ayrıcalıklı bir hat üzerinden akmasını sağladığını gösterdi. Bu hattı bozmak—tirozin düzeylerini düşürmek, YARS1 ya da tRNA-TyrGUA’yı susturmak veya tirozin bağlanmasını engellemek—plak kultürlerinde ve farelerde karaciğer kanseri hücrelerini belirgin şekilde zayıflattı ve yüksek protein üretim ihtiyaçlarına sıkı bağlı bir metabolik açık ortaya çıkardı.
Enerji Santrallerini ve Lipid Dengesini Felç Etmek
RNA, protein üretimi ve metabolitlerin genom çapında ölçümlerini birleştirerek ekip, tirozin kısıtlamasına özellikle hassas iki hedef belirledi. Bunlardan biri, hücrenin enerji üreten makinesinin temel parçalarından mitokondriyal kompleks I’in bir bileşeni olan NDUFB8’di. Diğeri ise doymuş yağları hücre zarlarında ve damlacıklarda depolanması daha güvenli olan tekli doymamış yağlara dönüştürmeye yardımcı olan SCD1’di. Çeviri için tirozin kısıtlandığında NDUFB8 ve SCD1 üretimi düştü, oysa onların RNA düzeyleri büyük ölçüde değişmedi—bu, etkilenenin gen ekspresyonu değil çeviri olduğunu açıkça gösteriyor. Bunun sonucunda kompleks I kötü monte oldu, hücresel solunum azaldı, reaktif oksijen türleri arttı ve yağlar tekli doymamış formlardan kolayca okside olan daha kırılgan çoklu doymamış formlara kaydı.
Kanser Hücrelerini Demire Bağlı Bir Ölüme Sürüklemek
Biriken mitokondri hasarı ve kararsız yağlar karaciğer kanseri hücrelerini lipit peroksidasyonu ile tetiklenen demire bağımlı bir hücre ölümü biçimi olan ferroptoz yönünde itti. Tümörler, GPX4 ve benzeri moleküller gibi doğal ferroptoz engelleyicilerini artırarak karşı koymaya çalıştı, ancak geniş çaplı bir CRISPR gen düzenleme ekranı bu koruyucuları devre dışı bırakmanın tirozin kısıtlamasını daha da öldürücü hale getirdiğini gösterdi. Hücre ve fare modellerinde, tirozin sınırlama stratejilerini GPX4 ya da BCL2 inhibitörleriyle—veya sorafenib ve venetoklaks gibi mevcut karaciğer kanseri ilaçlarıyla—eşleştirmek daha güçlü tümör kontrolü, daha küçük tümör yükleri ve daha uzun yaşam sağladı.
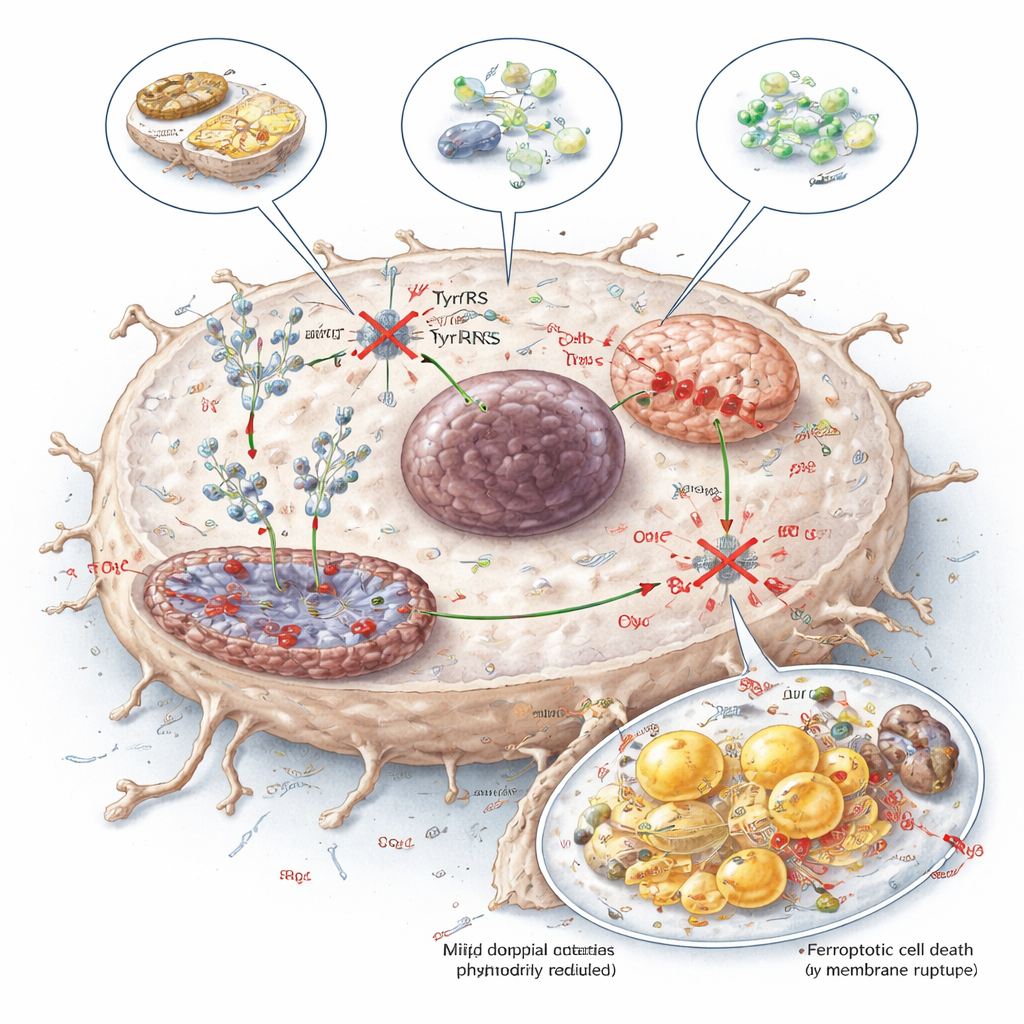
Metabolik Bir Zayıflığı Tedaviye Dönüştürmek
Bu zayıflığı pratik yollarla kullanmayı araştırmak için ekip üç yaklaşımı test etti: tirozin kısıtlı bir diyet, tirozini enzimatik olarak parçalayan bir enzim (TAL) ve YARS1’e bağlanmak için tirozinle yarışan küçük bir molekül olan tirozinol. Üçü de protein sentezi için tirozin bulunabilirliğini azalttı, NDUFB8 ve SCD1 düzeylerini düşürdü, mitokondri fonksiyonuna zarar verdi ve karaciğer tümörlerinde ferroptozu artırdı; farelerde normal dokular üzerinde yönetilebilir etkiler gösterdiler. Genel okuyucuya mesaj şu: karaciğer kanserleri tirozine sadece bir besin olarak değil, protein yapım makineleri için kesin bir yakıt olarak bağlanmış görünüyor. Bu bağımlılığı diyet, enzimler veya ilaçlarla hedeflemek, tümörleri zayıflatmak ve mevcut tedavilerin etkisini artırmak için umut verici yeni bir yol sunuyor.
Atıf: Zhang, H., Wang, Z., Zhao, Y. et al. Targeting tRNA-dependent tyrosine usage unveils a metabolic vulnerability in hepatocellular carcinoma. Nat Commun 17, 2244 (2026). https://doi.org/10.1038/s41467-026-70112-z
Anahtar kelimeler: karaciğer kanseri, amino asit metabolizması, tirozin, mitokondri, ferroptoz