Clear Sky Science · tr
Varyant-spesifik RNA yapı-küçük molekül etkileşimlerinin sistematik tanımlanması: RNA G-kuadrupleksleri örneği
Geleceğin ilaçları için RNA’daki küçük değişikliklerin neden önemi var
Çoğumuz benzersiz olmamızı sağlayan DNA’da küçük farklılıklar miras alırız. Bu küçük değişiklikler, hücrelerimizdeki RNA moleküllerinin kıvrımlarını ince biçimde yeniden şekillendirebilir. Yeni çalışma, bu tür genetik ince ayarların RNA’yı hedef alan deneysel ilaçların tutuşunu nasıl değiştirdiğini görmenin bir yolunu sunuyor. Bu önemli çünkü aynı ilaç, özellikle kanser veya genetik hastalık bağlamında, kişiden kişiye çok farklı davranabilir.
İlaçların RNA’ya nereden dokunduğunu gösteren yeni yöntem
Birçok ilaç geliştirici artık hedef olarak yalnızca proteinleri değil RNA’yı da inceliyor. Küçük moleküller özel RNA biçimlerine tutunup genlerin okunma şeklini etkileyebilir, ancak şimdiye kadar çoğu yöntem yalnızca tek bir “referans” RNA dizisi üzerinde çalışıyordu. Gerçek hastalarda bulunan sayısız tek harflik değişikliği büyük ölçüde göz ardı ettiler. Yazarlar, binlerce RNA varyantını eşzamanlı olarak test edebilen ve her biri için küçük molekülün nereye bağlandığını tek nükleotid çözünürlüğünde saptayabilen yüksek verimli bir yaklaşım olan BIVID-MaP’ı geliştirdiler. 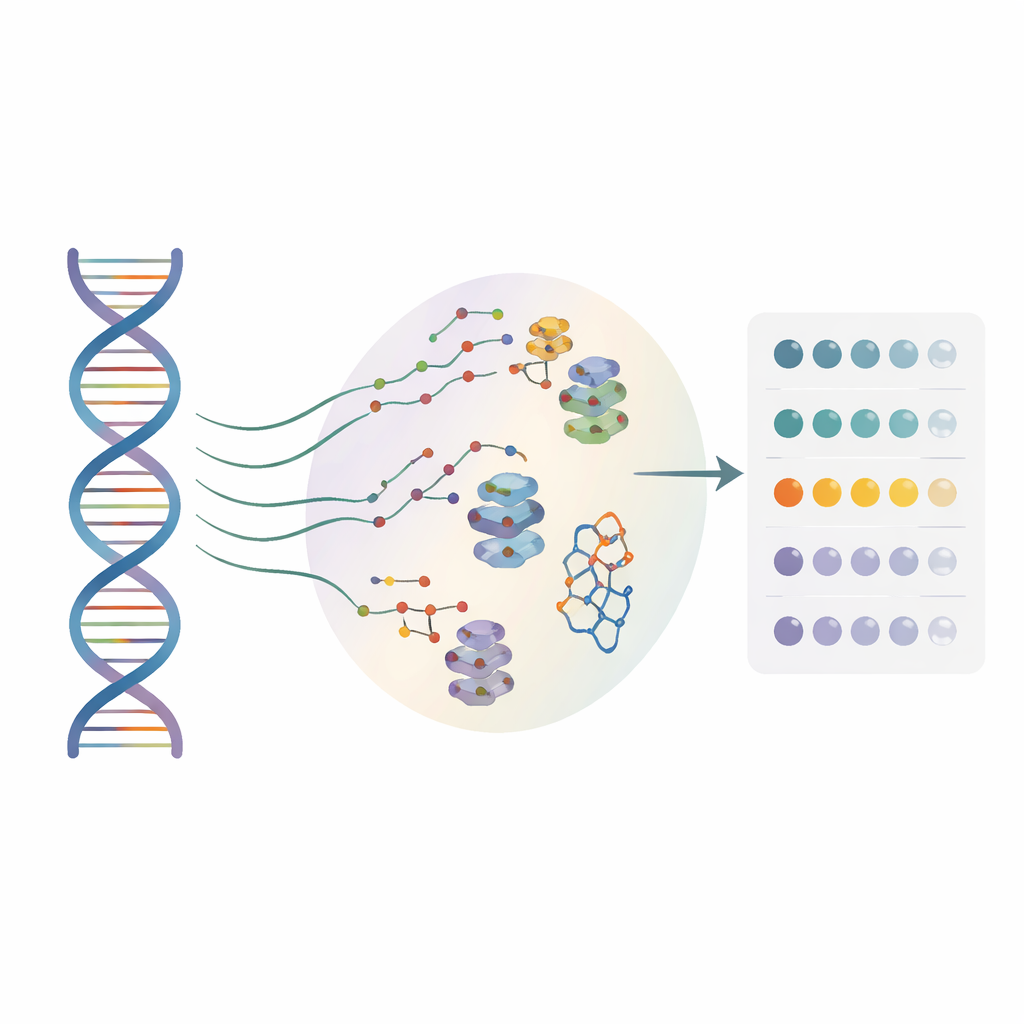
Kimyasal işaretleri okunabilir bir sinyale dönüştürmek
BIVID-MaP üç ana adımda işler. İlk olarak, ekip RNA’ya bağlanan küçük bir moleküle reaktif bir işaret bağlar. Bu işaretli bileşik tercih ettiği RNA yapısına — örneğin guanince zengin dizilerin oluşturduğu kompakt bir G-kuadrupleks gibi — yerleştiğinde, işaret yakındaki bir RNA bazıyla kalıcı bir kimyasal bağ oluşturur. İkinci olarak, özel bir enzim değiştirilmiş RNA’yı DNA’ya kopyalar. Bu kimyasal işaretlerle karşılaştığında genellikle tek bir bazı “atlayarak” kopyada küçük bir delesyon oluşturur. Üçüncü olarak, derin dizileme milyonlarca molekül arasındaki bu delesyon imzalarını okur. Çevreleyen dizinin neredeyse tamamı korunmuş olduğundan, delesyonlar karışık bir havuzdaki belirli genetik varyantlara doğru biçimde atanabilir.
Yöntemi kontrollü bir test vakasında kanıtlamak
BIVID-MaP’ın gerçekten varyant-spesifik bağlanmayı algıladığını doğrulamak için araştırmacılar normalde bir G-kuadrupleks oluşturan CD44 geninden bir RNA segmentini incelediler. Tek bir G’den A’ya değişim bu yapıyı bozar. Her iki versiyonun bulunduğu bir karışımda, berberin bazlı bir problara maruz kaldığında sadece sağlam form katlanmış bölge yakınlarında güçlü delesyon sinyalleri gösterdi ve bağımsız testler orada daha güçlü bağlanmayı doğruladı. Aynı şekli oluşturamayan mutant ise çok daha az delesyon ve daha zayıf bağlanma üretti. Diğer yaygın haritalama teknikleri ya bu farkı kaçırdı ya da kafa karıştırıcı arka plan üretti; bu da yeni yaklaşımın artan hassasiyetini ve özgüllüğünü vurguluyor.
Çok sayıda gen boyunca kansere bağlı mutasyonları taramak
Ekip sonra ölçeği büyüttü. Her biri tümörde bildirilen gerçek somatik mutasyonlarla eşleştirilmiş 283 kanser ilişkili genin 5′ dizilimsiz bölgelerinden (5′ UTR) oluşan bir RNA kütüphanesi yarattılar. G-kuadrupleks-benzeri yapıları tanıyan bir prob kullanarak, BIVID-MaP küçük molekül bağlanmasını güçlendiren veya zayıflatan çok sayıda mutasyonu ortaya çıkardı. DAXX ve ING2 gibi genlerde, guanince zengin dizilerdeki tek harf değişiklikleri bağlanmayı belirgin şekilde değiştirdi; bu, G-kuadrupleks oluşumunun bağımsız biyofiziksel testleri ve kütle spektrometrisiyle yapılan doğrudan bağlanma ölçümleriyle uyumluydu. Bazı durumlarda, bariz G-dizilerinin dışındaki mutasyonlar bile, yakınlardaki bazların eşleşme olasılığını ince biçimde değiştirerek yapısal “ensemble”i yeniden şekillendirdi ve tahmini genel katlanmayı çarpıcı biçimde değiştirmeden bağlanmayı kaydırdı. 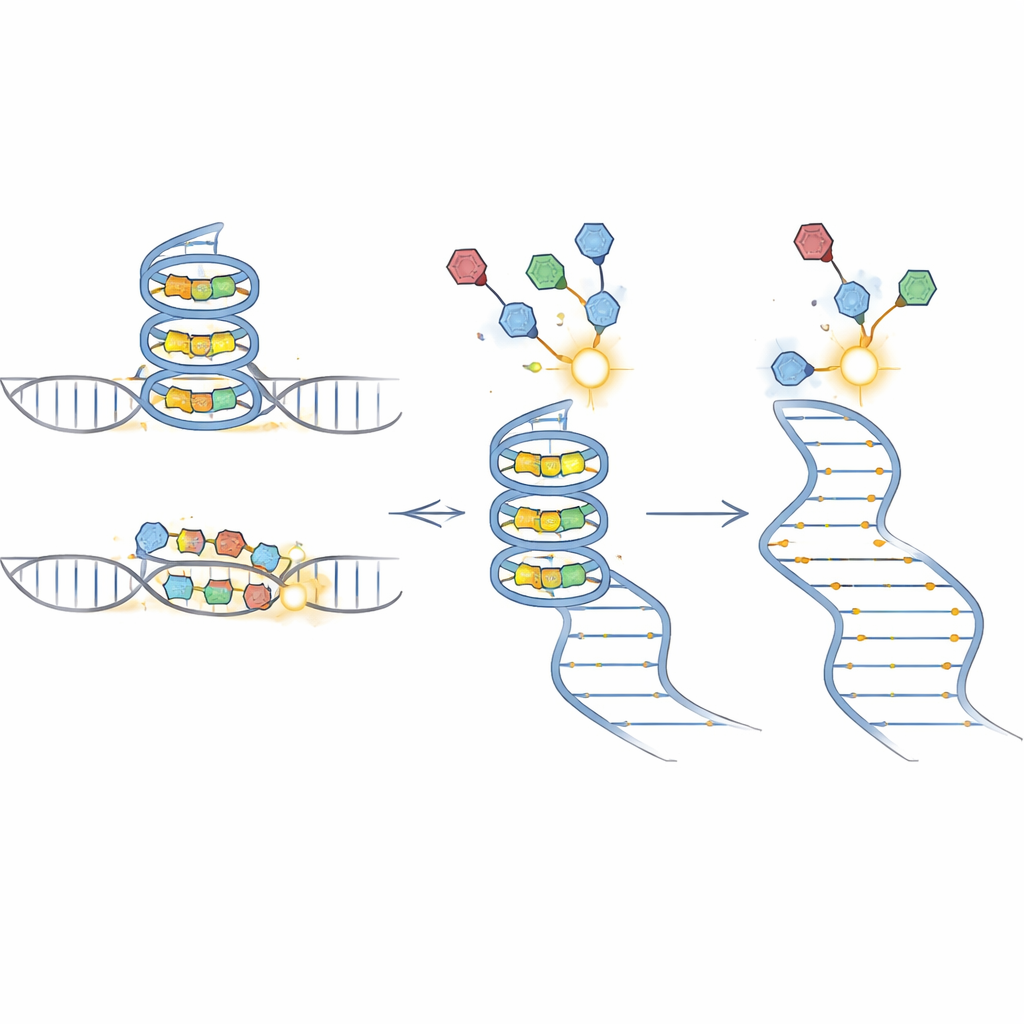
Bilgisayar tahminlerinin kaçırdıklarını görmek
Önemli olarak, mevcut RNA yapı ve G-kuadrupleks tahmin araçları sıklıkla BIVID-MaP’ın ortaya çıkardığı değişiklikleri öngöremedi. Hesaplamalı puanları neredeyse değiştirmeyen bazı varyantlar gerçek dünyada büyük bağlanma farkları üretti. Diğerleri G-kuadrupleks hedefleyen bir bileşik ailesi boyunca bağlanmayı etkiliyor gibi görünürken bazı mutasyonlar ilaç-spesifik etkiler gösterdi. Bu durum, tek nükleotid varyantlarının RNA katlanma manzarasını ve ilaç temaslarını diziden yalnızca çıkarım yapmakla zor tahmin edilebilecek şekilde ayarlayabileceğini gösteriyor.
Kişiselleştirilmiş RNA ilaçları için ne anlama geliyor
Yazarlar, BIVID-MaP’ın bireysel genetik farklılıkların RNA yapılarını ve bunların küçük molekül ilaçlarla etkileşimlerini nasıl yeniden şekillendirdiğini haritalamak için güçlü bir yol sunduğu sonucuna varıyor. Yerel kimyasal modifikasyonları hassas delesyon imzalarına dönüştürerek, yöntem binlerce varyantı paralel olarak tarayabilir ve ilaç bağlanmasını anlamlı biçimde değiştirenleri vurgulayabilir. Uzun vadede, bu tür haritalar çeşitlilik gösteren hasta popülasyonlarında daha etkili ve daha güvenli RNA-hedefli ilaçların tasarımına rehberlik edebilir ve yeni ilaç hedefleri olabilecek daha önce gizli RNA yapıları ortaya çıkarabilir.
Atıf: Miyashita, E., Onizuka, K., Chen, Y. et al. Systematic identification of variant-specific RNA structure-small molecule interactions exemplified by RNA G-quadruplexes. Nat Commun 17, 2243 (2026). https://doi.org/10.1038/s41467-026-70097-9
Anahtar kelimeler: RNA-hedefli ilaçlar, G-kuadrupleks, genetik varyantlar, küçük molekül bağlanması, kanser mutasyonları