Clear Sky Science · tr
Tek molekül dinamiği, yalnızca ATP bağlanmasının bir ABC taşıyıcısı tarafından substrat taşınmasını sağladığını ortaya koyuyor
Neden küçük hücresel pompalar önemli
Vücudunuzdaki her hücre, besin alımından bağışıklık savunmasına kadar birçok süreci belirleyen zarlar boyunca molekülleri taşıyan mikroskobik makinelerden yararlanır. Bu makinelerin önemli bir sınıfı olan ABC taşıyıcıları, hücrenin kimyasal yakıtı ATP’yi kullanarak yükleri doğal eğilimlere karşı yukarı doğru iter. Yine de onlarca yıldır bilim insanları temel bir konuda tartıştı: taşınma adımını yalnızca ATP bağlanmasının mı sağladığı yoksa enerjinin ancak ATP parçalandığında mı açığa çıktığı mı? Bu çalışma, o tartışmayı sona erdirmek için bir taşıyıcıyı molekül molekül inceleyip yakından bakıyor.
Bir seferde tek bir taşıyıcıyı izlemek
Milyonlarca molekülün toplu davranışını ölçmek yerine araştırmacılar, bireysel taşıma olaylarını gerçek zamanlı olarak izlemelerini sağlayan bir düzenek kurdular. Odaklandıkları protein, insan TAP taşıyıcısının bakteriyel bir akrabası olan TmrAB’ydi; bu taşıyıcı, öldürücü T hücrelerine sunulmak üzere bağışıklık peptidlerini yükler. TmrAB zar içinde yer alır ve kısa protein parçalarını (peptidleri) ATP kullanarak bir taraftan diğerine taşır. Her taşıma adımını görebilmek için ekip, tek bir TmrAB molekülünü yapay bir zar baloncuğuna (lipozom) hapsetti ve bu baloncuğun içine bir peptidi yakaladığında floresansını değiştiren özel tasarlanmış bir “sensör” proteini yerleştirdi. Son derece hassas bir mikroskop kullanarak, ışık sinyalindeki ani sıçramalar halinde bir peptidin ardından diğerinin baloncuğa ulaştığı kesin anları görebildiler.
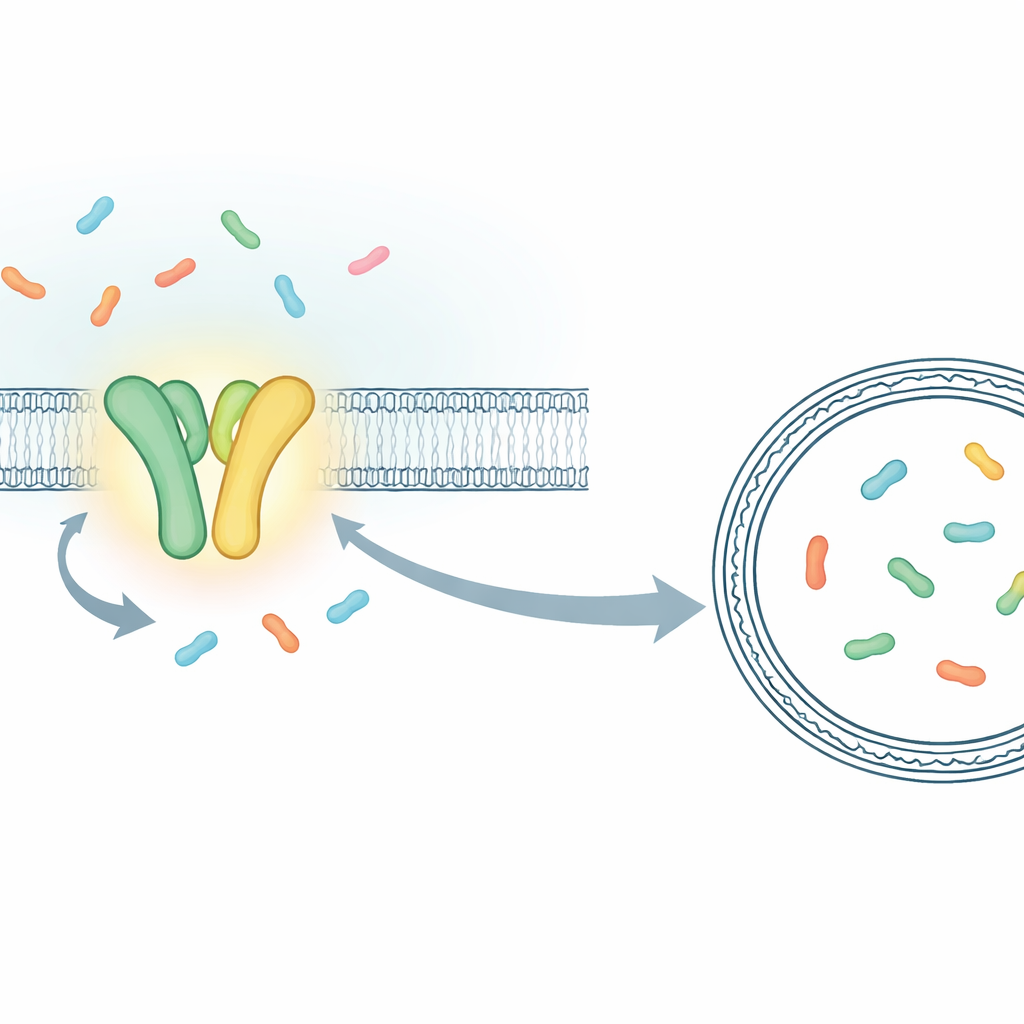
Bir ATP bağlanmasının bir peptidi hareket ettirdiğini kanıtlamak
Bu tek molekül ölçüm yöntemine sahip olarak araştırmacılar, normal TmrAB ile döngüleri zamana yayılmış, yavaş devirli bir versiyonunu karşılaştırdılar. Yavaş varyant, aksi halde birbirine karışacak olayları ayırt etmeyi mümkün kıldı. ATP ve peptidler birlikte bulunduğunda, lipozom içindeki sensörün “boş” durumundan “dolu” durumuna ayrık adımlarla geçtiğini, her birinin bir tek peptidin taşınmasına karşılık geldiğini gösterdiler. Sensörün peptidlere sarılma hızını ve her lipozom içindeki küçük hacmi tahmin ederek bu ışık değişikliklerini yaklaşık peptid konsantrasyonlarına çevirebildiler. Elde edilen sayılar, yaklaşık 100 nanometre çapındaki baloncuklarda önce bir, sonra iki peptidin biriktiğini beklentilere uygun şekilde göstererek taşıma olaylarını tek tek saydıklarını doğruladı.
ATP bağlanması tek başına moleküler anahtarı çevirir
Ana tartışma, hücrelerde ATP’ye genellikle eşlik eden ve ATP parçalanması için gerekli olduğu bilinen magnezyum iyonları (Mg2+) etrafında dönüyor. Bazı modeller Mg2+’nun ATP’nin bağlanması veya taşıyıcının kapanması için de gerekli olabileceğini öne sürmüştü. Bu rollerin ayrımını yapabilmek için araştırmacılar, bir şelatlayıcı kullanarak Mg2+’yı ortamdan uzaklaştırdılar ama yine de ATP verdiler. Bu koşullar altında hem normal hem de yavaş taşıyıcı her molekül başına tam olarak bir peptid taşıma adımı gerçekleştirebildi, sonra durdu. Bu davranış, Mg2+ olmadan da ATP’nin bağlanıp taşıyıcıyı içe bakan konumdan dışa bakan konuma çevirerek bir peptidi hareket ettirebildiğini gösterir. Ancak Mg2+ olmadan taşıyıcı ATP’yi verimli şekilde parçalayamaz ve dolayısıyla kendini bir sonraki tur için yeniden hazırlayamaz.
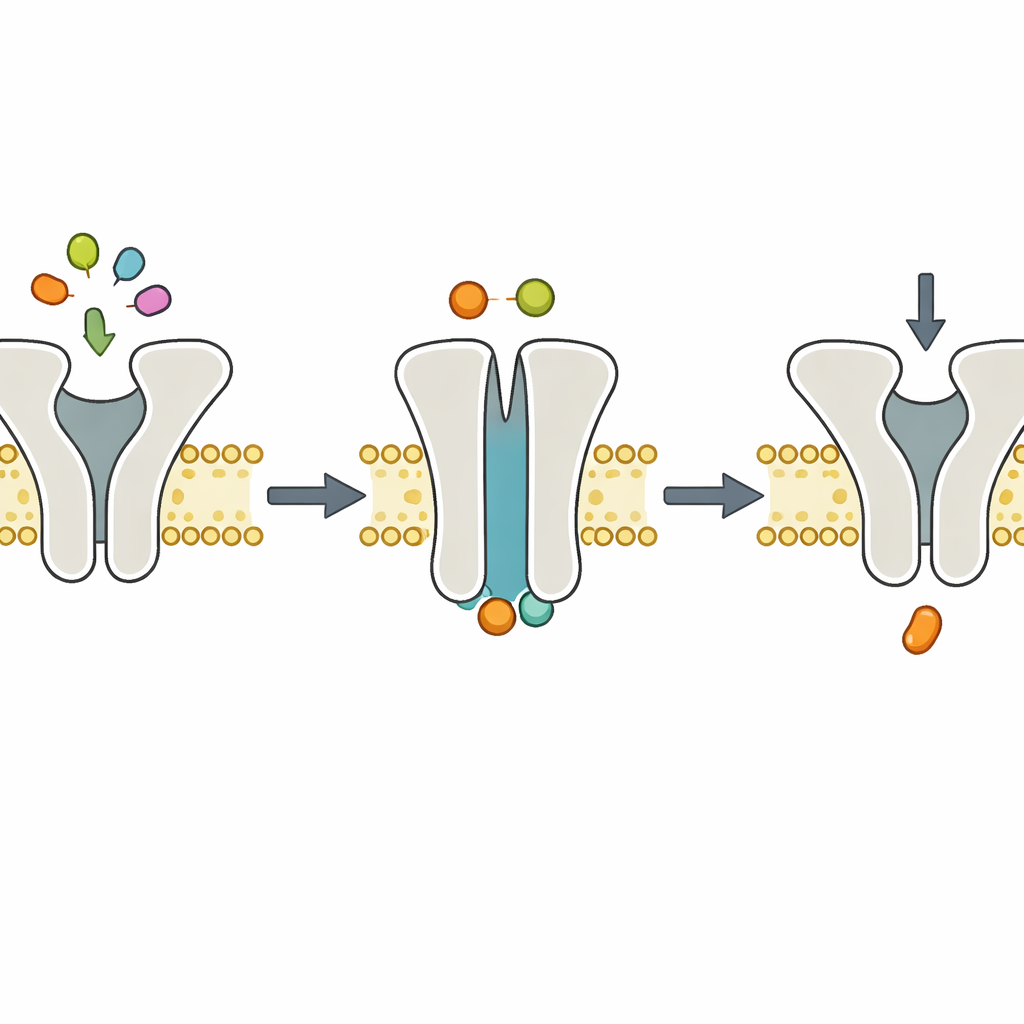
Yapısal anlık görüntüler dinamikleri destekliyor
Bu Mg2+ içermeyen adım sırasında makinenin nasıl göründüğünü görmek için ekip, hızlı dondurulmuş molekülleri yakın-atomik ayrıntıda görüntüleyen kriyo-elektron mikroskopisine başvurdu. TmrAB’yi lipid nanodisklerinde yeniden yapılandırdılar, Mg2+ olmadan ATP eklediler ve kompleksleri dondurdular. Ortaya çıkan yapılar, TmrAB’nin dışa bakan, “tutuklanmış” bir konformasyonunda olduğunu ve her iki iç bağlanma bölümüne sıkışmış ATP’yi gösterdi; ancak görülebilir Mg2+ yoktu. Bu anlık görüntüler, ATP ve Mg2+ birlikteyken elde edilen önceki yapılarla özdeşti. ATP parçalanmasının Mg2+ olmadan tamamen durduğunu gösteren biyokimyasal deneylerle birlikte bu veriler, işbölümünü destekliyor: ATP bağlanması peptidi hareket ettiren konformasyon değişimini sağlarken, Mg2+-bağımlı ATP hidrolizi ise taşıyıcıyı yeniden başlatma görevini üstleniyor.
Hücresel pompaların nasıl çalıştığına dair daha net bir tablo
Tek tek taşıyıcıları izleyip yapılarını çözen bu çalışma, ABC taşıyıcıları hakkında uzun süredir devam eden bir sorunu çözüyor: peptidi hareket ettiren mekanik güç darbesi, ATP’nin kimyasal olarak parçalanması değil, ATP bağlanmasının kendisi tarafından tetiklenir. Mg2+ hikâyeye esas olarak ATP’nin parçalanmasına izin vermek için girer; bu da taşıyıcının tekrar çalışabilir hale gelmesini sağlar. Temel bir hücre biyolojisi unsurunu netleştirmenin ötesinde, bu tek molekül yaklaşımı bağışıklık, ilaç direnci ve birçok hastalığı belirleyen diğer zar makinelerini adım adım incelemek için bir kılavuz sunuyor—bir molekül ve bir taşıma adımıyla.
Atıf: Nocker, C., Pečak, M., Nocker, T. et al. Single-molecule dynamics reveal ATP binding alone powers substrate translocation by an ABC transporter. Nat Commun 17, 3038 (2026). https://doi.org/10.1038/s41467-026-70021-1
Anahtar kelimeler: ABC taşıyıcıları, ATP bağlanması, tek molekül FRET, zar taşınımı, TAP ve TmrAB