Clear Sky Science · tr
Kiral peptidoglikan taklitleri, patojen müdahalesi için bakteri duvarı biyosentezini hedefliyor
Zararlı Mikropları Avlamanın Yeni Bir Yolu
Antibiyotiğe dirençli enfeksiyonlar dünya çapında artarken, doktorların zararlı bakterileri kendi hücrelerimizi zarar vermeden hassas biçimde saptayıp hedef alabilecek araçları hâlâ yetersiz. Bu çalışma, bakteri hücre duvarının temel yapı taşlarından birini taklit eden zekice bir moleküler “yem” sunuyor. Bu tasarım moleküller hem enfeksiyonları görüntülemek için parlak nokta oluşturuyor hem de antibiyotikleri doğrudan mikrobiyalara taşıyarak tedavi edilmesi güç patojenlere karşı yeni bir strateji sağlıyor.
Bakteriyel Zırhı Taklit Etmek
Bakteriler, bizim hücrelerimizin büyük ölçüde kullanmadığı şekerler ve sıra dışı ayna görüntülü aminoasitlerden oluşan, sert bir ağ olan hücre duvarıyla çevrilidir. Araştırmacılar bu farktan yararlanarak belirli ayna görüntüsündeki alaninle süslenmiş uzun şeker bazlı zincirler yarattı. Kiral peptidoglikan taklitleri olarak adlandırılan bu zincirler, bakterilerin duvarlarını inşa etmek için kullandıkları doğal bileşenlere yakın bir benzerlik gösterecek şekilde tasarlanmış, ancak memelilerde bulunmayan yapılardır. Eki olan D-formu alanin miktarını ince ayarlayarak ekip, insan hücreleri yerine bakterileri güçlü şekilde tercih eden versiyonlar üretti.
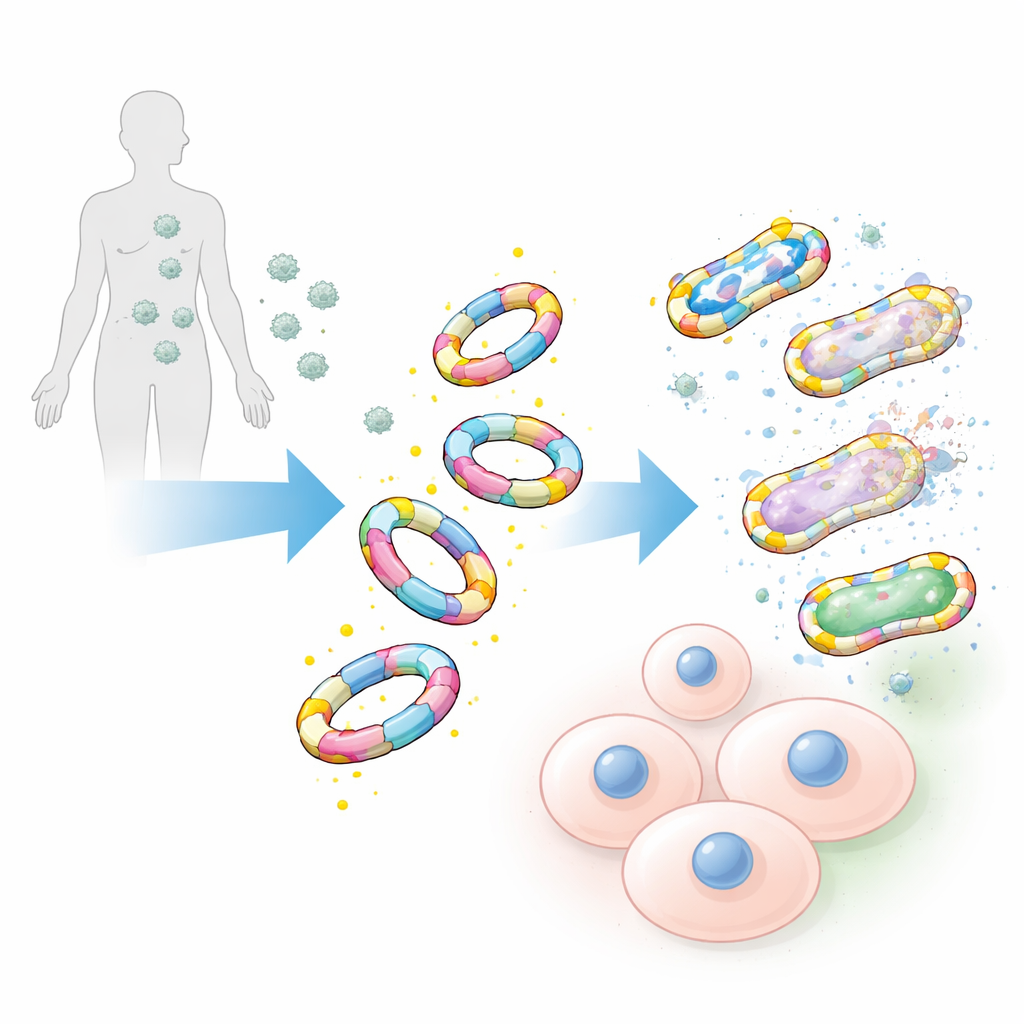
Bakterilere Tutunmak, Bizim Hücrelerimize Değil
Metisiline dirençli Staphylococcus aureus gibi hastane kaynaklı dikkat çekici suşlar ve diğer ESKAPE bakterileri de dahil olmak üzere geniş bir patojen yelpazesinde test edildiğinde, D-alanin ile dekore edilmiş taklitler bakteri yüzeylerine çarpıcı bir verimle bağlandı. L-form alaninden yapılan ayna görüntülü karşıtları ve yalnızca orijinal şeker zincirleri ise zayıf veya göz ardı edilebilir düzeyde bağlanma gösterdi. Ekip ayrıca bu büyük taklitleri tek D-alanin molekülüne dayalı geleneksel küçük kimyasal problarla karşılaştırdı. Küçük problar son derece parlak hâle getirildiğinde bile çok daha az bakteri etiketledi ve daha zayıf sinyaller verdi; bu da daha büyük, daha canlı tasarımın gücünü vurguluyor.
Hücre Duvarı Montaj Hattını Ele Geçirmek
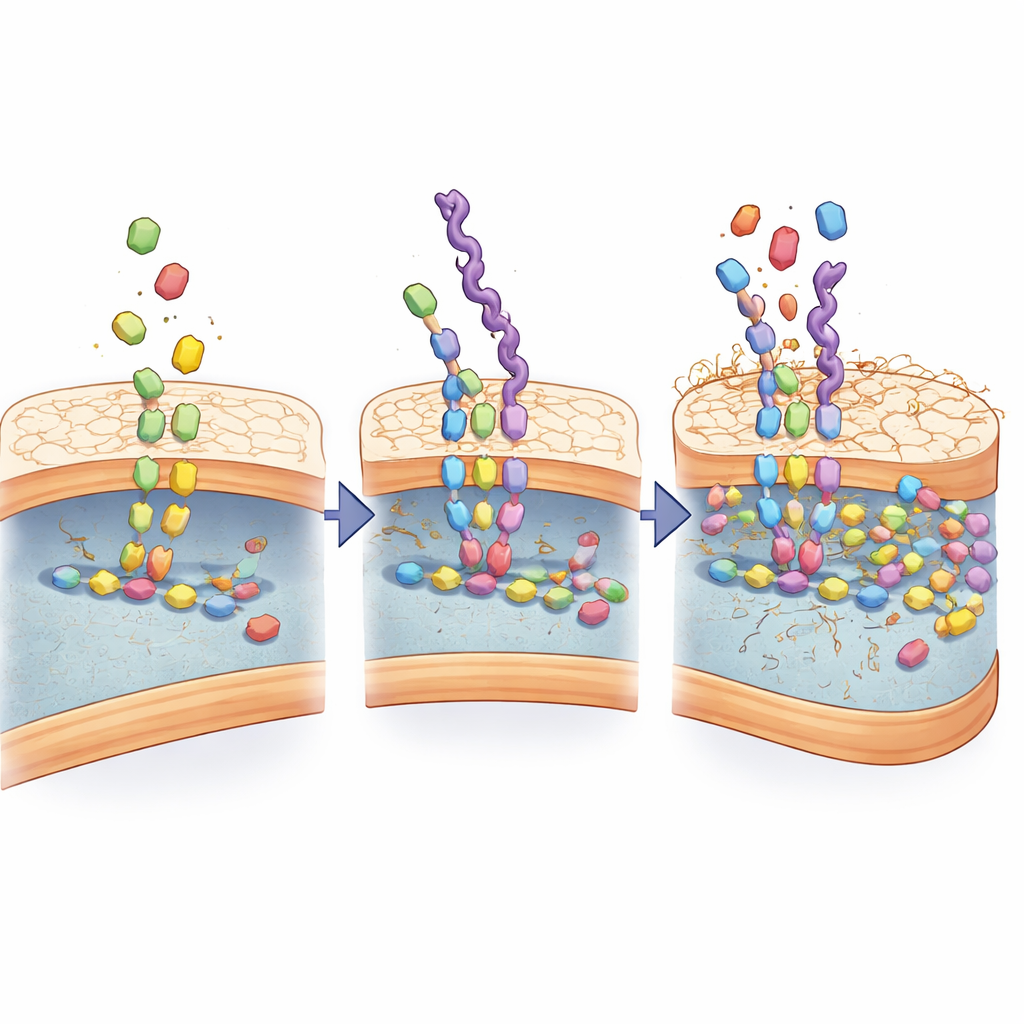
Tanınmanın nasıl bu kadar güçlü hâle geldiğini anlamak için bilim insanları taklitlerin bakteriyel duvar yapım makineyle nasıl etkileştiğini inceledi. D-alanin bazlı zincirlerin sadece dışarıya yapışmadığı, gerçek yapı taşlarıymış gibi alındıkları ve normalde hücre duvarı bileşenlerini birleştiren aynı enzimatik adımlara verildiği bulundu. Kimyasal analiz, bu taklitlerin varlığında yalnızca ortaya çıkan yeni ara molekülleri saptadı ve bilgisayar simülasyonları ana duvar yapım enzimlerinin taklitleri doğal substratlardan daha sıkı tutabildiğini gösterdi. Birkaç bakteri üreme turu boyunca taklitler duvarda birikerek yapısını yavaşça bozdu ve geçirgen hâle getirdi.
Taklitleri Akıllı İlaç Taşıyıcılarına Dönüştürmek
Bu zincirler suda doğal olarak küçük partiküller halinde toplanıp birçok kimyasal bağlantı noktası taşıdıkları için ekip bunları görüntüleme boyaları ve antibiyotikler için iskelet olarak kullandı. Floresan versiyonları hücre kültürlerinde bakterileri net bir şekilde işaretlerken, birlikte yetiştirilen memeli hücreleriyle neredeyse etkileşime girmedi. Araştırmacılar daha sonra antibiyotik tetrasiklini taklit bazlı partiküllere yükledi. Laboratuvar testlerinde bu paketleme tetrasiklinin etkinliğini birkaç kat artırdı; serbest ilaca göre çok daha düşük dozlarda bile dirençli suşları öldürdü. Mikroskopi, antibiyotik yüklü taklitlerin bakterilerin üzerine yığıldığını, zarlarını delip geçtiğini ve hedeflenmemiş formülasyonlara kıyasla yaygın hücre ölümünü tetiklediğini ortaya koydu.
Vücut İçindeki Enfeksiyonlarla Mücadele
En zorlu testler, lokalize deri yaraları ve hayati tehlike arz eden karın içi enfeksiyonlarının fare modellerinde yapıldı. Enfekte yaralarda, floresan taklitler derin dokudaki bakterilere yöneldi ve tetrasiklin taşıdıklarında mikropları neredeyse tamamen temizledi. Bu, daha hızlı iyileşme, daha kalın yeni deri, daha düzenli kolajen birikimi ve daha zengin küçük damar büyümesi ile sonuçlandı. Sistemik enfeksiyon modellerinde taklitler dalak ve akciğer gibi enfekte organlarda seçici olarak birikti ve antibiyotik yüklendiğinde bakteri sayısını keskin biçimde azalttı. Önemli olarak, yalnızca taklitlerin yüksek dozları iyi bir güvenlik profosu gösterdi; başlıca organlarda veya kan kimyasında belirgin bir hasar gözlenmedi.
Gelecekteki Tedaviler İçin Anlamı Ne Olabilir
Bakteriyel hücre duvarının kendi bileşenlerinin yakın bir kimyasal benzerini inşa ederek, bu çalışma bir patojenin metabolizmasına dışarıdan yalnızca saldırmak yerine “karışmanın” yeni bir yolunu gösteriyor. Bu kiral taklitler, hem görüntüleme için yüksek hassasiyetli işaretleyiciler hem de antibiyotikleri dirençli suşlar da dahil olmak üzere mikrobiyal hedeflerine doğrudan yönlendiren akıllı taşıyıcılar olarak hizmet ediyor ve memeli hücreleri koruyor. Klinik araçlara çevrildiğinde, bu tür biyomimetik platformlar doktorların enfeksiyonların tam olarak nerede saklandığını görmesine yardımcı olabilir ve daha düşük ilaç dozlarıyla daha etkili tedaviler sağlayarak artan antimikrobiyal direnç zorluğuna karşı umut vadeden bir silah sunabilir.
Atıf: Deng, K., Zou, D., Zeng, Z. et al. Chiral peptidoglycan mimics target bacterial wall biosynthesis for pathogen intervention. Nat Commun 17, 3258 (2026). https://doi.org/10.1038/s41467-026-69967-z
Anahtar kelimeler: antibiyotik direnci, bakteriyel hücre duvarı, hedefe yönelik ilaç taşıma, moleküler görüntüleme, nanotıp