Clear Sky Science · tr
Hareket korteksinde hücre tipi özgü TDP-43 patolojisinin çok-modlu çözümü
Bu araştırma insanların yaşamı için neden önemli
Amyotrofik lateral skleroz (ALS) ve frontotemporal demans (FTD), insanlardan hareket, konuşma ve kişilik gibi yetileri çalan yıkıcı beyin hastalıklarıdır. ALS’li çoğu hasta ve birçok FTD hastasında ortak mikroskobik bir özellik vardır: TDP-43 adındaki bir proteinin olması gereken yerin dışında birikmesi. Bu çalışma gelecekteki tedaviler için önemli iki pratik soruyu yanıtlamayı amaçlıyor: TDP-43 sorunlarından en çok hangi beyin hücreleri etkileniyor ve bu hücrelerin içinde DNA düzenlemesi ve gen etkinliği düzeyinde neler bozuluyor?
Hasarı beynin hareket merkezinde izlemek
Araştırmacılar, istemli hareketi kontrol eden beyin dokusu şeridi olan primer motor kortekse odaklandı. ALS, ALS-FTD ve nörolojik olarak sağlıklı kontrollerden bağışlanan post-mortem beyin örneklerini kullanarak tek tek hücre çekirdeklerini izole ettiler ve hem hangi genlerin aktif olduğunu hem de yerel DNA’nın ne kadar sıkı paketlendiğini okudular. 180.000’in üzerinde çekirdeğe uygulanan bu “multi-omik” yaklaşım, hücreleri birkaç sınıf eksitatör ve inhibitör nöron ile astroglia, oligodendrosit ve mikroglia gibi destek hücreleri dahil olmak üzere kesin türlere ayırmalarını sağladı. Ardından bunu başka bir insan beyin veri setinden alınan mekansal gen haritalarıyla birleştirerek bu hücre tiplerini korteksin tanıdık katmanlı yapısına yerleştirdiler.
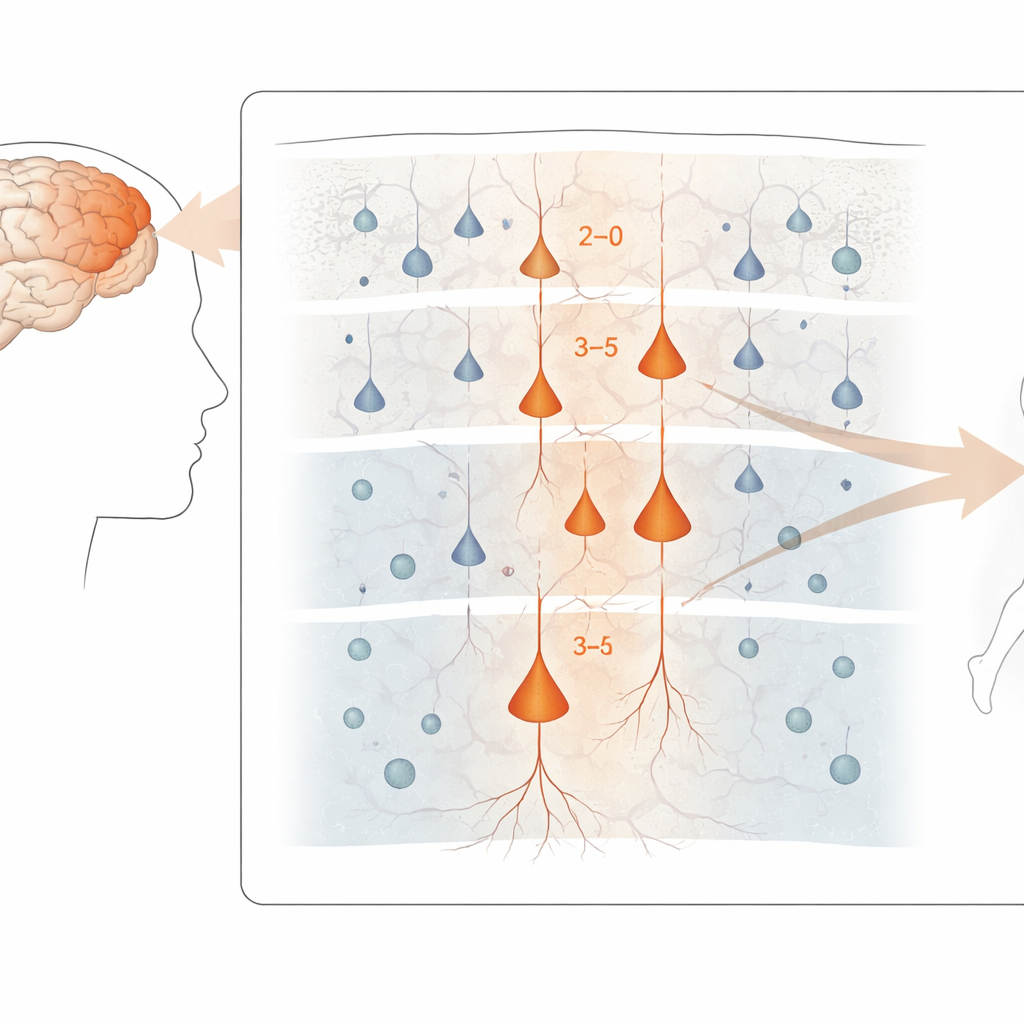
En savunmasız nöronları kesinleştirmek
Motor korteks genelinde hastalıkla ilişkili en güçlü gen değişiklikleri, beyin devreleri boyunca aktiviteyi ileri taşıyan hücreler olan eksitatör nöronlarda ortaya çıktı. Özellikle korteks içinde bağlantı kuran üst ve orta katman nöronları ile korteksten dışa sinyal gönderen belirli derin katman hücreleri—omurilik motor nöronlarını kontrol eden büyük “Betz” hücreleri dahil—en belirgin değişiklikleri gösterdi. Buna karşılık, inhibitör interneuronlar ve birçok glial hücre gen ifade düzeyinde daha az etkilendi; bazıları daha hafif kaymalar sergilemiş olsa da. Bu moleküler kargaşaya rağmen, dokudaki ana hücre tiplerinin genel karışımı hastalar ve kontroller arasında şaşırtıcı derecede benzerdi; bu durum hasarın daha çok hücre sayısının kaybından ziyade hücrelerin işlevindeki değişikliklerle ilgili olduğunu düşündürüyor.
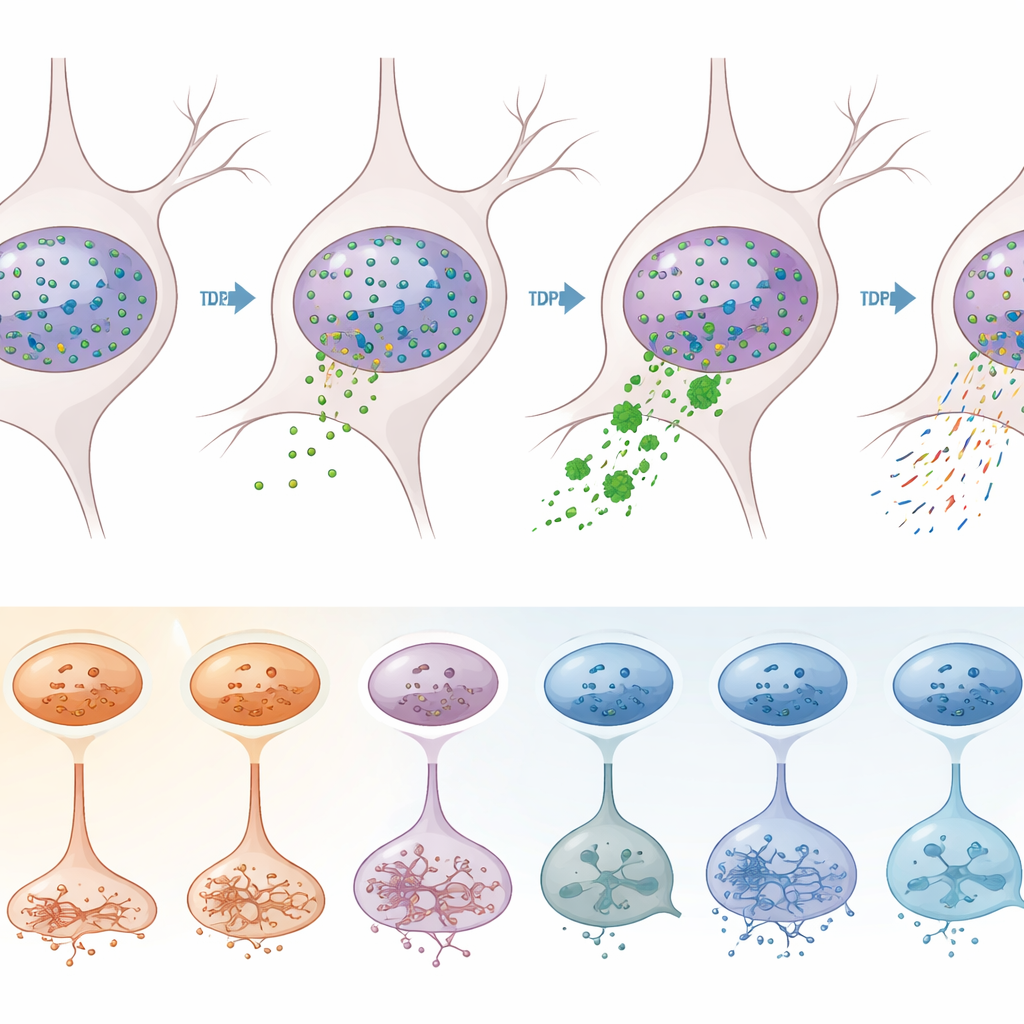
TDP-43’ün gen etkinliğini içeriden nasıl yeniden şekillendirdiği
TDP-43 kaynaklı doğrudan etkileri diğer hastalık süreçlerinden ayırmak için ekip zekice bir ayırma stratejisi kullandı. Çekirdekleri TDP-43 ve bir nöronal belirteç karşıtı antikorlarla işaretlediler, ardından akış sitometrisiyle çekirdeğinde TDP-43 kaybı olan (patoloji işareti) nöronları bunu koruyanlardan ayırdılar. Bu çekirdeklerden 12.000’den fazlasının dizilenmesi, TDP-43 kaybının ezici çoğunlukla eksitatör nöronlarda, özellikle 2–3, 3–5, 5 ve 6. katmanlardaki belirli alt tiplerde gerçekleştiğini ortaya koydu. Bu savunmasız nöronlarda yüzlerce gen yanlış düzenlenmişti; bunların birçoğu zaten ALS ile ilişkilendirilmişti. STMN2 ve KALRN gen transkriptlerinde “kriptik” ekstra parçaların ortaya çıkması ve RNA moleküllerinin uçlarının kesilip kuyruklanma yerlerindeki kaymalar gibi TDP-43 bozukluğunun klasik moleküler imzaları, TDP-43 eksikliği olan çekirdeklerde belirgin biçimde zenginleşmişti.
Epigenetik yeniden düzenleme: tüm değişiklikler TDP-43 kaynaklı değil
Aynı çekirdeklerde hem gen etkinliğini hem de kromatin açıklığını ölçebildikleri için yazarlar hangi değişikliklerin DNA paketlenmesindeki kaymalarla ilişkili olduğunu sorgulayabildi. Genomda yerel kromatin erişilebilirliğinin gen ifadesiyle paralel hareket ettiği on binlerce bölge buldular. ALS ve ALS-FTD’de değişen birçok gen bu tür bölgelerde yer alıyordu; bu da hastalık imzasının bir kısmının TDP-43 kaybının doğrudan etkisinden ziyade daha geniş epigenetik yeniden düzenlemeyi yansıttığını gösteriyor. İlginç biçimde, kromatinla bağlantılı bu değişiklikler sıklıkla hücre iletişimi ve akson yönlendirme ile ilgili sinyal yollarında birleşiyor ve özellikle belirli eksitatör nöronlarda ile oligodendrositlerde güçlüydü. Ekip, TDP-43 patolojisine bağlı gen değişiklikleri ile kromatin kaymalarına bağlı değişiklikleri karşılaştırdığında, bunların kısmen örtüştüğünü ama büyük ölçüde ayrı bozulma katmanları oluşturduğunu gördü.
Gelecekteki terapiler için anlamı
Hekim olmayan bir okuyucu için ana mesaj şudur: ALS ve ALS-FTD motor korteksi uniform bir şekilde yıpratmıyor. Bunun yerine belirli eksitatör nöron tiplerini ve daha az ölçüde bazı destek hücrelerini hedef alıyor; bu hücrelerin gen programlarını hem TDP-43’ün bozulmasından hem de DNA’nın paketlenme ve okunma biçimindeki daha geniş değişikliklerden kaynaklanan şekillerde değiştiriyor. Bu bulgular, etkili tedavilerin hücre tipi ve yolaklara özgü olmasının gerekebileceğini öne sürüyor—örneğin, en savunmasız nöronlarda TDP-43 işlevini yeniden sağlamak veya onunsplicing hatalarını düzeltmek ile epigenetik ve sinyal değişikliklerini ayrı biçimde hedeflemek gibi. Bu karmaşık manzarayı yüksek ayrıntıda haritalandırarak çalışma, ALS ve ALS-FTD’de hareket kontrolünün kaybını yavaşlatmaya veya önlemeye yönelik daha hassas müdahalelerin tasarlanması için bir yol haritası sunuyor.
Atıf: Ruf, W.P., Kühlwein, J.K., Meier, L. et al. Multi-modal dissection of cell-type specific TDP-43 pathology in the motor cortex. Nat Commun 17, 2406 (2026). https://doi.org/10.1038/s41467-026-69944-6
Anahtar kelimeler: ALS, frontotemporal demans, TDP-43, motor korteks nöronları, tek-nükleus multiomik