Clear Sky Science · tr
Eukaryotik başlatma faktörü 6, integrin-FAK sinyal ekseni yoluyla küçük hücreli akciğer karsinomunun plastisitesini modüle eder
Bu akciğer kanseri araştırmasının önemi
Küçük hücreli akciğer karsinomu (SCLC), akciğer kanserlerinin en ölümcül biçimlerinden biridir. İlk başta kemoterapiye genellikle iyi yanıt verir, ancak neredeyse her zaman, hızlı ve agresif biçimde geri döner. Bu çalışma temel bir soruyu ele alıyor: SCLC hücrelerinin “kişilik değiştirmesine” ve ilaç dirençli hale gelmesine ne oluyor ve bu şekil değiştirme yavaşlatılabilir veya engellenebilir mi?
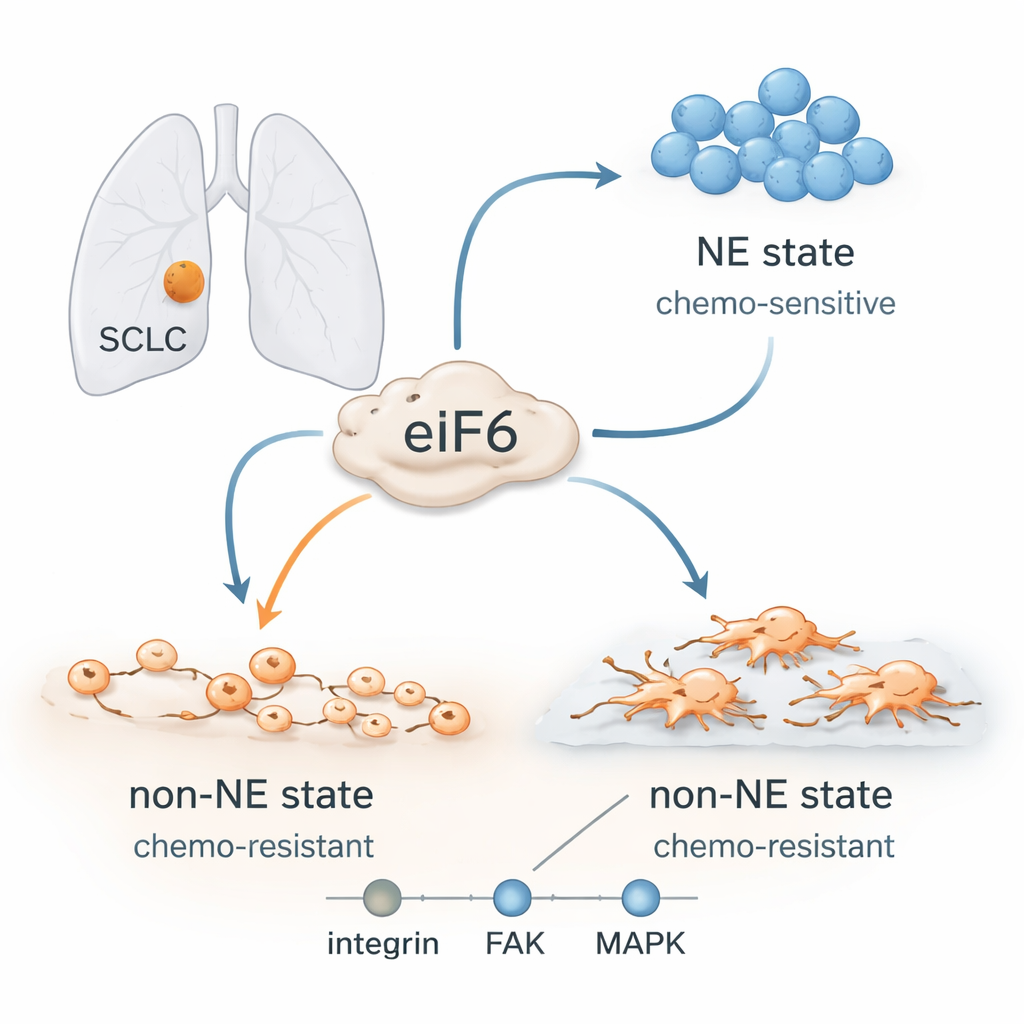
Şekil değiştiren kanser hücreleri
Doktorlar daha önce SCLC’nin tek tip bir hastalık olduğunu düşünüyordu, ancak artık bu tümörlerin farklı hücre tipleri içerdiği açık. Bazı hücreler güçlü bir “nöroendokrin” kimliğe sahiptir: sık, yüzen kümeler halinde büyürler, platin bazlı kemoterapiye iyi yanıt verirler ve belirli sinir-benzeri proteinlerce zengindirler. Diğerleri bu kimliği kaybeder ve “nöroendokrin olmayan” bir durumu benimser: etrafa yayılır, çevre dokulara tutunur, daha hareketli, invaziv hücre özellikleri gösterir ve ilaçlarla öldürülmesi çok daha zordur. Hastaların tümörleri genellikle tedavi sırasında veya sonrasında hassas durumdan dirençli duruma evrilir; DNA’larında büyük değişiklikler olmaması, nüksün itici gücünün yeni mutasyonlardan ziyade esnek hücresel programlar olduğunu gösterir.
Çift görevli bir çeviri faktörü
Yazarlar, ribozomların, yani hücrenin protein fabrikalarının montajına yardımcı olmasıyla tanınan eIF6 adlı bir proteine odaklandı. Hasta örnekleri, fare modelleri ve birkaç insan SCLC hücre hattı üzerinde çalışarak, hücreler ilaç dirençli, nöroendokrin olmayan duruma geçtiğinde eIF6 seviyelerinin tutarlı şekilde arttığını buldular. Şaşırtıcı şekilde, bu artış toplu protein üretiminde genel bir düşüşle eşlik etti; bu da eIF6’nın ders kitaplarındaki işinden daha fazlasını yapıyor olabileceğini ima etti. Haberci RNA’ların ribozomlara bağlanma biçimlerinin ayrıntılı analizleri, temel ribozom parçalarının çok değişmediğini gösterdi. Bunun yerine, mesajların çeviri için seçilme ve işlenme yolları, hücreler kimlik değiştirirken yeniden düzenlendi.
Kopup hayatta kalma sinyallerine bağlanma
Daha derine indiklerinde ekip, dirençli hücrelerde eIF6’nın kısmen ribozomlardan ayrılıp integrinler ve fokal adezyon kinaz (FAK) adlı bir protein etrafında kurulmuş yüzey sinyal merkezleriyle ilişkilendiğini keşfetti. İntegrinler hücrelerin çevresini hissetmesine ve ona tutunmasına yardımcı olur; FAK bu sinyalleri içeri aktarır ve sıklıkla hareket, hayatta kalma ve ilaç toleransını destekleyen yolakları tetikler. Biyokimyasal çekme deneyleri ve hücre içi yakınlık testleri, eIF6’nın integrin ortağı CD104 ve FAK ile fiziki etkileşimde olduğunu ve bu komplekslerin nöroendokrin olmayan hücrelerde daha bol bulunduğunu gösterdi. Bu eIF6–integrin–FAK düzenekleri ise MAPK sinyal yolunda aktiviteyi artırdı; bu yol büyüme ve stres direncinin bilinen bir sürücüsüdür.
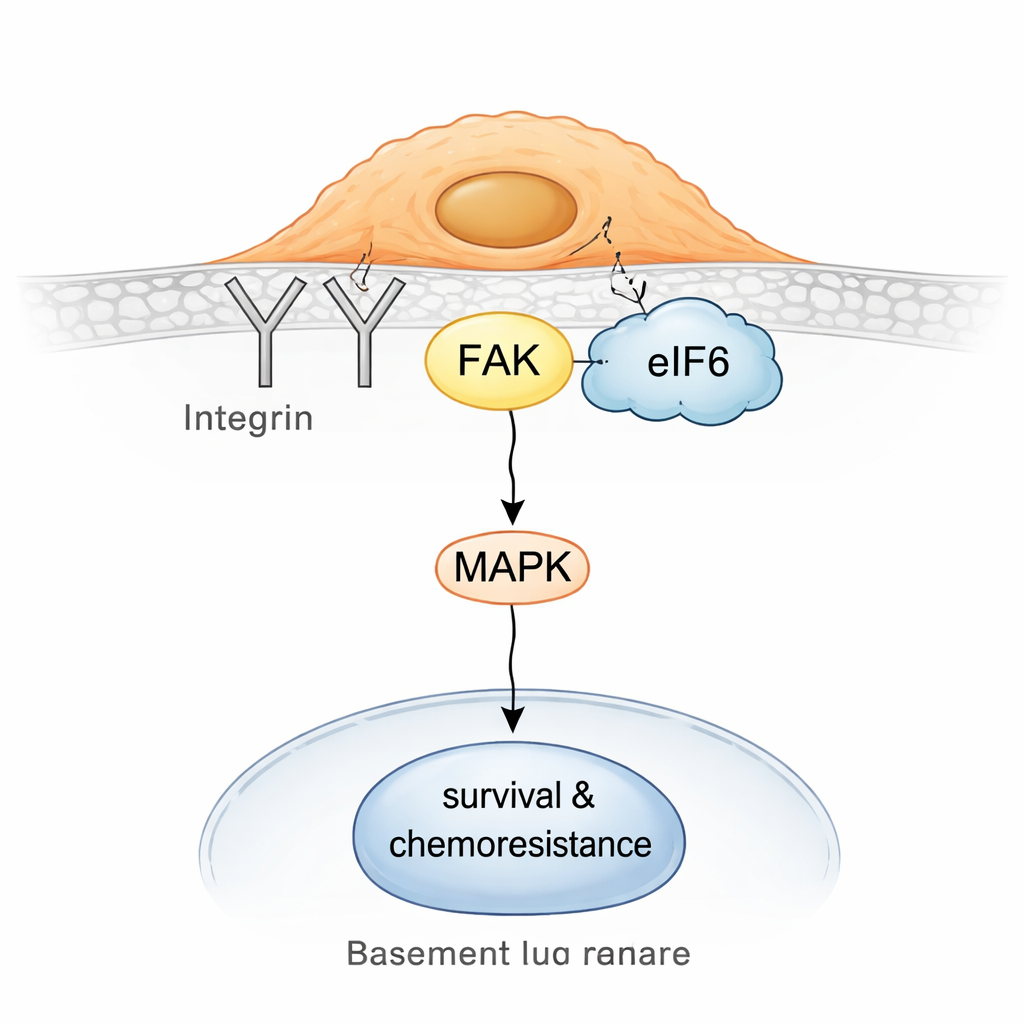
Dirençli tümörleri yeniden savunmasız hale getirmek
Araştırmacılar daha sonra eIF6’yı manipüle etmenin SCLC davranışını değiştirip değiştiremeyeceğini sordular. Dirençli hücrelerde eIF6 düzeylerini azalttıklarında, hareketli, yara izi oluşturan (epitel–mezenkimal) programla ilişkili genlerin aşağı regüle olduğu, klasik nöroendokrin genlerin ise kısmen geri getirildiği görüldü. Bu değişiklikler saati tamamen geriye döndürmedi ama dirençli duruma geçişi yavaşlattı. Kritik olarak, daha az eIF6 taşıyan hücreler kültürde ve fare tümörlerinde standart karboplatin–etoposid kemoterapisine karşı daha duyarlı hale geldi; daha az sağ kalan koloni ve daha kalıcı küçülme görüldü. eIF6’nın kendisi için henüz spesifik ilaçlar bulunmadığından ekip, klinik geliştirme aşamasında olan FAK inhibitörlerini test etti. FAK sinyalini bloke etmek dirençli hücreleri yeniden kemoterapiye duyarlı hale getirdi ve farelerde kombinasyon tedavisi en güçlü tümör kontrolünü sağladı.
Laboratuvar bulgusundan gelecekteki hasta araçlarına
Son olarak yazarlar, ameliyat olmuş sınırlı evre SCLC’li hastalardan alınmış tümör örneklerini incelediler. Proteinlerin yalnızca birbirine yakın olduklarında ışık veren hassas bir boyama yöntemi kullanarak, eIF6’nın tümör hücreleri içinde ne sıklıkla CD104 veya FAK ile kompleks oluşturduğunu ölçtüler. Bu komplekslerin yüksek düzeyleri—tek başına eIF6’dan daha fazla—daha erken nüks ve daha kısa sağkalımla ilişkiliydi ve bu nedenle umut verici prognostik belirteçler olarak öne çıkıyor. Bir arada ele alındığında bu çalışma, eIF6’nın ribozomlardan “ikincil iş” yapar gibi ayrılarak kanser hücrelerini güçlü hayatta kalma devrelerine bağlamaya yardımcı olabileceğini ortaya koyuyor. eIF6–integrin–FAK eksenini haritalandırarak, çalışmanın nüks riski yüksek hastaları tanımlamaya ve SCLC’nin tehlikeli plastisitesine karşı FAK inhibitörlerini kemoterapi ile birleştirmeyi desteklemeye yönelik yollar önerdi.
Atıf: Peng, H., Wang, Z., Wang, M. et al. Eukaryote initiation factor 6 modulates small-cell lung carcinoma plasticity via the integrin-FAK signaling axis. Nat Commun 17, 2048 (2026). https://doi.org/10.1038/s41467-026-69899-8
Anahtar kelimeler: küçük hücreli akciğer kanseri, ilaç direnci, hücre plastisitesi, eIF6, integrin FAK sinyalizasyonu