Clear Sky Science · tr
Bağlama-bağımlı çeviri inhibisyonu: kanser için terapötik bir yaklaşım
Protein Fabrikalarını Kansere Karşı Çevirmek
Kanser hücreleri, büyümeyi ve bölünmeyi sürdüren kısa ömürlü “sürücü” proteinleri sürekli olarak yüksek miktarlarda üreterek hayatta kalır. Bu çalışma, hücrenin protein üreten makineleri olan ribozomları, özellikle MYC gibi ilaçlanması zor onkogenlerde bulunan belirli protein dizilerini oluştururken hafifçe tıkayarak kansere karşı yeni bir mücadele yolu araştırıyor. Bu seçici müdahale, tümör hücrelerini öldürürken normal protein üretiminin büyük bölümünü koruyabilir.
Hücreler Proteini Nasıl Üretir—ve Nerede İşler Yanlış Gidebilir
Her hücre, genetik mesajları (mRNA’ları) okuyan ve amino asitleri bir araya getirerek protein yapan küçük moleküler fabrikalar olan ribozomlara bağımlıdır. Antibiyotikler veya eski tip kanser ilaçları gibi ribozomları hedef alan mevcut ilaçların çoğu kaba aletler gibidir: protein sentezini geniş ölçüde kapatırlar, bu da sağlıklı hücrelere zarar verebilir ve ciddi yan etkilere yol açabilir. Yazarlar, her yeni sentezlenen protein zincirinin kendine özgü dizisi ve kimyasal karakteri olduğu için, makinede belirli bir dizi bulunduğunda yalnızca o durumda ribozomu engelleyecek küçük moleküller tasarlamanın mümkün olabileceğini düşündüler; böylece hücrenin geri kalan protein üretimi büyük ölçüde korunabilir.
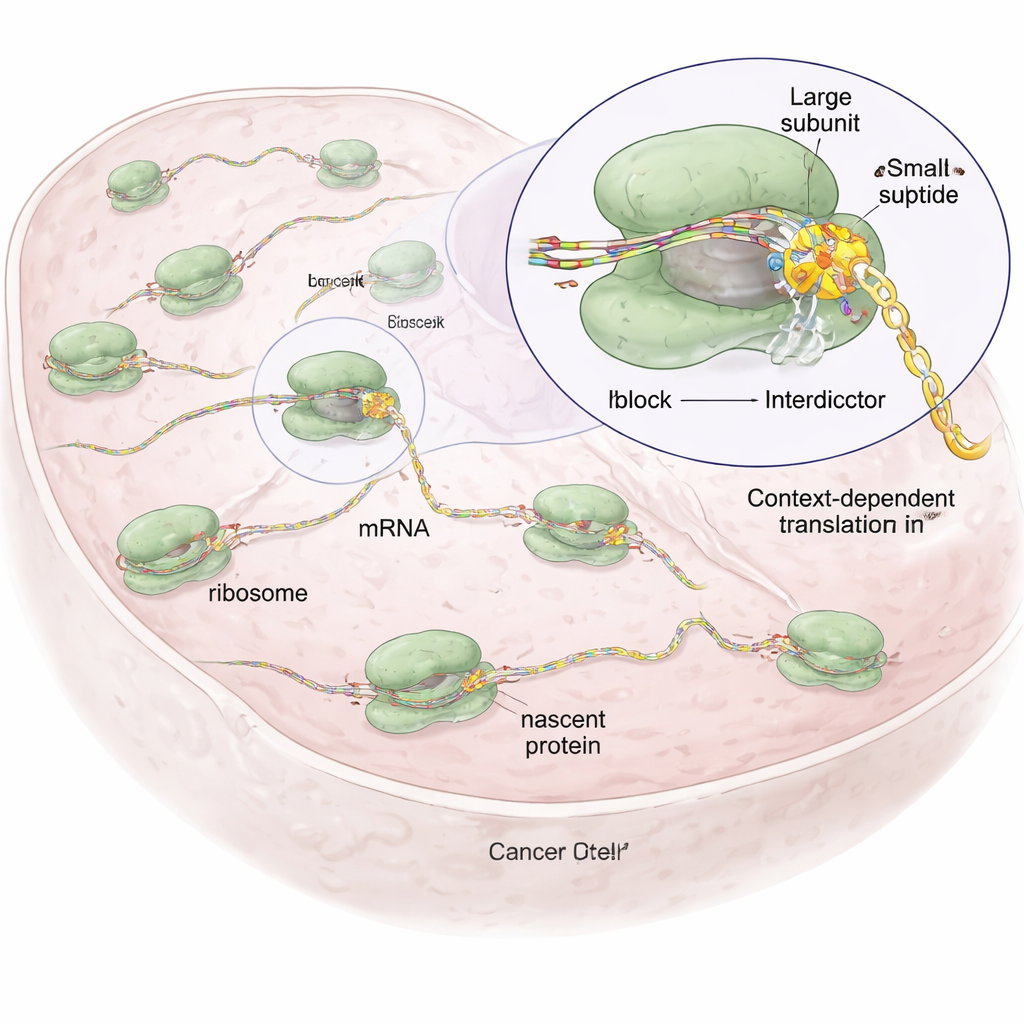
Sadece Belirli Protein Dizilerini Durduran Tasarım Moleküller
Peptid bağlarının oluştuğu ribozomun katalitik merkezine bağlanan doğal bir bileşik olan anisomisin üzerine inşa ederek, araştırmacılar “interdiktörler” adını verdikleri sentetik molekül ailesini geliştirdiler. Hepsi ribozom içinde onları sabitleyen bir çekirdek iskelete sahip, ancak büyüyen protein zincirine doğru bakan yan grupları farklılık gösteriyor. Bu yan gruplar belirli amino asit türlerini tercih edecek şekilde ayarlanmış: örneğin bir interdiktör (IDB‑001) negatif yüklü kalıntılara çekilirken, başka bir (IDB‑002) küçük, yağlı (hidrofobik) kalıntıları tercih ediyor. Hücre içindeki mRNA’larda ribozomların nerede durakladığını küresel olarak haritalayan ribozom profilleme tekniğini kullanarak, ekip her bileşiğin yeni zincirdeki belirli kısa motiflerde duraklamalara neden olduğunu, sıklıkla sondan bir önceki (−1) amino asitte bunun görüldüğünü gösterdi; bu da gelişigüzel bir kapatma yerine dizi‑bağımlı bir etkiyi kanıtlıyor.
İlaç ve Ribozomun Atom Atom Buluşmasını İzlemek
Bu seçiciliğin fiziksel ayrıntısını görmek için yazarlar, insan ribozomlarını tasarlanmış peptid dizilerini çevirirken dondurdular ve kriyogenik elektron mikroskobu ile neredeyse atomik çözünürlükte görüntülediler. Interdiktörün ribozomun aktif bölgesinde yeni zincirin son birkaç amino asidiyle hassas temaslar kurmuş halde yerleştiğini gözlemlediler. Bir yapıda, IDB‑002’nin hidrofobik yan grubu, peptiddeki küçük, hacimsiz olmayan kalıntılar tarafından kavranmıştı; bu durum oradaki daha büyük yan zincirlerin neden tercih edilmediğini açıklıyor. Başka bir yapıda ise MYC kaynaklı bir kalıntının asidik yan zinciri, IDB‑001’in pozitif yüklü grubuyla bir tuz köprüsü oluşturacak şekilde yöneliyor. İlacın varlığı ayrıca yakınlardaki ribozomal RNA bazlarını yeni konumlara iterek aktif siteyi daraltıyor ve bir sonraki tRNA’nın girişini kısmen engelliyor; bu da uzama evresinin bu tercih edilen dizilerde donmasına yardımcı oluyor.
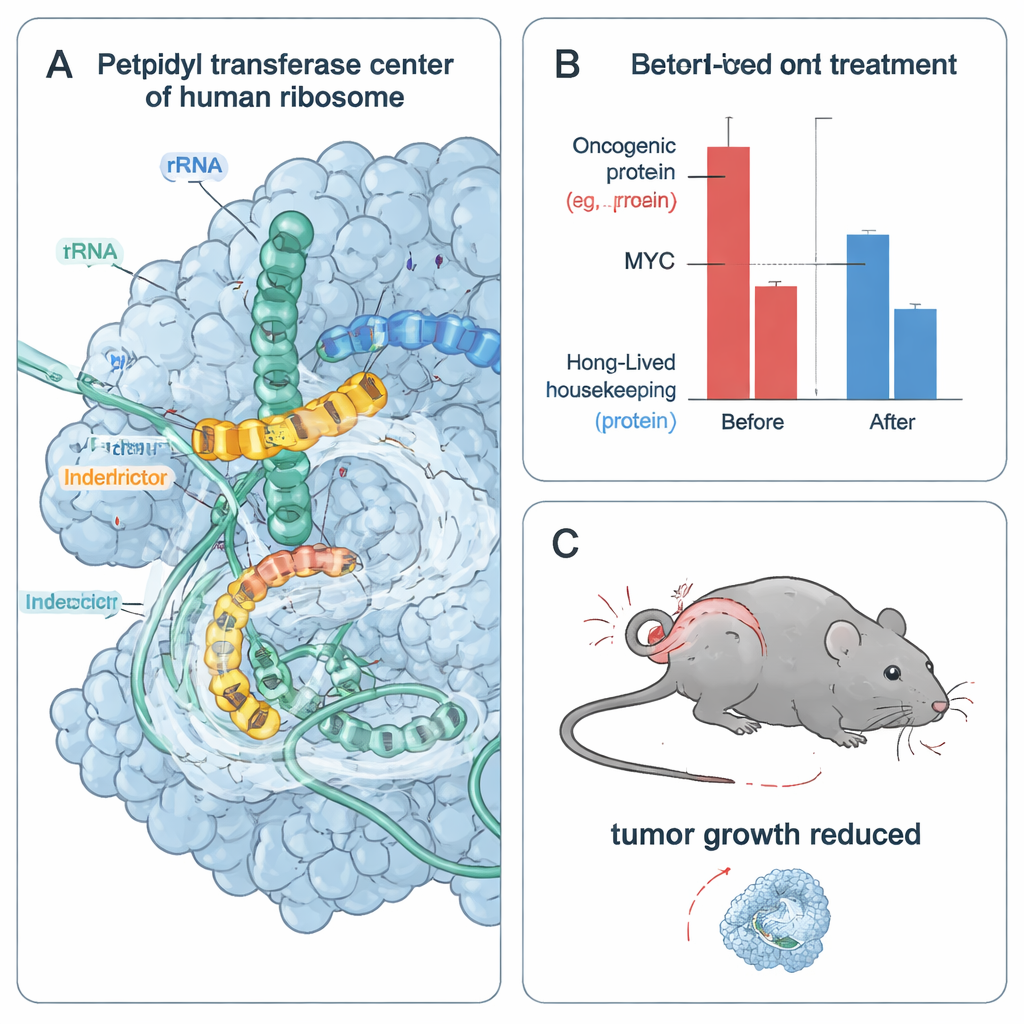
Duraklamış Ribozomlardan Stresli ve Ölen Tümör Hücrelerine
Hızla bölünen kanser hücreleri MYC ve CCND1 gibi kısa ömürlü onko‑proteinlere güçlü biçimde bağımlı olduğundan ekip, interdiktörlerin tümör hücresi canlılığı üzerindeki etkilerini test etti. Birden fazla MYC‑bağımlı kanser hücresi hattında IDB‑001 ve IDB‑002 nanomolardan düşük mikromolar konsantrasyonlara kadar hücre canlılığını azalttı. Daha da optimize edilmiş bir analog olan IDB‑003 daha güçlüydü ve oral uygulama için uygundu. Hücrelerde bu bileşikler MYC ve diğer hızlı parçalanan onkoproteinleri hızla tüketirken, aynı zaman aralığında daha uzun ömürlü ev işi (housekeeping) proteinlerini göreli olarak kararlı bıraktı. İlaçlar ayrıca çarpışmış ribozomlarla ilişkili hücresel stres yanıtlarını tetikledi, ancak bu stres sinyalleme yollarının bloke edilmesi canlılık kaybını ortadan kaldırmadı; bu da temel onko‑proteinlerin doğrudan yoksun bırakılmasının tümör hücresi ölümünde ana sürükleyici olduğunu düşündürüyor.
Zor Bir Meme Kanseri Modelinde Kavram Kanıtı
Bu yaklaşımın hayvanlarda işe yarayıp yaramadığını test etmek için yazarlar, insan triple‑negatif meme kanseri tümörleri taşıyan farelere oral yolla IDB‑003 verdiler. 28 gün boyunca tedavi edilen tümörler kontrol hayvanlardaki tümörlere göre çok daha yavaş büyüdü; yüksek dozlarda %80’e varan tümör büyümesi inhibisyonu gözlendi ve bu çalışmada ciddi toksisite bildirilmedi. Tümörlerin gen ifadesi analizi, in vivo azalmış MYC aktivitesiyle tutarlı şekilde MYC hedef gen programlarının güçlü şekilde aşağı regülasyonunu gösterdi. Birlikte ele alındığında, bu sonuçlar belirli protein dizilerinde ribozomları seçici olarak duraklatmanın, kararsız onko‑sürücülere bağımlı tümörleri zayıflatabileceğini ve klasik çeviri blokerlerinin geniş toksisitesinden potansiyel olarak kaçınabileceğini gösteriyor.
Geleceğin Kanser Tedavileri İçin Neden Önemli
Bu çalışma tamamlanmış bir proteine bağlanmak yerine, proteinin yapımı sırasında ve yalnızca kısa bir “adres etiketi” dizisi mevcut olduğunda onu kesintiye uğratan yeni bir küçük molekül ilaç türünü tanıtıyor. Birçok kanser‑teşvik edici protein gevşek yapılı, kısa ömürlü veya geleneksel ilaçların hedef alacağı belirgin ceplere sahip olmadığı için, sentezlerini doğrudan ribozomda hedeflemek, MYC gibi şu anda “ilaçlanamaz” olarak kabul edilen genlerin yol açtığı tümörleri tedavi etme yolunu açabilir. Çalışma ayrıca interdiktörlerin kimyasını ayarlayarak gelecekteki ilaçların farklı dizi motifleri ve hastalık hedeflerine odaklanacak şekilde tasarlanabileceğini, bu stratejiyi onkolojinin ötesine, belirli proteinlerin azaltılmasının sağlığı yeniden kazandırabileceği diğer durumlara genişletebileceğini öne sürüyor.
Atıf: Diamond, P.D., Sauer, P.V., Holm, M. et al. Context-dependent translation inhibition as a cancer therapeutic modality. Nat Commun 17, 1963 (2026). https://doi.org/10.1038/s41467-026-69891-2
Anahtar kelimeler: ribozoma hedeflenen kanser tedavisi, çeviri inhibisyonu, MYC kaynaklı tümörler, bağlama-bağımlı küçük moleküller, triple-negatif meme kanseri