Clear Sky Science · tr
Büyük ölçekli geçiş yolları ve alt-mesoskopik protein komplekslerinde ara konformasyonların verimli örneklenmesi
Hareket Halindeki Proteinleri İzlemek
Hayatta kalmamızı sağlayan birçok molekül katı Lego tuğlaları gibi durmaz; daha çok sürekli şekil değiştiren küçük makineler gibidir. Bu hareketler enerji üretimi, DNA onarımı ve virüslerin hücrelere girişine izin verme gibi süreçleri güçlendirir. Kryo-elektron mikroskobi gibi deneyler bu şekillerin bazılarını dondurabilir, ancak aradaki geçici adımları yakalayamaz. Bu makale, eBDIMS2 adındaki yeni bir bilgisayar yöntemini tanıtıyor; bu yöntem, daha önce sıradan bir bilgisayarda simüle edilmesi çok büyük ve karmaşık olduğu için erişilemeyen devasa moleküler makineler için bile protein hareketinin "eksik karelerini" doldurabiliyor.
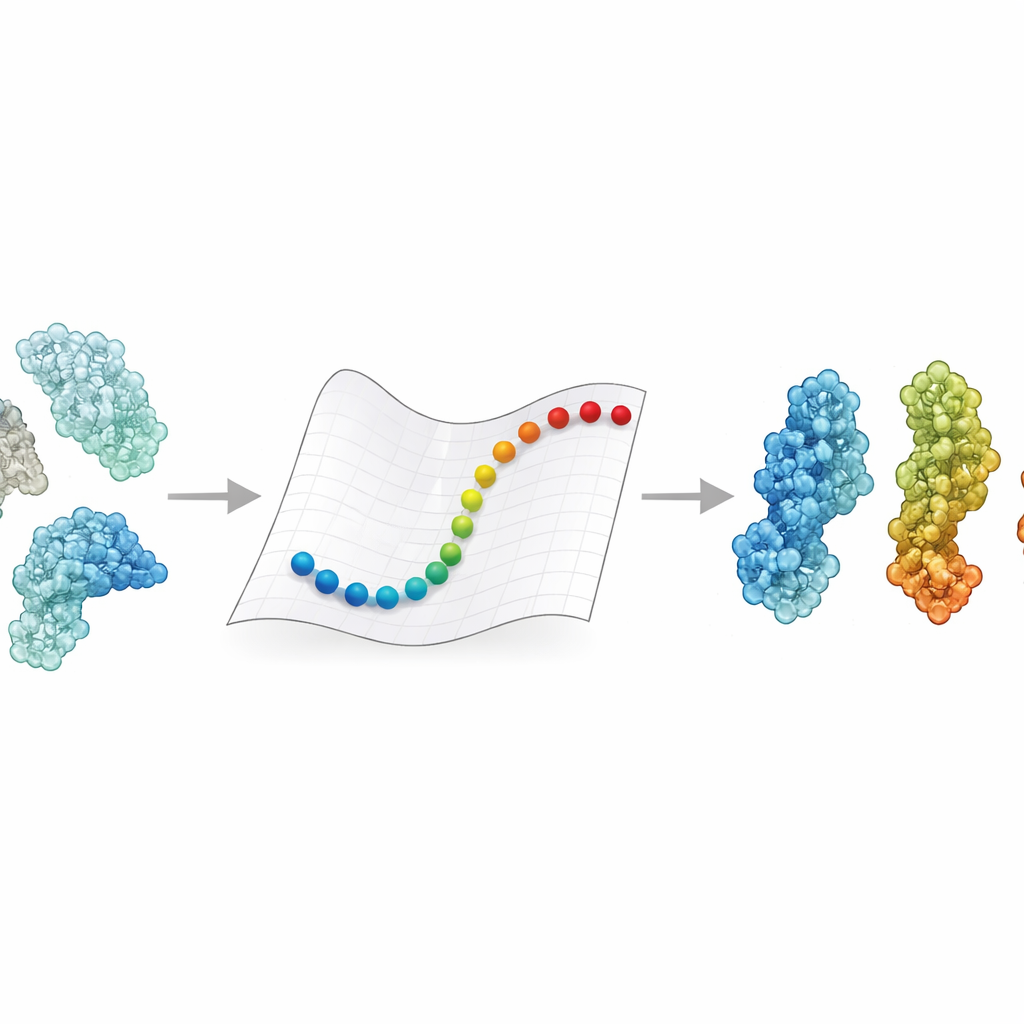
Protein Şekil Değişiklikleri Neden Önemlidir
Proteinler nadiren tek bir pozda kilitli kalır. Açılır ve kapanır, voltaj değişimleri, pH ya da bir bağlayıcı molekülün tutunması gibi sinyallere yanıt olarak burkulur ve bükülürler. Bu değişimler bir enzimin açık ya da kapalı olmasını, bir reseptörün bir virüsü yakalayıp yakalayamamasını belirleyebilir. Deneyler bize birkaç ana şeklin ayrıntılı anlık görüntülerini verir; moleküler dinamikler simülasyonları ise ilke olarak bu durumları her atomu zaman içinde izleyerek birbirine bağlayabilir. Ancak kryo-elektron mikroskobiyle elde edilen ve sıklıkla yüz binlerce ila milyonlarca Dalton ağırlığındaki dev komplekslerin hareketlerini takip etmek genellikle süperbilgisayarlar ve haftalar süren işlem gerektirir. Sonuç olarak, birçok tıbbi açıdan önemli dev için bir durumun diğerine nasıl dönüştüğünü hâlâ bilmiyoruz.
Protein Peyzajlarında Daha Hızlı Bir Rota
eBDIMS2, proteinlerin temsil edilme biçimini ve hareketlerinin hesaplanmasını sadeleştirerek kestirme bir yol izler. Her atomu takip etmek yerine her amino asidi, elastik bir ağdaki yaylarla bağlanmış tek bir nokta olarak ele alır. Bu yaylar proteinin farklı bölümlerinin birlikte nasıl hareket etme eğiliminde olduğunu yakalar. Yöntem daha sonra yapıyı bir deneysel olarak bilinen durumdan diğerine itmek için sıvı içindeki sallantıyı taklit eden matematiksel kurallar olan Brown hareketi kullanır. Kritik olarak, eBDIMS2 gerçekten önemli olan etkileşimlere odaklanır; mesafe kesme eşikleri ve paralel hesaplama kullanarak maliyeti azaltır. Bu, programın ölçeklenmesini yaklaşık kareden neredeyse lineere iyileştirir. Pratikte bu, iki milyon Daltona yakın dev montajlar için geçişlerin masaüstünde saatler içinde keşfedilebileceği, aksi halde aslında erişilemez olan durumların erişilebilir olduğu anlamına gelir.
Yolları Gerçek Proteinlerle Karşılaştırmak
Bu hızlı yolların biyolojik açıdan anlamlı olup olmadığını görmek için araştırmacılar 47 büyük protein ve ilave 15 kompleksten oluşan topluluklar derlediler; bunlar çoğunlukla kryo-elektron mikroskopi ile çözülmüş yüzlerce yapıyı içeriyordu. Bu yapıları açık, kapalı, aktif veya inaktif gibi konformasyon peyzajlarına düzenlemek için her proteinin hareket edebileceği baskın yolları seçen istatistiksel bir araç olan temel bileşen analizi kullandılar. eBDIMS2 daha sonra bu peyzaj üzerinde son durum çiftlerini birbirine bağlamaya çalışıldı. Ortaya çıkan yollar aynı düşük boyutlu haritalara geri projekte edildi ve deneysel olarak gözlemlenen ara durumlara yakın, düzgün rotalar izleyip izlemedikleri incelendi. Sistemlerin %30’undan fazlasında, simüle edilen rotalar, giriş olarak sağlanmamış ara yapılarla birkaç ångström içinde yakınlaştı. DNA onarım enzimi DNA-PKcs veya koronavirüs spike proteini gibi zorlu vakalarda, kaba taneli yollar hedeflenmiş moleküler dinamikler ve ileri düzey geliştirilmiş örnekleme çalışmaları gibi çok daha maliyetli atom düzeyindeki simülasyonlarla da iyi örtüştü.
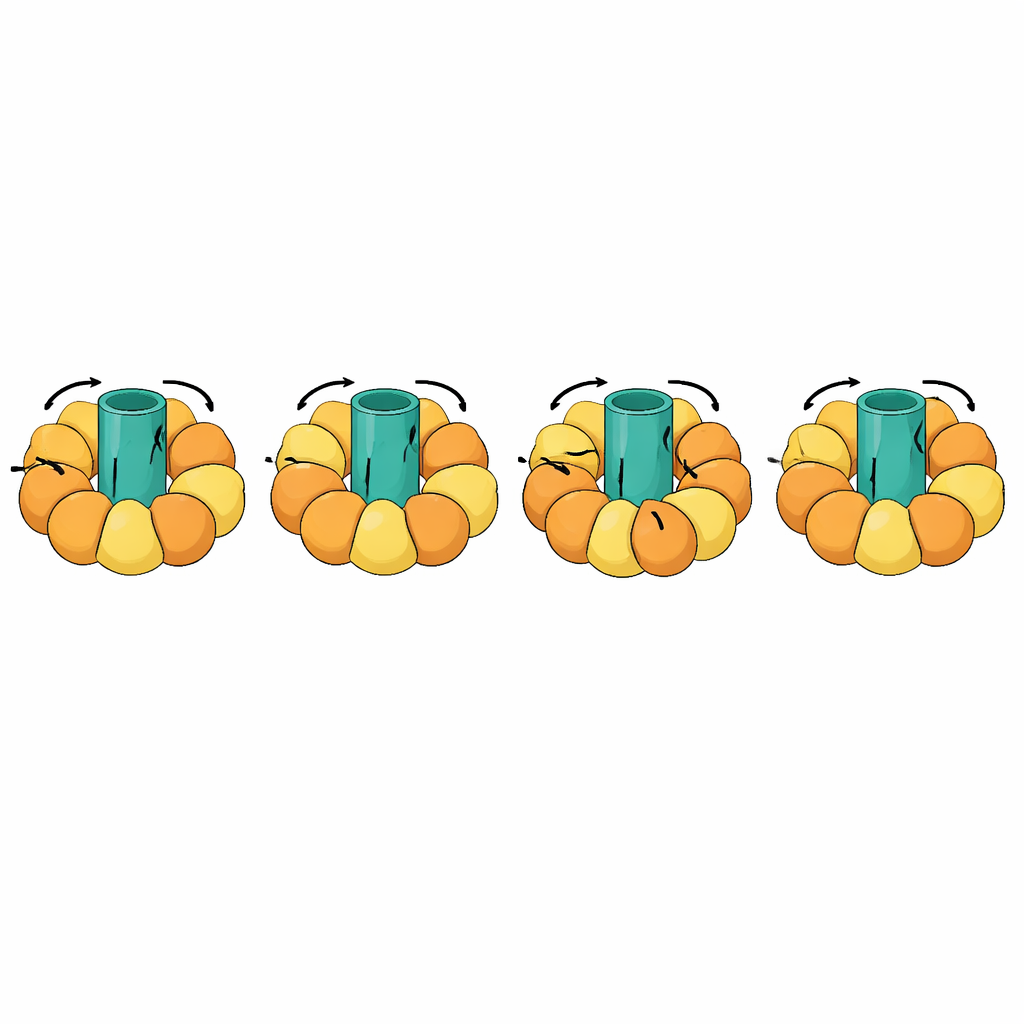
Dev Moleküler Makineleri İzlemek
En çarpıcı testlerden biri, membrandaki dönen bir rotorla çevresindeki altbirimlerde açılma ve kapanma hareketlerini eşleyen ATP sentazları gibi döner makineleri içeriyordu. Bu geçişler son derece karmaşıktır: molekülün bazı bölümleri birim olarak sert kalıp dönmeli, diğerleri ise koreografili bir döngü içinde esnemelidir. eBDIMS2 böyle yarı-rijit parçalar ve eksik segmentlere sahip tamamlanmamış deneysel modeller için özel işlem getirir; bunlar kryo-elektron mikroskopide sıkça rastlanan durumlardır. Bu özelliklerle ATP sentazının tam dönüşsel döngülerini ve moleküler şaperonlar, reseptörler ve viral montajlar gibi diğer büyük kompleksleri simüle edebilir. Üretilen ara yapılar, bazı rakip yöntemlerin oluşturduğu ciddi bozulmalardan kaçınır ve ilaç tasarımı hesaplamalarına veya daha uzun, daha ayrıntılı simülasyonlara uygun atomistik modellere dönüştürülebilir.
Bu Biyoloji ve Tıp İçin Ne Anlama Geliyor
Araştırma, eBDIMS2’nin geleneksel simülasyonların erişemediği sistemler için bilinen protein şekilleri arasındaki temel rotaları güvenilir şekilde taslağını çıkarabildiğini gösteriyor. Bu yöntem ayrıntılı atom düzeyindeki filmlerin yerini tutmaz veya kesin enerjiler ve zamanlamalar sunmaz; ancak yalnızca bir çift deneysel yapı kullanarak büyük moleküler makinelerin nasıl hareket edebileceğini haritalandırmak için hızlı ve fiziksel temelli bir yol sunar. Yapısal veri tabanları kanser, enfeksiyon ve diğer hastalıklarla ilişkili büyük protein montajlarının birden çok durumu ile doldukça, bu yaklaşım araştırmacılara noktaları birleştirmek, olası ara durumları önermek ve daha yüksek çözünürlüklü yöntemler veya hedefe yönelik ilaç tasarımı ile nereye bakılacağını yönlendirmek için erişilebilir bir araç sağlar.
Atıf: Scaramozzino, D., Lee, B.H. & Orellana, L. Efficient sampling of large-scale transition pathways and intermediate conformations in sub-mesoscopic protein complexes. Nat Commun 17, 2202 (2026). https://doi.org/10.1038/s41467-026-69809-y
Anahtar kelimeler: protein dinamikleri, moleküler simülasyonlar, kryo-EM, konformasyon yolları, kabaca-danışan modelleme