Clear Sky Science · tr
Kardiyomiyositlerde IRF3 aktivasyonu, PGC-1α inhibisyonu yoluyla mitokondriyal oksidatif işlevi bozar ve kalp yetmezliğine yol açar
Neden stres altındaki kalpler ve yorgun hücreler önemli
Kalp yetmezliği genellikle kalbin "aşınması" olarak tanımlanır, ancak perde arkasında kronik inflamasyon ve kalp kası hücrelerindeki tükenmiş enerji santralleri hakkında da bir hikayedir. Bu çalışma, büyük sonuçları olabilecek görünüşte basit bir soruyu soruyor: kalp hücreleri içinde zararlı inflamasyonu ve bozulmuş enerji üretimini birleştiren tek bir moleküler anahtar var mı—ve varsa, o anahtarı çevirmenin kalp yetmezliğinin seyrini değiştirme olanağı var mı? Bu ipi takip ederek, yazarlar önemli bir oyuncu keşfediyor ve kalbin kendi enerji programını nazikçe güçlendirmenin farelerde kısmen başarısız kalpleri düzeltebileceğini gösteriyor.
Hastalıklı insan kalplerinde bir moleküler anahtar
Araştırmacılar, hücrelerin viral enfeksiyonlara yanıt vermesine yardımcı olmasıyla en çok bilinen IRF3 adlı bir proteine odaklandı. Koroner damar tıkanıklığından sonra azalan kan akışı nedeniyle ortaya çıkan yaygın bir kalp yetmezliği türü olan iskemi kaynaklı kardiyomiyopatili kişilerden alınan dokuyu incelediler. Bu başarısız kalplerde IRF3 sadece bulunmakla kalmıyordu—belirli bölgelerde kimyasal olarak etkinleşmişti, bu da onun gen programlarını aktif olarak yönlendirdiğinin bir işaretiydi. Aynı zamanda mitokondrilerin yakıtı oksidatif fosforilasyon yoluyla enerjiye dönüştürmesine olanak veren mekanizma belirgin şekilde zayıflamıştı. Benzer bir desen, kalp krizi modellerindeki farelerde de ortaya çıktı: bir koroner arter bağlandığında, kalp kası hücrelerindeki IRF3 güçlü şekilde aktive oldu ve IRF3 tarafından kontrol edilen genler açığa çıktı. Hasar görmüş mitokondrilerden salınan ve içsel "tehlike" sinyalleri gibi davranan mitokondriyal DNA parçaları bile izole kalp hücrelerinde IRF3'ü açmaya yetti.
IRF3’ü kapatmak kalbi koruyor
IRF3 aktivitesinin kalp kası hücrelerinde gerçekten hastalığı kötüleştirip kötüleştirmediğini test etmek için ekip, IRF3'ün yalnızca kardiyomiyositlerden çıkarılabildiği, diğer bağışıklık ve destek hücrelerinin etkilenmediği fareler geliştirdi. Kalp krizi indükledikten sonra, bu fareler aynı başlangıç yaralanmasına rağmen normal farelerden daha iyi pompalama fonksiyonuna ve daha az skar dokusuna sahipti. Deney kabındaki kalp hücrelerinde IRF3'ü susturmak, ilgili diğer proteinleri bozmak yerine inflamatuar genleri azaltıyordu. Birlikte bu sonuçlar, kalp hücresinin içindeki IRF3'ün sadece kenarda duran bir unsur olmadığını; iskemi sonrası inflamasyonu ve yapısal hasarı artırdığını ve kalp yetmezliğine geçişi desteklediğini ileri sürüyor.
IRF3 “açık” kaldığında yakıt sistemi çöker
Yazarlar sonra deneyi tersine çevirdiler: kardiyomiyositlerde IRF3'ün kalıcı olarak aktif bir duruma zorlanabildiği, kurnaz bir genetik "fosfomimetik" hilesi kullanan fareler yarattılar. Dışsal bir tetik olmasa bile, bu fareler hızla şiddetli kalp disfonksiyonu, kanda yüksek düzeyde inflamatuar haberci moleküller ve hücresel yaralanma belirtileri geliştirdiler. Kalp dokularına yapılan derinlemesine analiz, IRF3 kronik olarak aktif olduğunda PGC-1α adlı ana enerji koordinatörünü baskıladığını gösterdi. Bu molekül normalde sağlıklı mitokondrileri, yağların verimli yakılmasını ve dengeli hücresel enerjiyi teşvik eder. PGC-1α bastırıldığında birden çok mitokondriyal protein azaldı, elektron taşıma zinciri aksadı ve kalbin yakıt tercihlerinde kayma oldu: yağ yakımı için gerekli karnitin ve ilgili bileşikler düştü, keton kullanımı bozuldu ve glukoz kullanımı çarpıtıldı. Hücresel redoks dengesinin ana göstergelerinden biri olan NAD⁺/NADH oranı bile yanlış yöne kaydı.
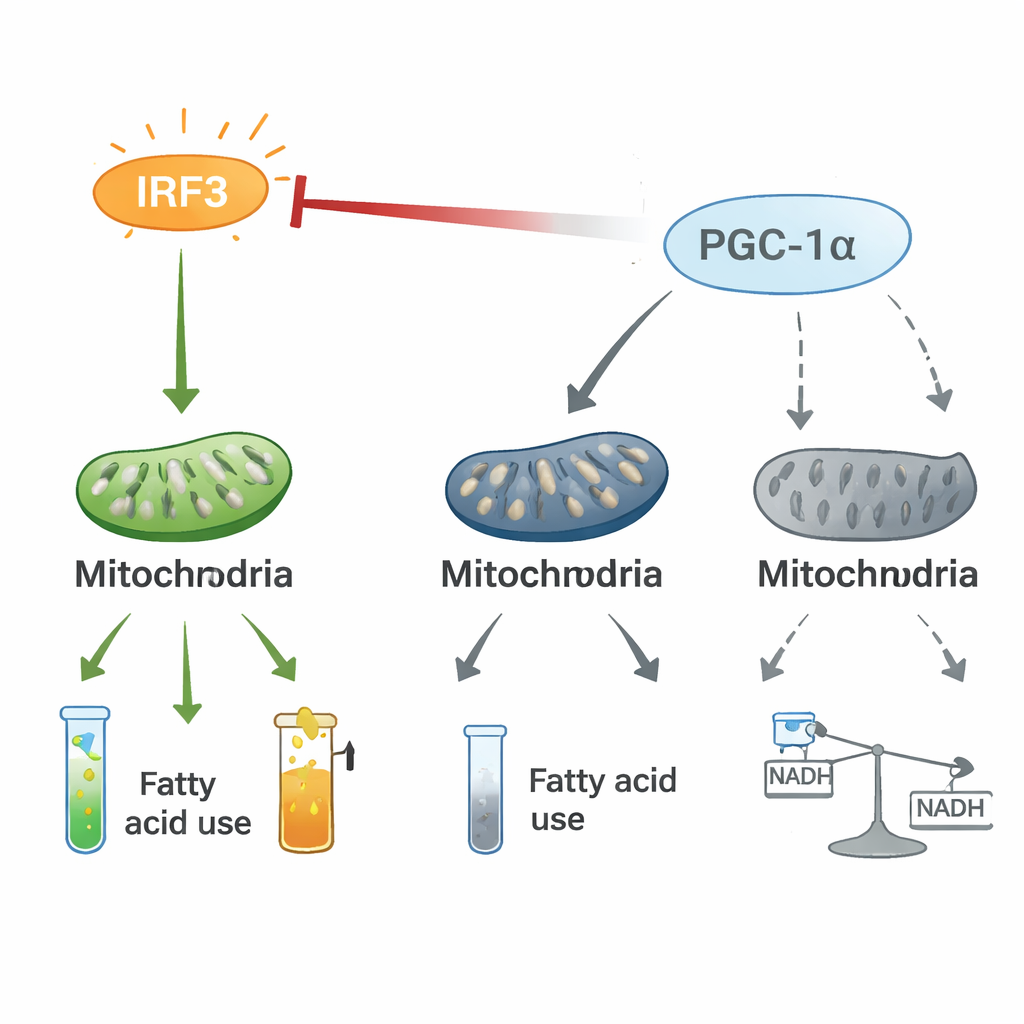
İnflamasyon ile enerji kontrolü arasında bir çekişme
Mekanik deneyler, IRF3 ile PGC-1α arasında iki yönlü bir düzenleyici eksen olduğunu ortaya koydu. Kalp hücrelerinde aktive olmuş IRF3, fiziksel olarak PGC-1α ile etkileşiyor ve yağ yakımı genlerini açma yeteneğini köreltir. IRF3'ü düşürmek PGC-1α düzeylerini ve aktivitesini yükseltirken, PGC-1α'yı artırmak IRF3 kaynaklı inflamatuar genleri söndürür ve mitokondriyal belirteçleri stres koşullarında—düşük oksijen veya bakteriyel toksinler gibi—bile geri getirir. Stabil izotop izleme, IRF3 aktivasyonunun karbonu normal enerji üretiminden sitrik asit döngüsü üzerinden alternatif bir yolu, pentoz fosfat yoluna yönlendirdiğini ve metabolitlerin akışını bozduğunu gösterdi. Pro-inflamatuar bir anahtar (IRF3) ile enerji yardımcı pilotu (PGC-1α) arasındaki bu çekişme, kalbin metabolizmasını inflamasyon ve enerji kaybını destekleyecek şekilde yeniden biçimlendiriyor gibi görünüyor.
Kalbin pillerini nazikçe yeniden şarj etmek
Son olarak ekip, PGC-1α'yı hafifçe yükseltmenin IRF3'ün zararlarını karşılayıp karşılayamayacağını sordu. Aşırıya kaçmadan PGC-1α'yı ılımlı şekilde yükseltmek için kalbe hedeflenmiş bir gen terapisi vektörü kullandılar; bunu IRF3 hiperaktif olan aynı farelerde uyguladılar. Bu mütevazı artış, pompalama fonksiyonunu iyileştirdi, mitokondriyal proteinleri artırdı, yağ yakımı ve NAD metabolizması için genleri güçlendirdi ve inflamatuar ile fibrotik gen aktivitesini azalttı. Hücre deneylerinde PGC-1α'yı aktif IRF3 ile birlikte ifade etmek, daha sağlıklı bir NAD⁺/NADH dengesini geri getirdi ve yakıt kullanımını tekrar yağlara kaydırdı. Bir okuyucu için bu, kalbin "pil yönetim sistemini" dikkatli bir şekilde yeniden şarj etmenin, sürekli açık kalan bir inflamatuar anahtarın zararlı etkilerini kısmen dengeleyebileceği anlamına geliyor.
Geleceğin kalp yetmezliği bakımına etkisi
Bu çalışma, IRF3'ü kalp kası hücreleri içindeki inflamasyon ile enerji yetersizliği arasındaki merkezi bir bağ olarak konumlandırıyor. Kalp yetmezliğinde inflamasyonu ve metabolizmayı ayrı sorunlar olarak ele almak yerine, bulgular IRF3–PGC-1α ekseni aracılığıyla birbirine bağlı olduklarını öne sürüyor. Bu bulgular farelerde ve hücrelerde elde edilmiş olsa da, gelecekteki tedavilerin ya IRF3 aktivitesini düşürebileceği ya da PGC-1α ve mitokondriyal işlevi güçlendirerek kalp krizi sonrası kalp yetmezliğini yavaşlatma veya önleme olanağı sunabileceğini düşündürüyor. Basitçe söylemek gerekirse, aşırı aktif bir hücresel alarm sistemini yatıştırmak ve kalbin enerji fabrikalarını desteklemek, zayıflamış kalplerin daha uzun süre güçlü atmasını sağlamak için güçlü bir birleşik strateji olabilir.
Atıf: Kumari, M., Evangelakos, I., Deshpande, A. et al. Activation of IRF3 in cardiomyocytes impairs mitochondrial oxidative function through PGC-1α inhibition and drives heart failure. Nat Commun 17, 2051 (2026). https://doi.org/10.1038/s41467-026-69792-4
Anahtar kelimeler: kalp yetmezliği, inflamasyon, mitokondri, kardiyomiyositler, PGC-1α