Clear Sky Science · tr
Hücre içi ve in vitro protein asetilasyonunu incelemek için hidrolize olmayan asetillizin analoğları
Proteinler üzerindeki küçük kimyasal etiketlerin önemi
Her hücrenin içinde, proteinler etkinliklerini açıp kapatan veya kısan küçük kimyasal etiketlerle sürekli olarak değiştirilir. Bu etiketlerden en önemlilerinden biri asetilasyon olarak adlandırılır; bu değişiklik bir proteinin davranışını alttaki genetik kodu değiştirmeden etkileyebilir. Belirli bir proteindeki belirli bir konumdaki asetilasyonun tam olarak ne yaptığını anlamak şaşırtıcı derecede zor oldu, çünkü hücreler bu etiketleri ekledikleri kadar çabuk çıkarabilirler. Bu çalışma, kaldırılamayan zeki bir kimyasal "temsilci" (stand‑in) tanıtıyor; bu, bilim insanlarına bu anahtarları yerinde dondurma ve ne olduğunu izleme olanağı veriyor.
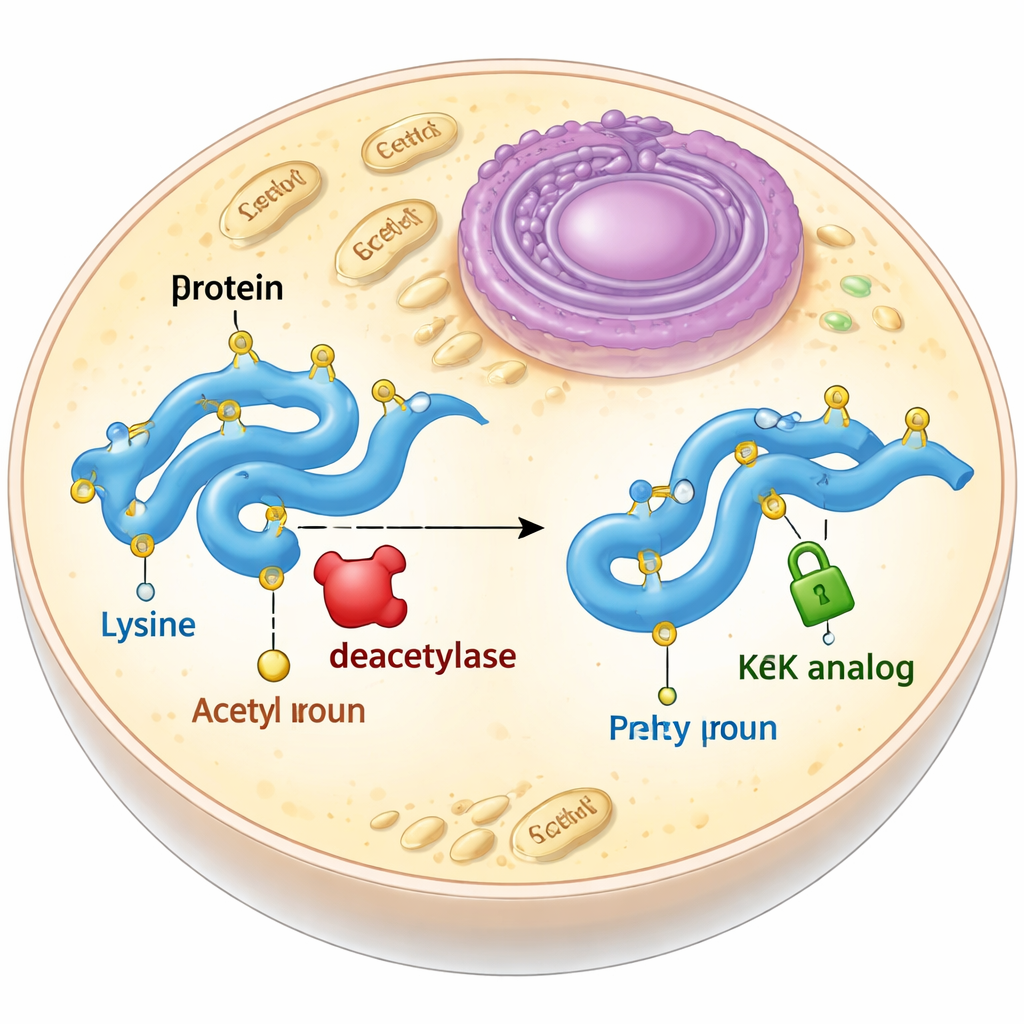
Kısa ömürlü bir etiket için kararlı bir temsilci
Asetilasyon genellikle lizinin adı verilen bir protein yapı taşı üzerinde olur. Bir lizin asetillenince pozitif yükünü kaybeder ve yan zinciri biraz uzar. Biyologlar bunu taklit etmek için sıklıkla lizini yüklü olmayan ama daha kısa olan glutamin ile değiştirirler ya da genişletilmiş genetik kod kullanarak gerçek asetillizin eklerler. Her iki yaklaşımın da sakıncaları vardır: glutamin asetilasyonun neden olduğu şekil değişikliklerini tam olarak yeniden üretmez ve gerçek asetillizin hücre içindeki deasetilazlar adı verilen enzimler tarafından hızla çıkarılmasıyla karşılaşılır. Yazarlar, doğru boyut ve şekli koruyan ancak kaldırılamayan asetillizin benzerlerini tasarlamayı ve test etmeyi amaçladılar.
Model bir proteinde yeni kimyasal taklitçilerin test edilmesi
Ekip ilk olarak, kendisi birçok farklı etiketle dekore edilen küçük ve iyi incelenmiş bir protein olan ubikitine odaklandı. İleri düzey genetik mühendislik kullanarak, ubikitinin bir konumuna farklı lizin varyantları yerleştirdiler: doğal asetillizin, TFAcK ve ketolizin (KeK) adlandırılan iki kaldırılamayan analog ve glutamin, alanin ve arjinin gibi yaygın temsilciler. Ardından bu değişikliklerin ubikitinin şekli ve işlevi üzerindeki etkilerini incelediler. Yüksek çözünürlüklü NMR ölçümleri asetillizin, TFAcK ve KeK’nin özellikle merkezi bir heliks çevresinde neredeyse aynı yapısal değişiklikleri ürettiğini gösterdi; oysa glutamin ve diğer basit mutasyonlar bunu yapmadı. HDM2 adlı bir enzim kullanılarak yapılan fonksiyonel testler, asetillizin, TFAcK veya KeK taşıyan ubikitinin benzer davrandığını ve glutamin versiyonundan farklı olduğunu ortaya koydu; bu da yan zincirin yalnızca yükü değil, uzunluğu ve hacminin de kritik olduğunu vurguluyor.
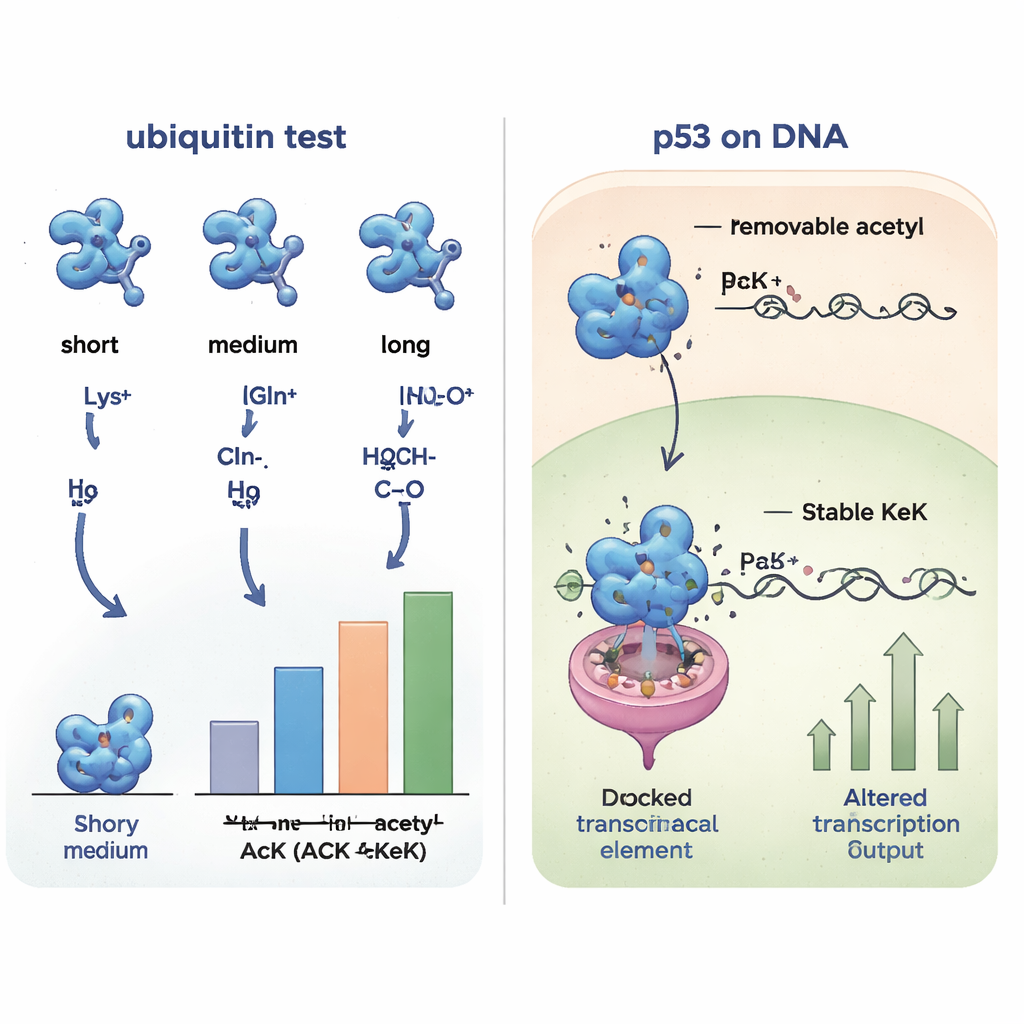
Hücre çapında protein ortaklıklarını araştırmak
Küçük yapısal değişiklikler bir proteinin hangi ortaklarla etkileşime girdiğini değiştirebileceğinden, araştırmacılar bir sonraki adımda farklı ubikitin versiyonlarının insan hücre özütlerindeki diğer proteinlere nasıl bağlandığını karşılaştırdılar. Bağlanan partnerleri yakalayıp kütle spektrometrisi ile tanımlayarak, asetillizin, TFAcK veya KeK içeren ubikitinin çok benzer etkileşim desenlerini paylaştığını, glutamin veya alanin içeren formların ise birlikte gruplaşıp farklı göründüğünü buldular. Pozitif yüklü varyantlar (lizin veya arjinin) ise başka bir grubu oluşturdu. Bu sistematik karşılaştırma, kaldırılamayan analogların özellikle KeK’nin gerçek asetilasyonu yapı ve bağlanma davranışı bakımından geleneksel glutamin yerine çok daha iyi taklit ettiğini gösterdi.
Tümör baskılayıcı p53’te asetilasyonu kilitlemek
Bu araçların canlı hücrelerde işe yarayıp yaramadığını görmek için yazarlar genellikle "genomun bekçisi" olarak adlandırılan önemli tümör baskılayıcı p53’e yöneldiler. p53’ün DNA bağlayıcı bölgesindeki belirli lizinekler asetillenebilir ve bunun sonucunda hangi genleri etkinleştirdiği değişir; örneğin hücre döngüsünü durduran veya hücre ölümünü tetikleyen genler. Ekip, p53’ün iki önemli lizin pozisyonuna (120 ve 164) yalnızca ilgili standart dışı amino asit sağlandığında asetillizin, TFAcK veya KeK yerleştirecek şekilde insan hücrelerini mühendislikledi. Üçü de p53’e entegre edilebildi, ancak ayrıntılı ölçümler hücrelerde asetil ve TFAcK gruplarının büyük ölçüde deasetilazlar tarafından çıkarıldığını, oysa KeK’nin yerinde kaldığını gösterdi. Bir rapor genini ve doğal p21 genini aktive etme yeteneğini test ettiklerinde, bu konumlarda KeK taşıyan varyantlar çok daha az aktiftı; bu, o pozisyonlardaki asetilasyon kilitlendiğinde beklenenle uyumluydu. Asetillizin ve TFAcK ise deasetillenmiş oldukları için daha çok normal p53 gibi davrandı.
Hücre kararlarını incelemek için ne anlama geliyor
Genel olarak çalışma, KeK’nin sadık ve kaldırılamayan bir asetillizin temsilcisi olduğunu gösteriyor: hem yapısal değişiklikleri, hem bağlanma tercihlerini hem de asetilasyonun fonksiyonel sonuçlarını yakından yeniden üretir, fakat hücresel enzimler tarafından silinemez. Uzman olmayanlar için bunun anlamı şu: araştırmacıların artık bir proteinin tek bir sitesindeki tersinir kimyasal anahtarı "dondurma" ve bunun gen düzenlemesi ve hücre kaderi kararları gibi süreçleri nasıl etkilediğini gözlemleme yolları olduğudur. Bu, asetilasyonun özgül rollerini diğer örtüşen modifikasyonlardan ayırmayı çok daha kolay hale getirmeli ve nihayetinde hatalı düzenlenen protein asetilasyonunun kanser gibi hastalıklara nasıl katkıda bulunduğunu açıklığa kavuşturabilir.
Atıf: Kienle, S.M., Sigg, M., Schneider, T. et al. Non-hydrolyzable acetyllysine analogs to study protein acetylation in vitro and in cells. Nat Commun 17, 1985 (2026). https://doi.org/10.1038/s41467-026-69782-6
Anahtar kelimeler: protein asetilasyonu, posttranslasyonel modifikasyon, ubikitin, p53, genetik kod genişletme