Clear Sky Science · tr
İnsan nöral progenitör hücrelerinde greft sonrası dinamik transkriptomik yeniden yapılanma, retinitis pigmentosa rat modelinde görme korunması mekanizmalarını ortaya koyuyor
Solmakta olan görmenin korunması neden önemli
Retinitis pigmentosa, genellikle gece körlüğü ile başlayıp ilerleyerek yasal körlüğe kadar gidebilen, görmeyi yavaşça elinden alan kalıtsal hastalıklar grubudur. Bu duruma yüzlerce farklı gen mutasyonu neden olabildiği için her birini ayrı ayrı gen terapisiyle tedavi etmek zordur. Bu çalışma daha evrensel bir yaklaşımı araştırıyor: laboratuvarda yetiştirilen olgunlaşmamış sinir hücreleri olan insan nöral progenitör hücrelerini göze naklederek kalan ışık algılayıcı hücreleri korumak. Greftlenen hücrelerin tam olarak nasıl davrandığını ve görmeyi nasıl koruduklarını anlamak, yalnızca retinitis pigmentosa için değil, diğer kör edici hastalıklar için de gelecekteki tedavileri şekillendirebilir.
Hücreleri değiştirmek yerine onlara yardım etmek
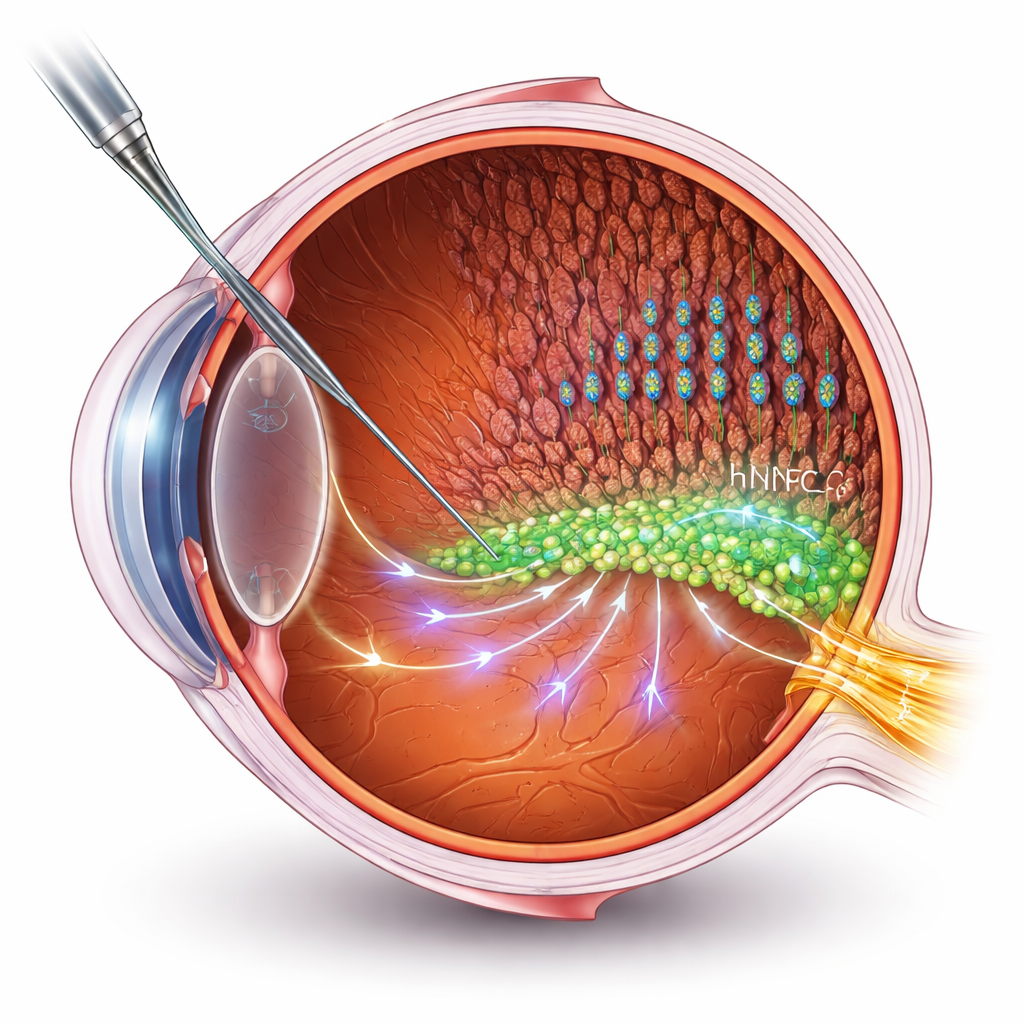
Birçok kök hücre terapisi ölü veya hasarlı hücreleri geri koymayı hedefler. Ancak ileri retinal hastalıklarda beyne yeni bağlantılar kurmak büyük bir teknik engeldir. Burada araştırmacılar farklı bir yol izliyor: insan nöral progenitör hücrelerini (hNPC'ler) hastanın kendi retinal hücrelerini destekleyen “yardımcılar” olarak kullanmak. hNPC'leri retinitis pigmentosa için iyi bilinen bir rat modelinin subretinal boşluğuna naklettiler ve görmeyi elektriksel kayıtlar ve davranış testleriyle ölçtüler. Tedavi edilen ratlar, tedavi edilmeyenlere kıyasla görsel fonksiyonu ve ışığı yakalayan çubuk ve konilerin de dahil olduğu fotoreseptör katmanlarının bütünlüğünü daha iyi korudu; ancak dejenerasyon yine de zamanla yavaşça ilerledi.
Greftlenen hücreler hastalıklı göz içinde nasıl değişiyor
Moleküler düzeyde neler olduğunu görmek için ekip binlerce bireysel hücrede hangi genlerin aktif olduğunu profilleyen tek hücre RNA dizilemesini kullandı. Nakilden sonra erken ve daha geç olmak üzere iki zaman noktasında greftlenen hNPC'leri izlediler. Transplante hücrelerin çoğu yeni fotoreseptörlere dönüşmek yerine astrosit benzeri destek hücrelerine olgunlaştı; daha küçük bir kısmı oligodendrosit veya olgunlaşmamış nöron belirteçleri gösterdi. Zaman içinde bu hücreler stabil hale geldi ve stresli, dejeneratif bir ortama uyum sağlamış ve komşu retinal hücrelerle yakın etkileşime girmeye uygun özellikler benimsediklerini gösterdiler.
Koruyucu sinyaller, metabolizma ve temizlik
hNPC'ler MANF ve MYDGF gibi hücre sağkalımı, oksidatif stresin azalması ve inflamasyonun yatıştırılması ile ilişkilendirilenler de dahil olmak üzere zengin bir koruyucu protein (trofik faktör) karışımı üretti; ayrıca midkine ve pleiotrofin gibi nöral hücrelerin büyümesini ve hareketini destekleyen diğer faktörler de vardı. Bu moleküller hem grefti hem de çevreleyen retinayı etkiliyor gibi görünüyordu. Tedavi edilen ratlarda çubuklar ve koniler, görsel sinyal iletimi ve hücre bakımına yönelik destek açısından sağlıklı kontrollere daha yakın gen aktivite desenleri gösterdi. Greftlenen hücreler ayrıca hücresel artıkların temizlenmesi ve metabolizmanın ayarlanmasıyla ilgili yolakları güçlendirdi; bu da fotoreseptörlerin hastalık sırasında biriken enerji talepleri ve toksik artıklarla başa çıkmasına yardımcı olduklarını düşündürüyor.
Destek hücrelerini yatıştırmak ve retinal çevreyi yeniden şekillendirmek
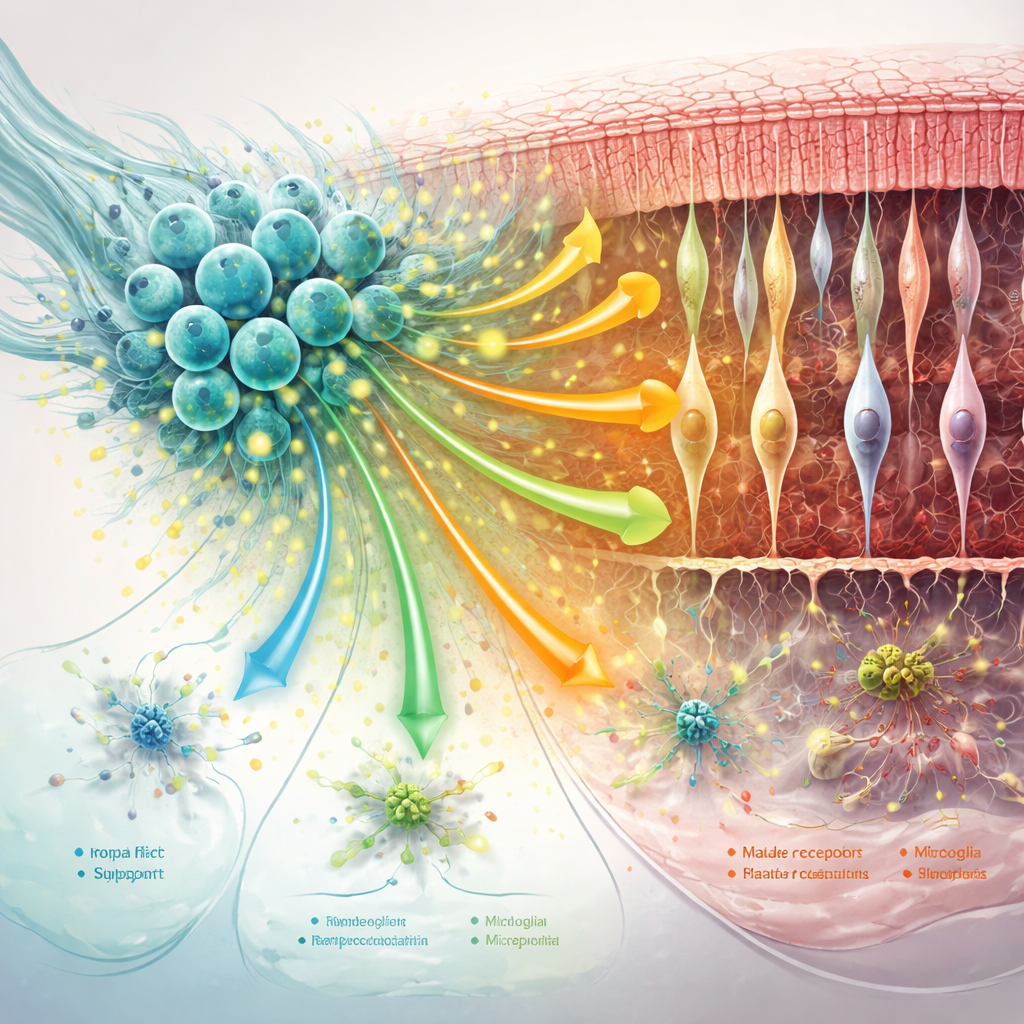
Retinanın destek ağı—Müller glia, mikroglia ve etrafındaki protein matriksi—dejenerasyonu ya kötüleştirmede ya da yavaşlatmada büyük rol oynar. Çalışma, hNPC tedavisinin Müller gliasındaki zararlı “reaktif” değişikliklerin ana belirteçlerini azalttığını ve mikrogliayı özellikle erken zaman noktasında aşırı inflamatuar durumlardan uzaklaştırdığını buldu. Aynı zamanda sinapsları stabilize etmeye, hücreleri birbirine yapıştırmaya ve fotoreseptörlerin etrafındaki iskelenin korunmasına yardımcı olan iletişim sinyalleri güçlendi. Hastalık ilerledikçe bu faydaların bazıları azaldı: hücrelerarası iletişim genel olarak zayıfladı, MANF ile ilişkili sinyalizasyon da dahil olmak üzere bazı koruyucu yolaklar düştü ve destek hücreleri daha çok stres ve immün odaklı profiller benimsedi.
Gelecekteki göz tedavileri için anlamı
Uzman olmayan biri için alınacak mesaj şudur: nakledilen insan nöral progenitör hücreleri, dejeneratif bir retina içinde yerinde “ilk müdahale edenler” gibi davranabilir. Retinayı baştan inşa etmezler; fakat koruyucu moleküller salar, metabolizmayı ayarlar, zararlı inflamasyonu yatıştırır ve yerel yapıyı korumaya yardımcı olur; bunların hepsi görme kaybını yavaşlatır. Bununla birlikte, çevre daha düşmanca hale geldikçe ve greft ile konak hücreler arasındaki iletişim zayıfladıkça bu koruyucu etki zamanla azalır. Yazarlar, MANF gibi anahtar faktörlerin güçlendirilmesinin ve greftin genetik mühendisliği veya kombine tedavilerle konak retinanın sağlığının iyileştirilmesinin, geçici bir rahatlamayı kalıcı görme korumasına dönüştürmek için gerekli olabileceğini öne sürüyorlar.
Atıf: Shahin, S., Bell, S., Lu, B. et al. Dynamic transcriptomic remodeling in grafted human neural progenitor cells uncovers mechanisms for vision preservation in a rat model of retinitis pigmentosa. Nat Commun 17, 2164 (2026). https://doi.org/10.1038/s41467-026-69776-4
Anahtar kelimeler: retinitis pigmentosa, kök hücre terapisi, retinal dejenerasyon, nöroprotektion, tek hücre RNA dizileme