Clear Sky Science · tr
N-Myc MB0-MBI bölgesi Aurora kinaz A’nın N-lobuyla özgül ve dinamik etkileşim kurar
Kanser tedavisi açısından neden önemli
Birçok agresif çocukluk çağı kanseri, tümör hücrelerinin büyümesini sürdürmek için N-Myc adlı bir proteine bağımlıdır. N-Myc kendisi, sert bir kilide uyabilecek anahtar gibi tek bir katı yapı göstermediği için ilaçlarla doğrudan engellenmesi zordur; daha çok gevşek bir spagetti parçası gibi davranır. Bu çalışma, N-Myc’in kanser hücrelerinin hayatta kalmasına yardımcı olmak ve aktivitesini artırmak için başka bir protein olan Aurora kinaz A (AurA) ile nasıl kavradığını benzeri görülmemiş ayrıntıda ortaya koyuyor. Bu ortaklığı haritalandırarak, araştırmacılar onu küçük moleküllerle parçalamanın gerçekçi bir yolunu ortaya çıkarıyorlar.
Esnek bir sorun yaratan, sağlam bir ortak bulur
N-Myc, hücre büyümesini, metabolizmayı ve bölünmeyi kontrol eden MYC ailesinin ana anahtarlarından biridir. Aşırı üretildiğinde bu anahtarlar, özellikle çocuklarda yüksek riskli nöroblastom gibi sinir sistemi tümörlerinde güçlü kanser sürücüleri haline gelir. Pek çok enzim veya reseptörün aksine N-Myc tek başına sabit bir 3B şekline katlanmaz; sürekli kıpırdayan ve yeniden şekillenen “doğası gereği düzensiz” bir proteindir. Bu esneklik onu uyarlanabilir kılar ama aynı zamanda ilaçla hedeflemeyi son derece zorlaştırır. Buna karşılık AurA, hücre bölünmesini düzenlemeye yardımcı olan iyi yapılandırılmış bir enzimi temsil eder. Önceki çalışmalar AurA’nın tümör hücrelerinde N-Myc’i stabilize etmeye yardımcı olduğunu ve iki proteinin fiziksel olarak etkileştiğini göstermişti, ancak temas noktalarının tam doğası ve önemi belirsizliğini koruyordu.
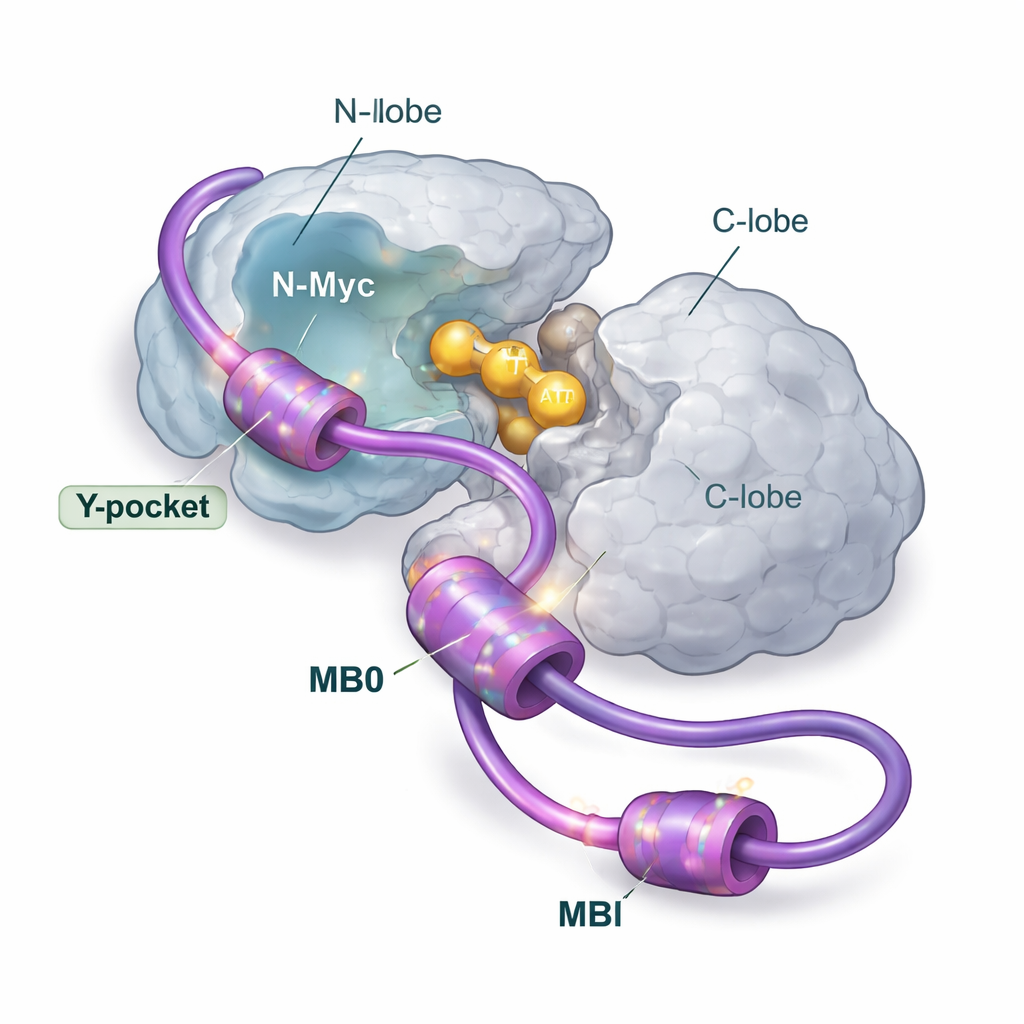
Birden çok kavrama noktası, bir ana iniş yeri
Yazarlar, nükleer manyetik rezonans, X-ışını saçılması, kütle spektrometrisi, kalorimetri ve bilgisayar modellemesi de dahil olmak üzere geniş bir yapısal ve biyofiziksel yöntem takımı kullanarak N-Myc ile AurA’nın çözelti içinde nasıl bir araya geldiğini parçalara ayırdı. Odaklandıkları nokta N-Myc’in ön ucu olup burada MB0 ve MBI adı verilen iki korunmuş bölge bulunur. Bu kısa segmentler, fenilalanin, tirozin ve triptofan gibi aromatik yapı taşları bakımından zengindir ve ortak proteinlerin yağlı ceplerine tutunma eğilimindedir. Ekip, N-Myc’in AurA’ya esas olarak 1:1 oranında bağlandığını, MB0 ve MBI’nin birincil temas bölgeleri olarak davrandığını gösteriyor. Önceki kristal yapılarında dikkat çeken başka bir N-Myc bölgesi, tam MB0–MBI bölgesi mevcut olduğunda yalnızca küçük bir rol oynuyor.
Enzimi açan dinamik bir el sıkışma
N-Myc bağlandığında tek bir kilitlenmiş pozisyona geçmek yerine büyük ölçüde düzensiz kalır. Veriler “bulanık” bir kompleks gösteriyor: birkaç N-Myc segmenti AurA N-lobundaki farklı yamalara sırayla temas ediyor, özellikle Y-cebi olarak bilinen bir oluğa ve sinyalleri aktif merkeze bağlayan yakınlardaki bir döngüye. Bu gevşekliğe rağmen etki nettir—MB0 ve MBI’nin bağlanması AurA N-lobunu stabilize eder ve kinaz aktivitesini artırır; yani fosfat gruplarını hedeflerine daha verimli aktarır. Araştırmacılar MB0 ve MBI’deki kilit aromatik kalıntıları sistematik olarak alaninle değiştirdiklerinde, N-Myc–AurA kompleksi zayıfladı, enzim daha az stabilize oldu ve aktivitesi düştü. Bu, aksi halde gevşek N-Myc zincirinde bulunan spesifik aromatik “çapa”ların AurA’yı açmak için gerekli olduğunu gösterir.
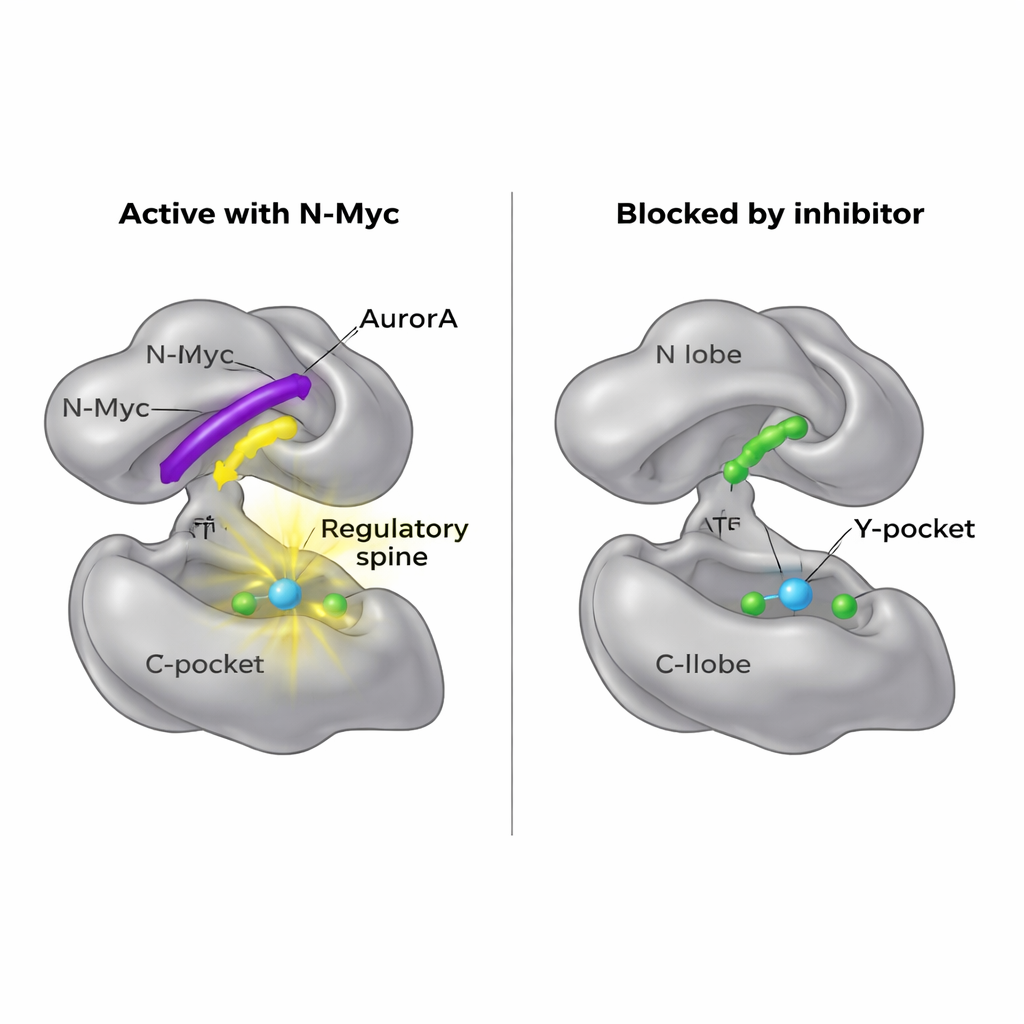
Yeni bir ilaç giriş noktasını kırmak
N-Myc’in kendisi ilaçla hedeflenmesi zor olduğundan, araştırmacılar bunun yerine AurA üzerindeki kenetlenme bölgesini engelleyip engelleyemeyeceklerini sordular. Yapısal haritaları, MB0 ve MBI’nin AurA N-lobunun TPX2 adlı başka bir ortak proteinin AurA’yı aktive etmek için kullandığı aynı genel bölgeyi işgal ettiğini ortaya koydu. AurkinA adlı küçük bir molekülün Y-cebine girerek TPX2’yi yerinden ettiğini zaten biliyorduk. Bağlanma deneylerinde AurkinA, N-Myc ile AurA’nın N-lobu için etkili bir şekilde rekabet etti ve N-Myc1–69 ile N-Myc1–100 fragmanlarının bağlanmasını engelledi. Bu sonuç, N-lob yüzeyinin ve özellikle Y-cebinin, yalnızca TPX2 gibi klasik düzenleyicileri değil aynı zamanda N-Myc gibi düzensiz onkoproteinleri de kontrol eden ilaçlanabilir bir sıcak nokta olduğunu gösterir.
Gelecek terapiler için ne anlama geliyor
Bu çalışma, N-Myc–AurA ortaklığını tek bir katı bağlanma bölgesinden ziyade AurA N-lobu etrafında merkezlenen dinamik, çok temaslı bir kucaklaşma olarak yeniden çerçeveliyor. Uzman olmayanlar için ana mesaj şudur: N-Myc gibi şekilsiz bir kanser proteini bile, ortağı olan enzimin sağlam bir kenetlenme yamasını hedefleyerek dolaylı yoldan ele alınabilir. Mevcut N-lob bağlayıcı bileşiklerin N-Myc’i AurA’dan uzaklaştırabildiğini göstererek çalışma, bu etkileşimi seçici olarak bozacak ilaçlara giden net bir yol açıyor. Bu tür ajanlar, yüksek riskli çocukluk tümörlerinde N-Myc için kritik bir desteği zayıflatabilir ve daha fazla geliştirme ile uzun süredir “ilaçlanamaz” kabul edilen kanserler için yeni bir tedavi yolu sunabilir.
Atıf: Hultman, J., Morad, V., Tanner, E. et al. The N-Myc MB0-MBI region interacts specifically and dynamically with the N-lobe of Aurora kinase A. Nat Commun 17, 2016 (2026). https://doi.org/10.1038/s41467-026-69725-1
Anahtar kelimeler: N-Myc, Aurora kinaz A, doğası gereği düzensiz proteinler, nöroblastom, protein–protein etkileşim inhibitörleri