Clear Sky Science · tr
Ekzon dahil etme imzeleri, splice faktör aktivitesinin doğru tahminini sağlar
Hücresel Gizli Düzenleme İzlerini Okumak
Vücudumuzdaki her hücre, RNA mesajlarını proteinlere dönüştürmeden önce sürekli olarak düzenler. Bu düzenleme, splicing olarak adlandırılır ve bir hücrenin sağlıklı kalıp kalmayacağını ya da kanserleşip kanserleşmeyeceğini belirlemede rol oynar. Bu makalenin temelini oluşturan çalışma, RNA parçalarının hangilerinin korunup hangilerinin atıldığını—ekzon dahil etme imzaları olarak adlandırılan—dikkatle inceleyerek, bilim insanlarının splicing’i kontrol eden moleküler “editörlerin” aktivitesini karmaşık hastalıklarda bile doğru biçimde çıkarabileceğini gösteriyor.
Hücreler Mesajlarını Nasıl Kesip Yapıştırır
Genler tek bir kesintisiz şekilde okunmaz. Bunun yerine hücreler kodlamayan bölümleri çıkarır ve kodlayan parçaları, yani ekzonları, birleştirerek son RNA mesajlarını oluşturur. Splice faktörleri olarak adlandırılan uzman proteinler bu kes‑ve‑yapıştır sürecine rehberlik eder ve hangi ekzonların dahil edileceğine karar verir. Bu faktörlerin davranışı, kendi RNA ve protein düzeyleri, kimyasal modifikasyonları, hücre içindeki konumları ve diğer proteinlerle etkileşimleri gibi birçok düzenleme katmanından etkilenir. Bu kadar çok değişken splicing faktörlerinin davranışını değiştirebildiğinden, yalnızca tek bir tür veri—örneğin gen ekspresyonu—ölçülmesi genellikle bu faktörlerin gerçekte ne yaptığını açığa çıkarmaya yetmez.
Ekzon Desenlerini Aktivite Ölçümlerine Dönüştürmek
Transkripsiyon faktörleri üzerine yapılan önceki çalışmalardan ilham alan yazarlar farklı bir strateji öneriyor: splice faktörlerini doğrudan ölçmeye çalışmak yerine etkilerinden okumak. Bir splice faktörü değiştiğinde, hedef ekzonlarının dahil edilme oranı tanınabilir desenler halinde kayar. Ekip, bireysel splice faktörlerin susturulduğu, işlevsizleştirildiği veya aşırı eksprese edildiği yüzlerce deneyi derleyip bu verileri her bir faktörü açıkça etkileyen ekzonlarla bağlayan “ampirik ağlar” kurmak için kullandı. Ardından VIPER adlı hesaplamalı çerçeveyi uyarlayarak yeni bir ekzon dahil etme imzasını okudu ve gözlenen deseni açıklamak için her splice faktörünün ne kadar aktif olması gerektiğini puanladı.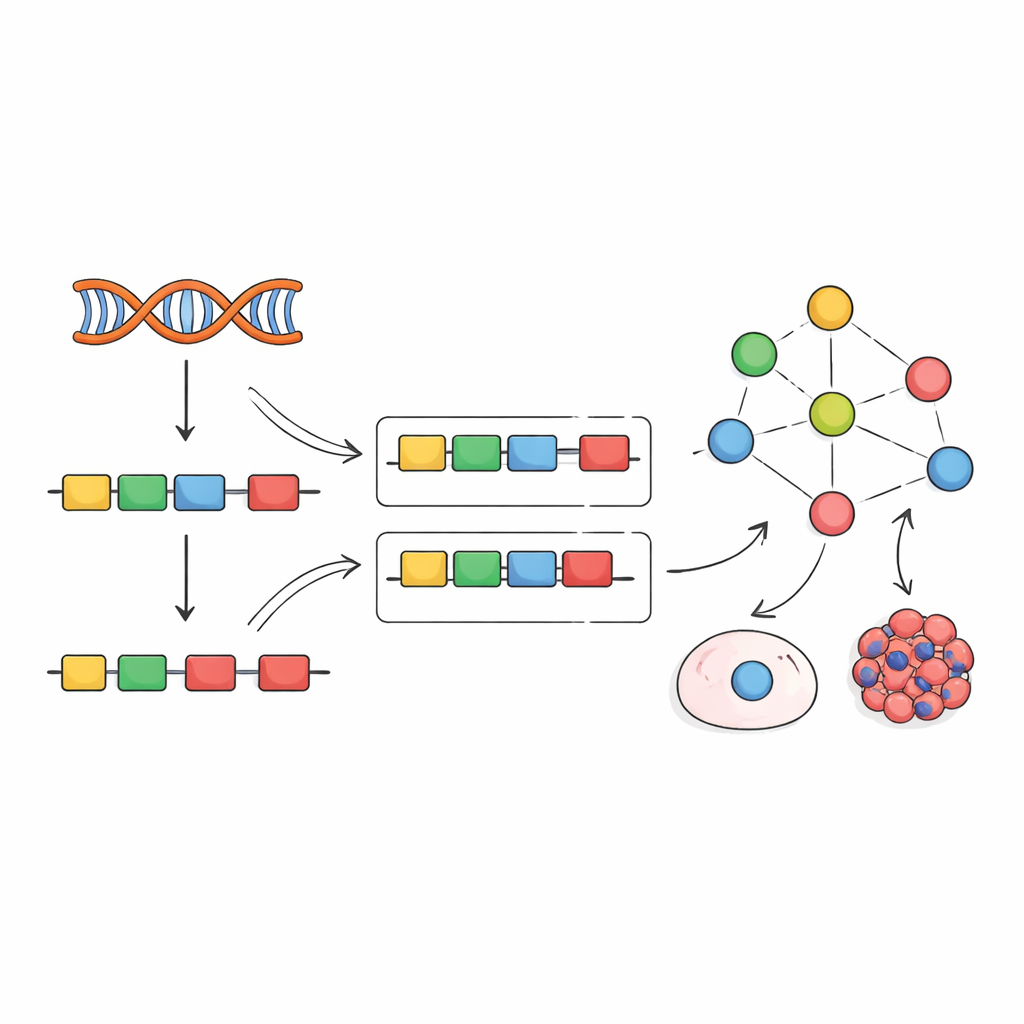
Yöntemi Gerçek Dünyadaki Müdahalelerde Test Etmek
Bu yaklaşımın işe yarayıp yaramadığını görmek için araştırmacılar ağ kurmanın ve aktivite puanları hesaplamanın çeşitli yollarını karşılaştırdı. Müdahale deneylerinden doğrudan türetilen ampirik ağlar ile VIPER’in zenginleştirme analizinin birleşimi, yalnızca istatistiksel çıkarıma dayanan alternatiflerden açıkça daha iyi performans gösterdi. Yöntem, çoğu testte deneysel olarak müdahale edilen splice faktörünü doğru şekilde tanımladı; bunu farklı hücre tipleri ve çalışmalar arasında bile başardı. Ayrıca daha ince düzenleyici mekanizmaları da yakaladı. Örneğin, Indisulam adlı bir kanser ilacı, RBM39 splice faktörü proteinini parçalayarak yok ederken, RBM39’un RNA düzeyleri telafi çabası gibi artıyor. Geleneksel ekspresyon analizi yanıltıcı olarak RBM39’un daha aktif olduğunu öne sürebilirken, ekzon‑temelli aktivite skoru ilacın bilinen etkisine uygun olarak belirgin bir işlev kaybını doğru şekilde ortaya koydu.
Kanserde Gizli Splicing Programlarını Ortaya Çıkarmak
Bu araçla donanmış olarak yazarlar, The Cancer Genome Atlas veritabanına yönelip birden çok tümör türünden ve eşleştirilmiş sağlıklı dokulardan ekzon düzeyinde verileri analiz ettiler. İki geniş ve tekrarlayan splicing programı keşfettiler. Bir program tümörlerde genellikle daha aktif olan splice faktörlerinden oluşuyor ve daha kötü hasta sağkalımıyla ilişkili—onkogen benzeri bir program. Diğer program ise tümörlerde sistematik olarak daha az aktif olan ve daha iyi sonuçlarla bağlantılı faktörleri içeriyor; bu da tümör baskılayıcı benzeri bir profile karşılık geliyor. Bu programlar hızlı hücre bölünmesi ve tümörlerin bağışıklık sisteminden saklanma yeteneği gibi temel kanser özellikleriyle ilişkili genleri etkiliyor. Örneğin, tümör‑baskılayıcı‑benzeri program tarafından düzenlenen bazı ekzonlar hastaların immün kontrol noktası tedavilerine ne kadar iyi yanıt verdiğini etkiliyor gibi görünerek yeni belirteçler veya müdahale noktaları olabileceğini işaret ediyor.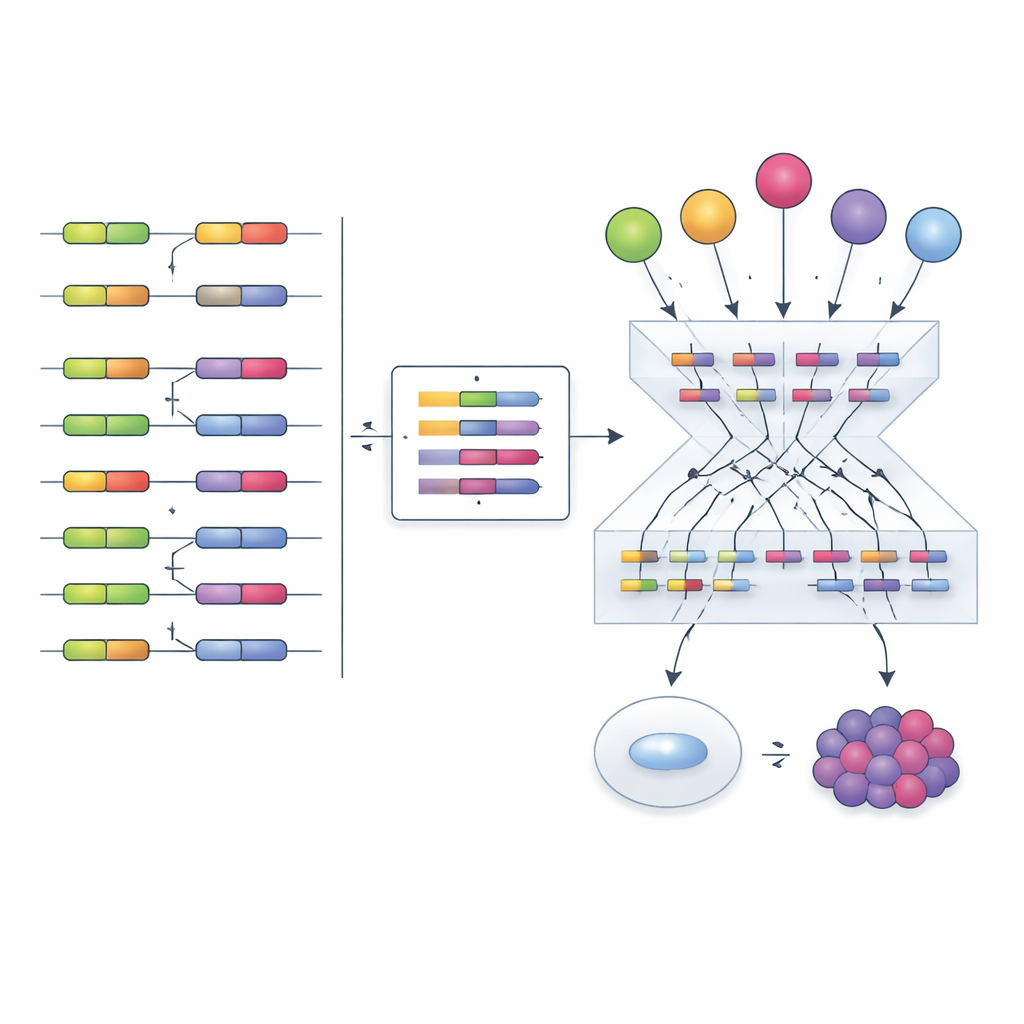
Kanser Yolunda Splicing Değişikliklerini Takip Etmek
Ekip ayrıca normalden immortalize olmuşa, tümör oluşturana ve nihayetinde metastaz yapan durumlara ilerleyen insan hücrelerinin adım‑adım bir modelini inceledi. Onkogen benzeri splicing programının, hücreler kanser sürükleyici mutasyonlar edindikçe daha aktif hale geldiğini, tümör‑baskılayıcı‑benzeri programın ise zayıfladığını buldular. RNA düzeyleri, protein bolluğu, kimyasal modifikasyonlar ve splice faktörlerin kendi içlerindeki splicing değişiklikleri gibi birden çok veri katmanını entegre ederek, bu program kaymalarını tetikliyor olabilecek odaklanmış bir aday moleküler olay seti tanımladılar ve gelecekteki deneysel testler için önceliklendirilmiş bir liste sundular.
Hastalar ve Gelecek Araştırma İçin Neden Önemli
Özetle çalışma, splice faktörlerinin karmaşık davranışının ekzonların nasıl dahil edilip atıldığından türetilen tek, yorumlanabilir bir aktivite skoruna indirgenebileceğini gösteriyor. Bu, pahalı çok‑omik profilleme gerektirmeden yalnızca standart RNA dizileme verileri kullanılarak büyük hasta kohortlarında ve çeşitli deneylerde splicing düzenlemesini çalışmayı mümkün kılıyor. Genel okuyucu için ana mesaj şudur: genlerin nasıl kesilip yapıştırıldığına dair desenler hücrenin gizli kontrol sistemleri hakkında zengin bilgi taşır ve bu desenlerin çözülmesi yeni kanser sürücüleri ortaya çıkarabilir, prognozu iyileştirebilir ve daha hassas tedaviler arayışına rehberlik edebilir.
Atıf: Anglada-Girotto, M., Segura-Morales, C., Moakley, D.F. et al. Exon inclusion signatures enable accurate estimation of splicing factor activity. Nat Commun 17, 1994 (2026). https://doi.org/10.1038/s41467-026-69642-3
Anahtar kelimeler: RNA ekzon kesme (splicing), splice faktörleri, kanser genomikleri, transkriptomik, protein aktivitesi çıkarımı