Clear Sky Science · tr
LOAd703 kaynaklı tümör mikroçevresi gen mühendisliği ile atezolizumab kombinasyonu metastatik malign melanomda: Faz I/II çalışması
Bu yeni melanom çalışması neden önemli
Günümüzün güçlü immünoterapilerine artık yanıt vermeyen ileri evre deri melanomu olan kişiler için tedavi seçenekleri sınırlı ve sıkça zorlu oluyor. Bu çalışma başka bir fikri test ediyor: tümörlere doğrudan enjekte edilen gen mühendisliğine tabi bir virüsün, mevcut bir bağışıklık güçlendirici ilaçla birlikte kullanılarak vücudun savunmasını uyandırıp kanseri yeniden kontrol altına alıp alamayacağını. Erken sonuçlar bu yaklaşımın güvenle uygulanabileceğini ve standart tedaviye dirençli hastaların anlamlı bir bölümünde fayda sağlayabileceğini gösteriyor.
Tedaviyi alt eden inatçı bir deri kanseri
Melanom, Batı ülkelerinde en sık görülen ciddi deri kanserlerinden biridir ve son on yıllarda insidansı hızla artmıştır. T hücreleri üzerindeki frenleri kaldıran modern immün kontrol noktası ilaçları sonuçları dönüştürdü; ileri melanomlu hastalarda beş yıllık sağkalım oranını yaklaşık yarıya kadar yükseltti. Yine de birçok tümör sonunda yanıt vermeyi bırakıyor. Çoğu zaman bu dirençli kanserler, bağışıklık hücrelerini dışarıda tutan veya işlevlerini baskılayan “soğuk” bir hücre ve molekül çevresiyle sarılıdır. T hücrelerinin tekrar kanseri tanıyıp saldırabilmesi için bu tümör mikroçevresini yeniden kablolaştırmanın yollarını bulmak büyük bir araştırma önceliğidir.
Tümörün çevresini yeniden programlamak üzere tasarlanmış bir virüs
Burada test edilen tedavi LOAd703 adını taşıyan modifiye bir adenovirüstür—soğuk algınlığı virüsleri ailesine ait bir tür—ve iki işi yapmak üzere mühendislik edilmiştir. Birincisi, tümör hücrelerinde çoğalmayı ve onları yok etmeyi tercih eder; bu strateji onkolitik viroterapi olarak bilinir. İkincisi, enfekte hücrelerde iki güçlü immün uyarıcı sinyalin genetik talimatlarını taşır. Bu sinyaller CD40L ve 4‑1BBL, profesyonel bağışıklık gözcüleri (dendritik hücreler) olgunlaşmasına ve tümör parçacıklarını sunmasına yardımcı olur; ayrıca kanserle savaşan T hücrelerini ve doğal öldürücü hücreleri güçlendirir ve genişletir. Çalışmadaki hastalar üç haftada bir bir veya daha fazla tümöre doğrudan LOAd703 enjeksiyonu aldılar ve aynı zamanda damar yoluyla verilen, T hücreler üzerindeki PD‑L1 frenini engelleyen yerleşik bir antikor ilacı olan atezolizumab verildi. Umut, virüsün tümörleri vücut içi aşı fabrikalarına çevirirken antikorun yeniden canlandırılmış T hücrelerini etkin tutmasıydı.
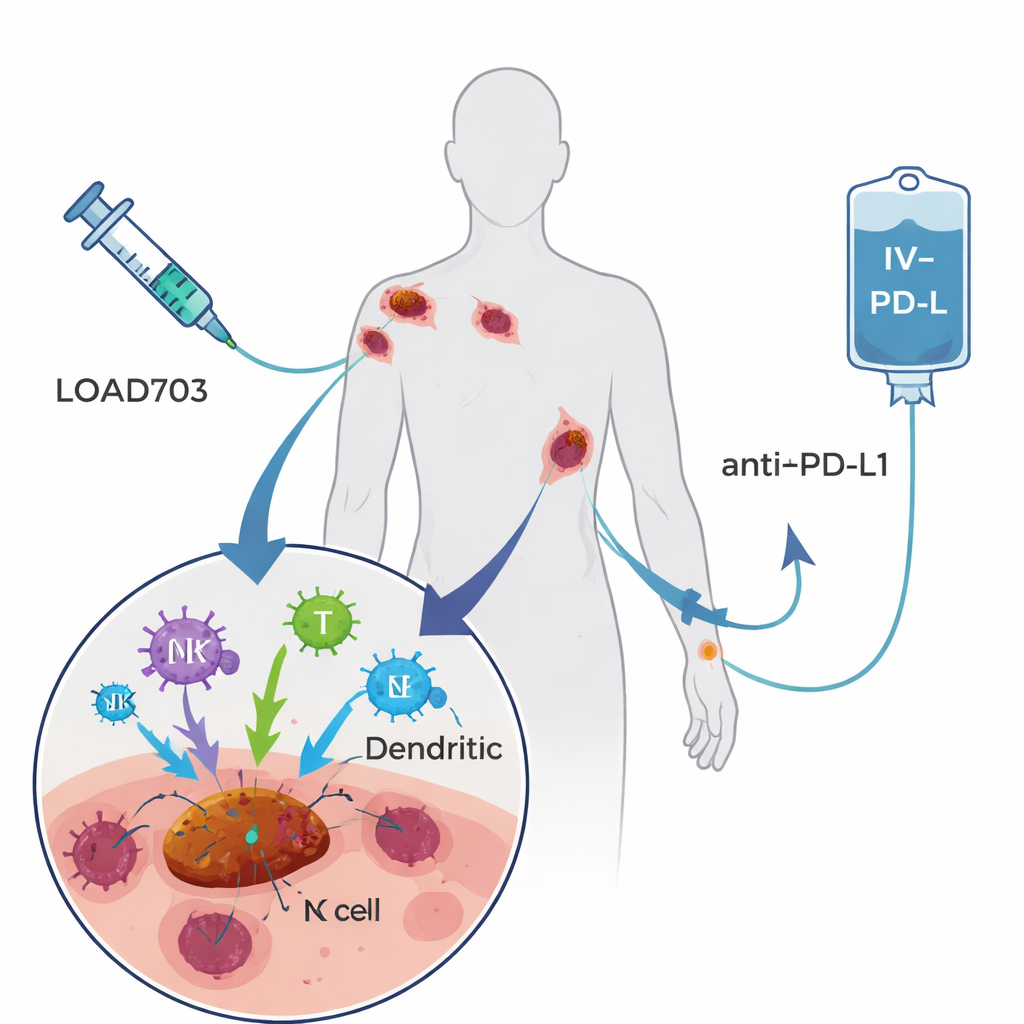
Kim tedavi edildi ve nasıl sonuç aldılar
Faz I/II çalışmaya en az bir önceki PD‑1 blokaj tedavisine rağmen açıkça ilerleme gösteren evre IV melanomlu 24 kişi alındı; birçoğu birkaç farklı immünoterapi ve hedefe yönelik ilaç hattı almıştı. İki farklı virüs doz seviyesi test edildi. Genel olarak kombinasyon iyi tolere edildi. Virüsle ilişkili en yaygın yan etkiler—ateş, titremeler, bulantı ve grip benzeri belirtiler—çoğunlukla hafif ve geçiciydi. Sadece iki hastada daha yüksek dozda daha ciddi ama geri döndürülebilir reaksiyonlar görüldü ve hiç kimse virüse bağlı sorunlar nedeniyle tedaviyi durdurmak zorunda kalmadı. Araştırmacılar tümör yanıtlarını incelediklerinde dört hastada (%17) ölçülebilir tümör küçülmesi görüldü ve yarıdan fazlasında bir süre için en az stabil hastalık vardı. Çalışmaya girişten iki yıl sonra katılımcıların yaklaşık yarısı hâlâ hayattaydı; bunların arasında tedaviyi bitirdikten sonra uzun süreli kontrol veya tüm tespit edilebilir hastalığın tamamen kaybolduğu görülenler de vardı.
Bağışıklık sisteminin yeniden devreye girdiğine dair işaretler
Tümörlerin ve kan dolaşımının içinde neler olduğunu görmek için ekip tedavi öncesi ve başladıktan yaklaşık dokuz hafta sonra alınan doku biyopsileri ve kan örneklerini analiz etti. Enjekte edilen tümörlerde, aktifleşmiş T hücreleri ve doğal öldürücü hücreleri belirten markörler dahil olmak üzere tip 1 immün yanıtlarla ilişkili genlerin daha yüksek aktivitesi ve bu hücrelerin çevre kan damarlarından tümörlere girmesine yardımcı olan moleküller gözlendi. T hücrelerine tümör parçacıklarının sunulduğu süreç olan antijen sunumuyla ilişkili işaretler de arttı; bu durum viral terapinin tümör mikroçevresini baskılayıcıdan daha immün‑dostu bir hale getirdiğini öne sürüyor. Kanda, PD‑L1 dahil birkaç immünle ilişkili protein tedaviden sonra yükseldi; bu, immün yolakların geniş çaplı bir aktivasyonuyla tutarlı. Daha uzun yaşayan hastalar genellikle güçlü T hücre fonksiyonu ve antiviral korumayla ilişkilendirilen gen desenleri gösterirken, daha kısa sağkalım gösterenlerde baskılayıcı hücre tipleri ve doku yeniden şekillendirme sinyalleriyle ilişkili desenler görüldü.
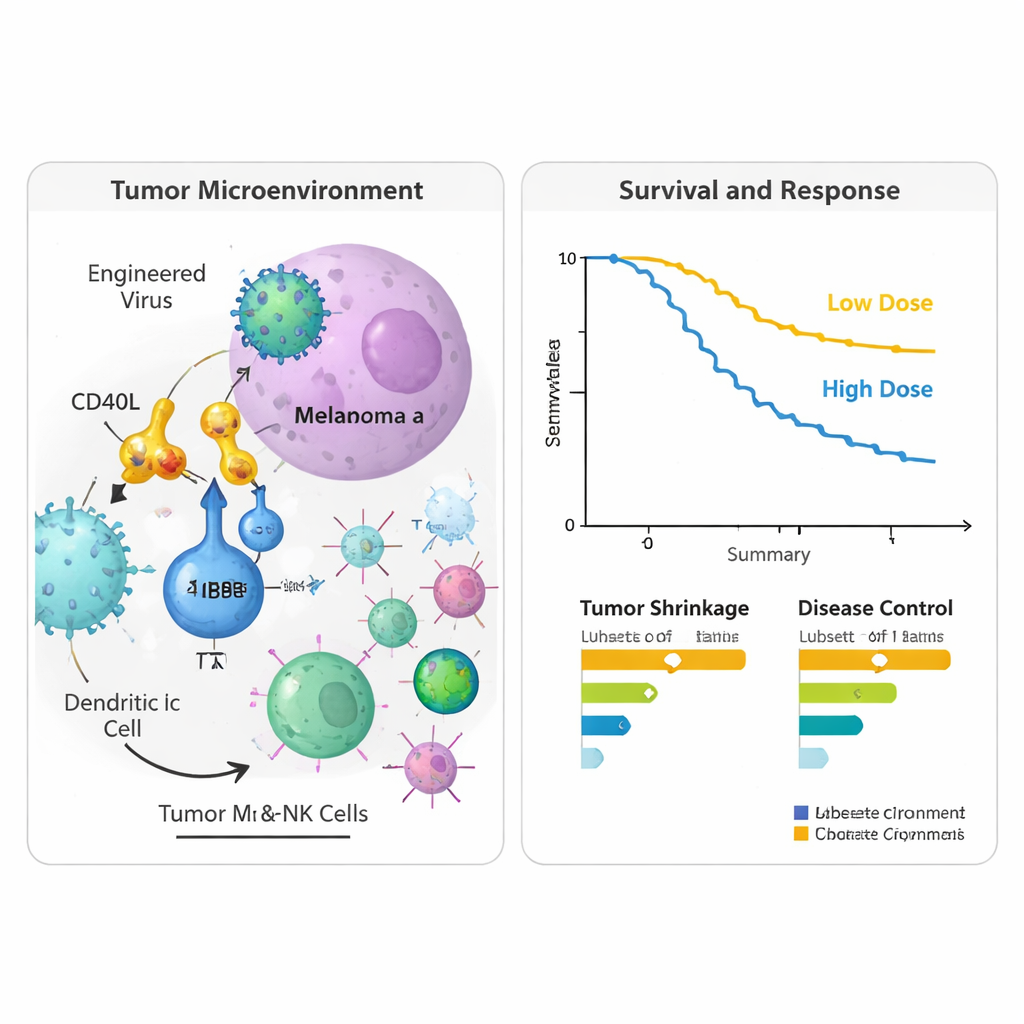
Bu, gelecekteki bakım için ne anlama gelebilir
Bu küçük, karşılaştırma grubu olmayan tek kollu bir çalışmaydı; bu yüzden sağkalım ve yanıt rakamları dikkatle yorumlanmalıdır. Yine de iyi tolere edilebilirlik, tümörlerde immün aktivasyon ve ağır ile tedavi edilmiş hastalardaki teşvik edici hastalık kontrolü kombinasyonu, LOAd703 gibi gen mühendisliği onkolitik virüslerin melanomu kontrol noktası blokajına yeniden duyarlı hale getirmeye yardımcı olabileceği veya tek başına tümörleri kontrol altında tutabileceği fikrini destekliyor. Sonuçlar, hangi hastaların en çok fayda gördüğünü ve bu stratejiyi melanom tedavisine en iyi nasıl entegre edeceğimizi netleştirmek için virüsü ek immün‑hedefleyen ilaçlarla eşleştiren daha büyük, kontrollü çalışmaları destekliyor.
Atıf: Hamid, O., Ekström-Rydén, V., Mehmi, I. et al. LOAd703-induced tumor microenvironment gene engineering in combination with atezolizumab in metastatic malignant melanoma: a phase I/II trial. Nat Commun 17, 1760 (2026). https://doi.org/10.1038/s41467-026-69629-0
Anahtar kelimeler: melanom, immünoterapi, onkolitik virüs, tümör mikroçevresi, kontrol noktası inhibitör direnci