Clear Sky Science · tr
İlaç-kafesli ilaçlar, nitroksit oksit ve anesteziklerin fotokatalitik çift serbestleşmesini sağlayarak antibakteriyel analjezi sunuyor
Mikroplarla ve ağrıyla aynı anda mücadele
Bakteriyel enfeksiyonlar yalnızca sağlığımızı tehdit etmekle kalmaz; aynı zamanda çok şiddetli ağrıya da yol açar. Standart tedaviler genellikle mikropları hedefler fakat hastaları ayrı ağrı kesicilere bağımlı bırakır; bu ilaçlar hızla etkisini kaybedebilir veya yan etkilere neden olabilir. Bu çalışma, bakterileri öldürmeyi ve ağrıyı tek, koordine adımda hafifletmeyi amaçlayan ışık kontrollü bir ilacı tanıtıyor; bu, daha akıllı ve daha konforlu enfeksiyon bakımına dair bir önizleme sunuyor.
İki işlevli ilaç fikri
Araştırmacılar yaklaşımlarını, ciltte ve sinirlerde uyuşturma için kullanılan tanıdık bir lokal anestezik olan tetrakain etrafında kurdular. Güçlü antibakteriyel ve antiinflamatuar etkileriyle bilinen küçük bir gaz molekülü nitroksit oksiti (azot oksit) tetrakaina kimyasal olarak bağladılar. Bu, tetiklenene kadar büyük ölçüde etkisiz kalan TTC-NO adlı bir “proilaç” oluşturdu. TTC-NO daha sonra su bazlı ortamlar (kan veya doku sıvısı gibi) içinde hareket edebilen, ışığa duyarlı bir yardımcı molekül ile birlikte polimer kabarcıklar olan mikellere paketlendi. 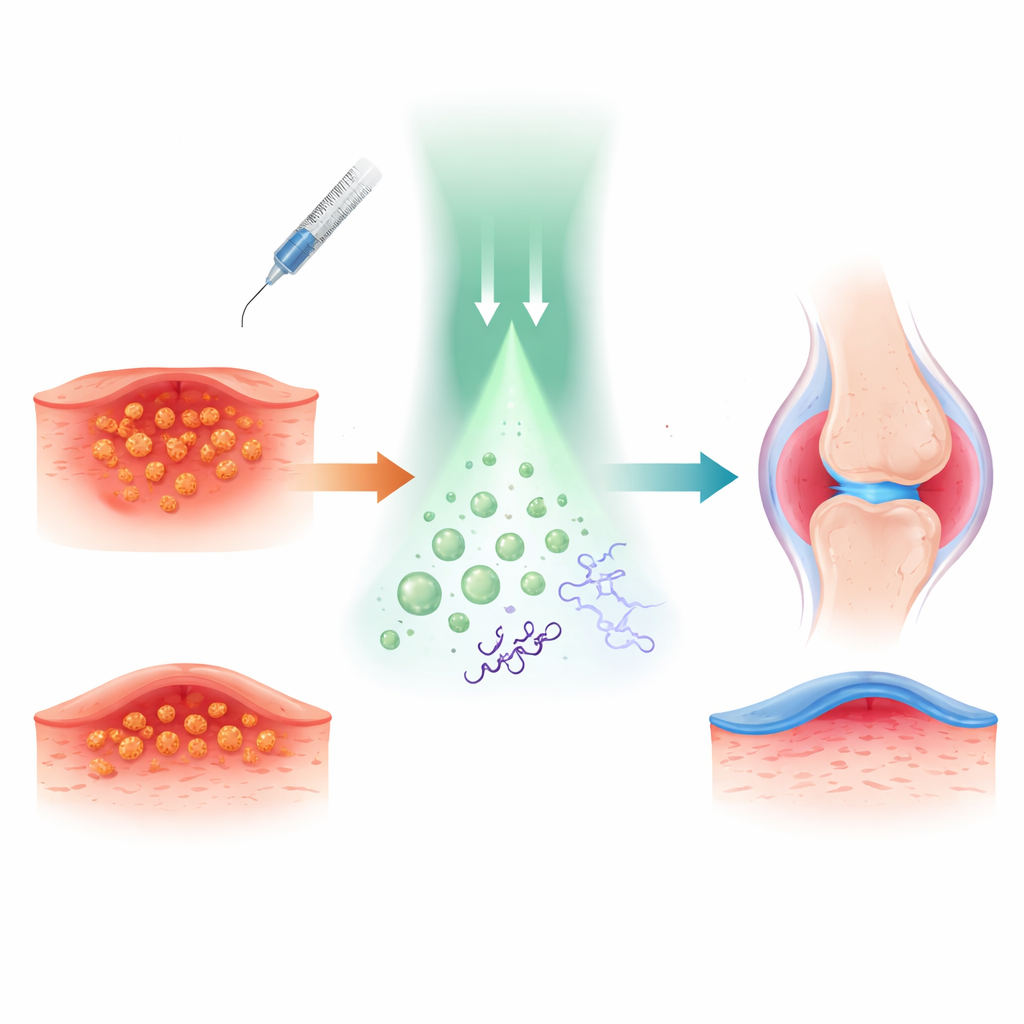
İlacı nazik bir ışıkla etkinleştirmek
Bu ışık anahtarının nasıl çalıştığını anlamak için ekip kimyayı çözeltide inceledi. Yeşil ışıkla aydınlatıldığında iridyum bazlı bir fotokatalizörün TTC-NO’ya elektron transfer edebildiğini gösterdiler. Bu, belirli bir bağı zayıflatarak azot oksidin serbest kalmasına ve tetrakainin aktif haline dönmesine neden oldu. Spektroskopi ve kromatografi kullanılarak yapılan ölçümler, TTC-NO’nun bu koşullar altında neredeyse tamamen tetrakain ve azot okside dönüştüğünü, karanlıkta ise esasen değişmeden kaldığını doğruladı. İki bileşen mikellere kapsüllenince parçacıklar yaklaşık 80 nanometre çapında kararlı kaldı ve yalnızca ışınlandığında içeriklerini serbest bıraktı; bu da “ilaç-kafesli ilaç” konseptinin vücut dışından ışıkla kontrol edilebileceğini gösterdi.
Enfekte yaraların daha hızlı iyileşmesine yardımcı olmak
Ekip daha sonra, kasıtlı olarak metisiline dirençli Staphylococcus aureus (MRSA) ile enfekte edilmiş deri yaralarına sahip fareler üzerinde çalıştı; bu hastane kaynaklı sorunlu bir mikroptur. Bazı yaralara bir antibiyotik veya büyüme faktörü gibi standart tedaviler uygulandı; diğerleri ise TTC-NO mikelleri ile ışıkla veya ışık olmadan tedavi edildi. Işık açıldığında TTC-NO sistemi bakteri sayısını hızla azalttı, iltihabı yatıştırdı, yeni damar büyümesini teşvik etti ve kolajen birikimini artırdı; bunların tümü düzgün onarım için elzemdi. Bu şekilde tedavi edilen yaralar, yalnızca tetrakain verilen veya karanlıkta tutulan mikellere kıyasla daha hızlı ve daha eksiksiz kapandı ve etkinliği ön cephe antibiyotiklerinden biriyle karşılaştırılabilirdi. Önemli olarak, güvenlik kontrolleri organlarda veya kan kimyasında belirgin bir hasar göstermedi.
Ağrıyı hafifletme ve sinir sinyallerini susturma
Enfeksiyon ve doku yaralanması ağrı yollarını güçlü şekilde aktive ettiğinden, bilim insanları aynı yara modelinde ağrı ilişkili davranışları dikkatle ölçtüler. Geleneksel tetrakain ağrı yanıtını tetiklemek için gereken kuvveti kısa süreliğine artırdı ancak birkaç saat içinde etkisini kaybetti. Buna karşılık, ışıkla aktive edilen TTC-NO mikelleri 12 saate kadar rahatlama sağladı. Omurilik yakınındaki sinir kümelerinin mikroskobik incelemeleri ve beynin duyu korteksindeki aktivite kayıtları, birleşik tedavinin ağrı algılayan nöronların ateşlenmesini saf tetrakainin etkisini kaybetmesinden çok sonra bile azalttığını gösterdi. Ek deneyler, ekstra etkinin yalnızca sinirleri uyuşturmaktan değil, azot oksidin bakteriyel yükü ve iltihabı azaltmasından kaynaklandığını öne sürdü.
Ağrılı enfekte eklemleri korumak
Araştırmacılar sistemi ayrıca diz eklemi içinde şişlik, kemik kaybı ve yoğun ağrıya neden olan şiddetli bir MRSA enfeksiyonu olan septik artritisi olan farelerde test ettiler. Işıkla aktive edilen TTC-NO mikelleri eklem genişliğini azalttı, bakteri sayısını kesti ve yüksek çözünürlüklü taramalarda görüldüğü üzere kemik yapısını korudu. Kanda zararlı inflamatuar molekül düzeyleri düştü, koruyucu sinyal molekülleri ise yükseldi. Davranışsal olarak, tedavi edilen fareler etkilenen paterna daha yüksek mekanik baskıya dayanabildi ve açık bir alanda daha özgürce hareket etti; bu da yine tetrakain tek başına verilen tedavilerden daha uzun süreli rahatlama gösterdi. Sinir ve beyin ölçümleri bu davranışsal kazanımları yansıttı ve belirgin lokal veya sistemik toksisite olmaksızın ağrı yollarının geniş çaplı şekilde baskılandığını gösterdi. 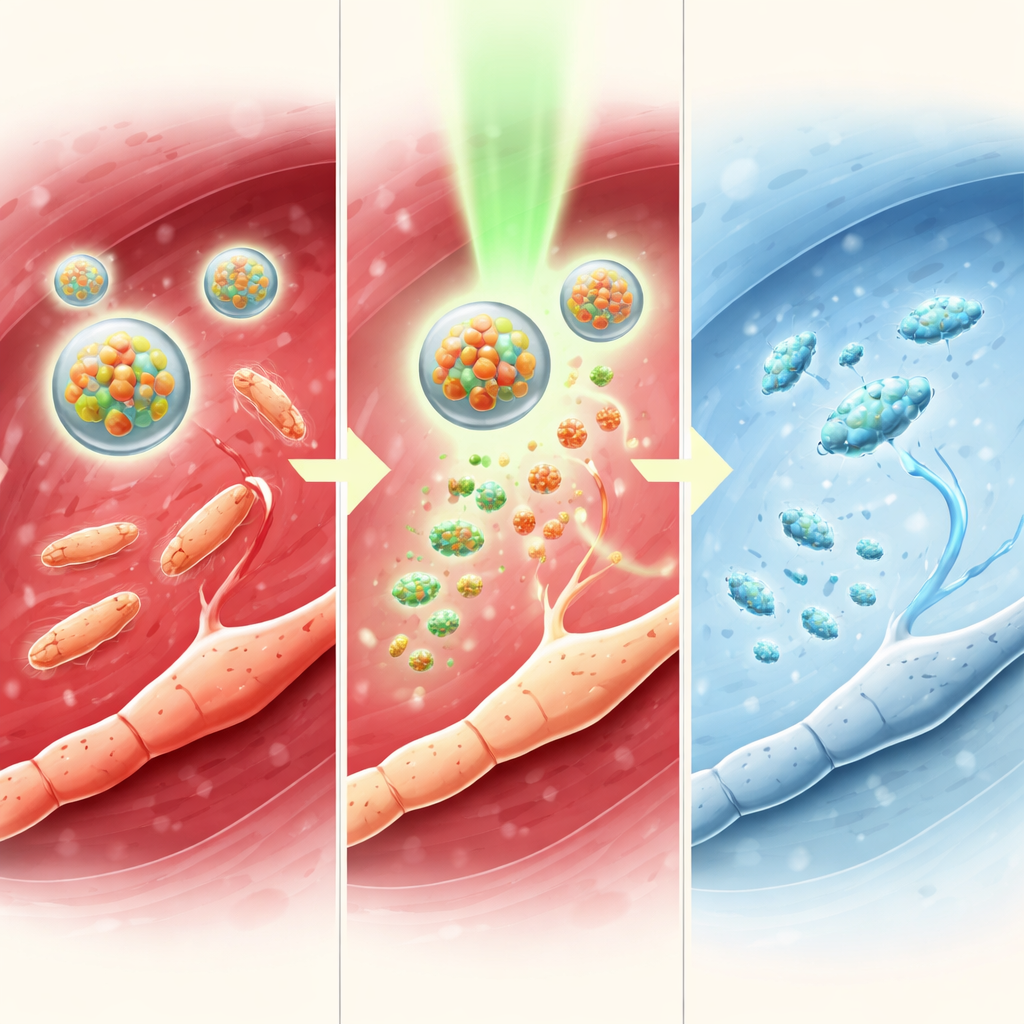
Bu hastalar için ne anlama gelebilir
Toplu olarak bakıldığında, çalışma inatçı bakteriyel enfeksiyonları temizleyebilen ve ilişkili ağrıyı önemli ölçüde azaltabilen tek bir, ışıkla aktive edilen nanosistem gösteriyor. Bir anesteziği kimyasal olarak azot oksit salan bir yapının içine “kafesleyip” mikellere paketleyerek, yazarlar hafif görünür ışık kullanarak iki yararlı ajanın isteğe bağlı, lokal salımını başarıyor. Deri yaraları ve eklem enfeksiyonlarının hayvan modellerinde bu tasarım iyileşmeyi hızlandırıyor ve geleneksel bir lokal anesteziğin sunabildiğinden daha uzun süreli ağrı giderimi sağlıyor. İnsan kullanımı öncesinde hâlâ çok sayıda test gerekse de, çalışma akıllı, anahtarlanabilir ilaçların bir gün enfeksiyon tedavilerini hem daha etkili hem de daha konforlu hale getirebileceğini vurguluyor.
Atıf: Zhang, J., Gan, G., Cao, C. et al. Drug-caged drugs enable photocatalytic dual decaging of nitric oxide and anesthetics for antibacterial analgesia. Nat Commun 17, 2843 (2026). https://doi.org/10.1038/s41467-026-69624-5
Anahtar kelimeler: azot oksit tedavisi, ışıkla aktive edilen ilaçlar, antibakteriyel analjezi, nanotıp, MRSA enfeksiyonları