Clear Sky Science · tr
Dialumene’in izole edilebilir radikal katyonu ve dikasyonu
Bu alüminyum hikâyesi neden önemli
Kemistler, palladyum veya platinyum gibi değerli elementlerin üstlendiği karmaşık görevleri daha ucuz ve daha bol bulunan metallere devretmenin yollarını sürekli araştırıyor. Bu çalışma, soda kutuları ve uçaklarla daha çok bilinen alüminyumun, küçük elektrik anahtarları gibi davranan sıra dışı reaktif formlara kışkırtılabileceğini gösteriyor. Bu egzotik alüminyum türlerini anlamak ve kontrol etmek, sonunda daha temiz kimyasal süreçler ve malzemeler için yeni katalizörlerin geliştirilmesine yardımcı olabilir.
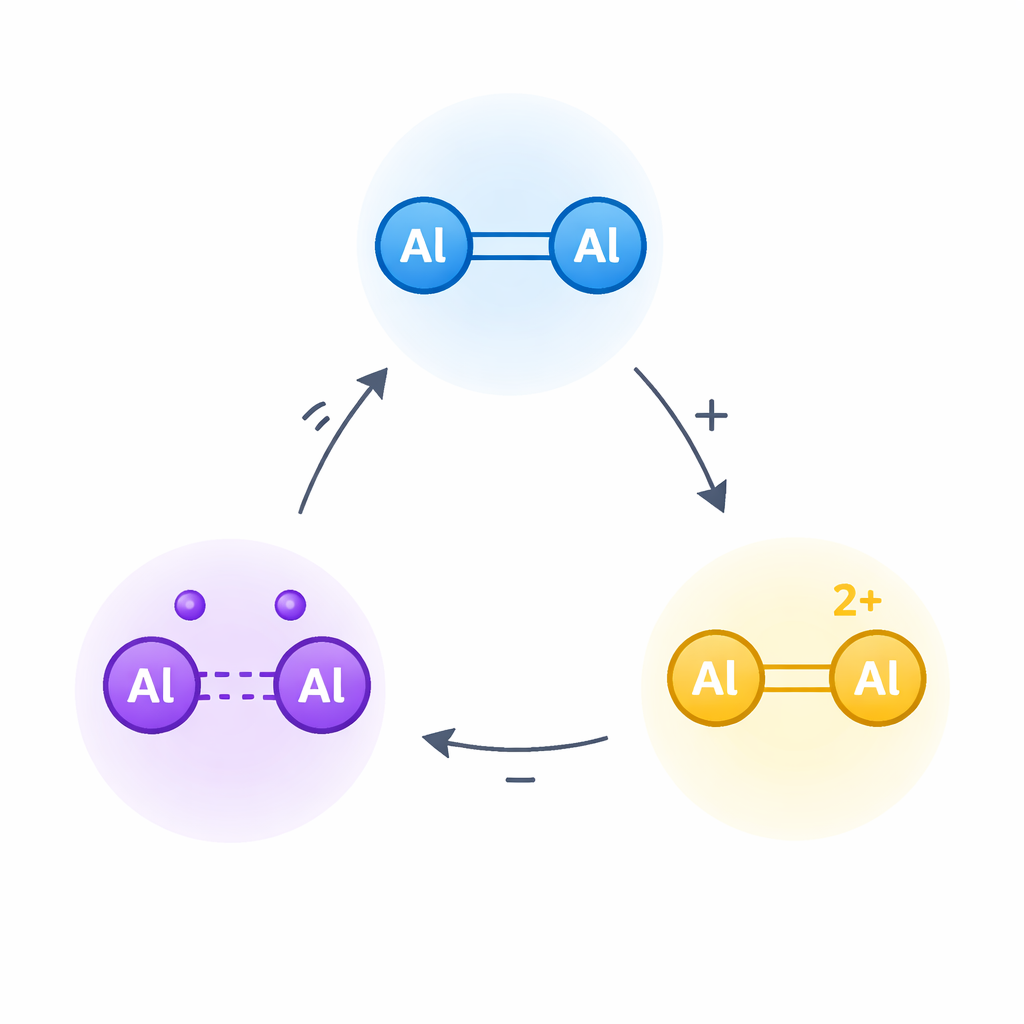
Aşina bir bağı elektronik bir anahtara dönüştürmek
Çalışma, iki alüminyum atomunun karbon–karbon çift bağlarına benzeyen bir çift bağ paylaştığı bir molekül olan dialumene üzerine odaklanıyor. Organik moleküllerde bu tür çift bağlar adım adım yükseltgenerek önce radikal katyonlar sonra da dikasyonlar verebilir — elektro-kimya ve malzeme biliminde birçok reaksiyonun temelini oluşturan yüksek yüklü, yüksek reaktif formlar. Yazarlar, alüminyumun güçlü elektron çeken bir element olmasına ve bu tür yüklü türlerin olağanüstü derecede kararsız olması beklenmesine rağmen, dialumene’deki alüminyum–alüminyum çift bağının benzer iki adımlı bir yükseltgemeye zorlanıp zorlanamayacağını sordular.
Koruyucu bir moleküler çerçeve tasarlamak
Bu reaktiviteyi dizginlemek için ekip, dialumene etrafına hacimli silikon bazlı gruplar ve güçlü elektron verici “karben” ligandları yerleştirdi. Bunlar yumuşak zırh ve elektronik yastık gibi davranır: hassas alüminyum–alüminyum çekirdeğini istenmeyen reaksiyonlardan korur ve gerektiğinde elektron yoğunluğu sağlar. Nötr dialumene (1 olarak adlandırılmış) başlangıç noktasından, dikkatle seçilmiş oksitleyicilerle önce bir elektronu sonra ikinciyi uzaklaştırdılar; böylece alüminyum merkezli bir radikal katyon (2) ve ardından bir dikasyon (3) oluşturdular. X-ışını kristalografisi, elektronlar uzaklaştırıldıkça alüminyum–alüminyum bağının nasıl kademeli olarak uzayıp karakter değiştirdiğine dair üç durumu da gösteren anlık görüntüler sağladı.
Gerçek bir üç-yollu redoks çevriminin kanıtlanması
Anahtar ölçümler, radikal katyonun gerçekten etraftaki ligandlarda değil, iki alüminyum atomunun arasında merkezlenen eşleşmemiş bir elektrona sahip olduğunu doğruladı. Elektron paramanyetik rezonans spektroskopisi, her iki alüminyum merkezinin paylaştığı tek bir elektrona uygun net bir sinyal gösterdi. Hesaplamalı çalışmalar bu görüntüyü destekleyerek, kalan bağ elektronunun büyük ölçüde bir alüminyum–alüminyum orbitalinde yer aldığını işaret etti. İkinci elektron uzaklaştırılarak dikasyon oluşturulduğunda bağ zayıflayıp tek bağa yaklaşır ve pozitif yük alüminyum çiftinde birikir. Önemli olarak, araştırmacılar bu değişimlerin geri döndürülebilir olduğunu gösterdiler: bir indirgenle elektronların geri verilmesi önce radikal katyonu ardından orijinal dialumeneyi yeniden oluşturuyor ve nötr ile çift yüklü formların karıştırılması komproportionasyon yoluyla radikal katyonu veriyor. Birlikte bu reaksiyonlar basit bir alüminyum–alüminyum ünitesinde sağlam, izole edilebilir üç durumlu bir redoks çevrimi olduğunu gösteriyor.
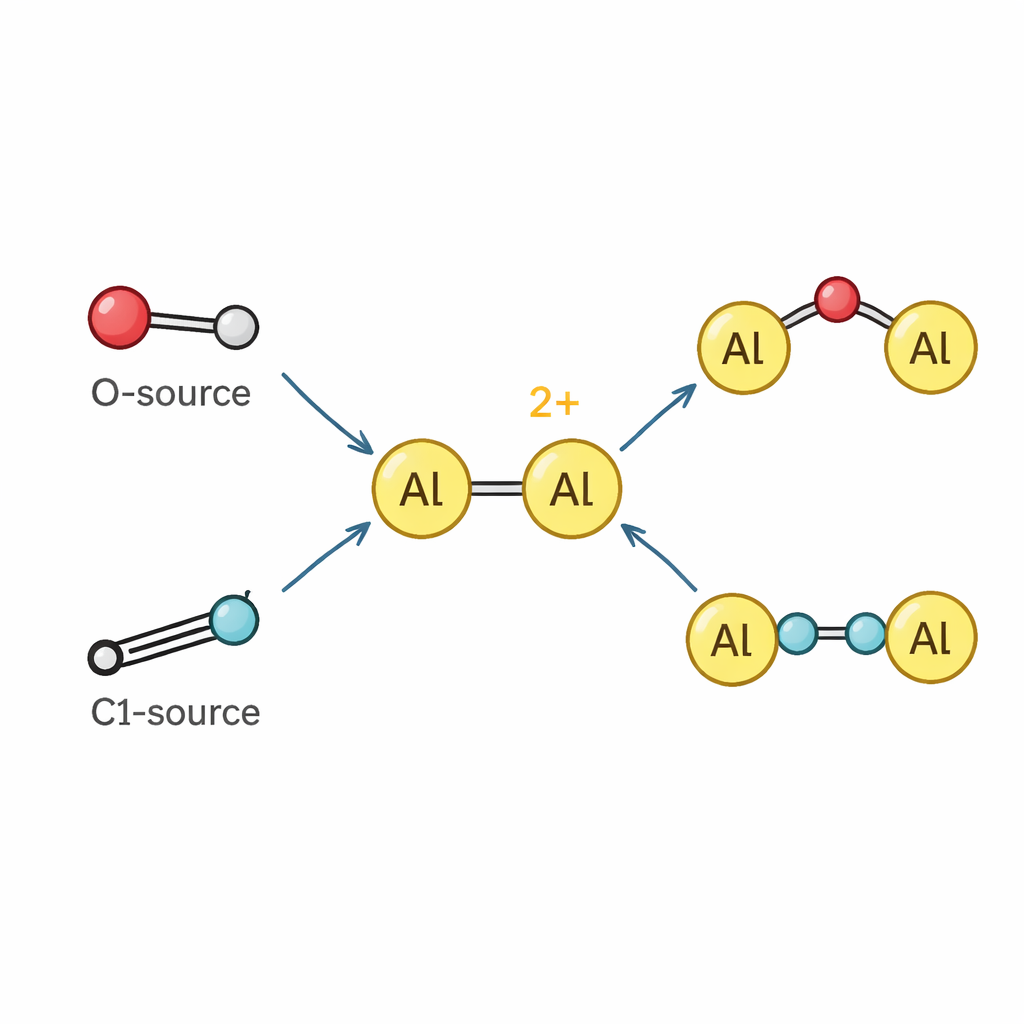
Alüminyumu geçiş metali gibi davranmaya zorlamak
Dikasyon bulunduğunda ekip, bunun diğer moleküllerle nasıl reaksiyona girdiğini araştırdı. Alüminyum atomları güçlü biçimde elektron fakiri olduğundan dikasyon güçlü bir Lewis asidi gibi davranıyor; piridin ve benzeri bazik ortaklarla kolayca bağlanarak yeni dialüminyum kompleksleri oluşturuyor. Basit bağlanmanın ötesinde, dikasyon kimyasal bağları parçalayabilir ve içine yerleşebilir. N2O ve piridin N-oksitten oksijen atomlarını çekerek iki alüminyum merkezi arasında bir oksijen atomunun köprü kurduğu veya kısa bir alüminyum–oksijen–silikon zincirine dahil olduğu stabil türler oluşturuyor; bu, zeolit çerçevesinin küçük bir parçacığını anımsatıyor. Ayrıca isosiyanidler — bir karbon–azot birimi olarak kullanılan küçük yapı taşları — ile etkileşerek bunları daha uzun N–C–C–N parçacıklarına diker; bu parçalar iki alüminyum atomu arasında uzanıyor ve ana grup katyonu tarafından yönlendirilen nadir bir isosiyanid “homologasyon” örneğini gösteriyor.
İleriye dönük anlamı
Günlük terimlerle, araştırmacılar bir alüminyum–alüminyum bağını nötr, tek yüklü ve çift yüklü olmak üzere her birinin farklı şekil ve reaktiflik gösterdiği kontrol edilebilir üç konumlu bir elektronik anahtara dönüştürdüler. Çift yüklü versiyon özellikle çok yönlü; genellikle daha pahalı geçiş metalleriyle ilişkilendirilen şekillerde diğer moleküllerden elektron ve küçük parçacıklar çekiyor. Böyle bir davranışın alüminyumla mümkün olduğunu ve farklı durumların güvenilir biçimde birbirine dönüştürülebileceğini göstererek, bu çalışma Dünya’nın en bol metallerinden birinden inşa edilebilecek yeni, sürdürülebilir katalizörler ve fonksiyonel malzemeler tasarlama yolunu aralıyor.
Atıf: Liu, X., Kostenko, A., Körber, E. et al. Isolable radical cation and dication of dialumene. Nat Commun 17, 1937 (2026). https://doi.org/10.1038/s41467-026-69607-6
Anahtar kelimeler: alüminyum katalizi, redoks-geçişli moleküller, ana grup kimyası, radikal katyonlar, küçük-molekül aktivasyonu