Clear Sky Science · tr
Pirimidinerjik kalsiyum sinyallemesi böbrek hastalığında tübüler metabolizmayı fibrozise bağlıyor
Neden böbrek skarı önemli?
Kronik böbrek hastalığı dünyada yüz milyonlarca insanı sessizce etkiler ve sıklıkla böbreklerin skarlaşması ve sertleşmesiyle sonuçlanır. Bu skarlaşma —fibrozis— bir kez yerleştiğinde kaybedilen böbrek işlevini geri kazanmak zordur. Yine de hekimlerin fibrozisi özel olarak durduracak ilaçları yok. Bu çalışma temel ama kritik bir soruyu soruyor: böbreğin filtreleme tüplerine kısa süreli verilen zarar nasıl kademeli olarak kalıcı skar dokusuna dönüşür ve bu zinciri kesmek böbrek yetmezliğini yavaşlatır veya önleyebilir mi?
Yoğun çalışan böbrek tüpleri ve onların saklı kimyası
Böbreğin proksimal tübülleri kandan filtrelenen su ve besinlerin çoğunu geri alan mikroskobik işçi hücrelerdir. Bu işi yürütmek için kimyaları olağandışın etkin çalışır. Fare böbreklerinden alınan tek hücre gen ifadesi verilerini analiz ederek araştırmacılar, bu tübül hücrelerinin pirimidinleri işleyen genler bakımından özellikle zengin olduğunu buldular; pirimidinler normalde DNA ve RNA inşası ve onarımına yardımcı olan küçük molekül ailesidir. Yaralanmış tübüllerde, bir “salvaj” yolundaki enzim sitidin deaminaz belirgin şekilde artmıştı; bu da hasarlı hücrelerin UDP gibi enerji açısından zengin bazı yapı taşlarını korumak için pirimidin kullanımını yeniden düzenlediğini düşündürüyordu.
Hasarlı hücrelerden yayılan sinyaller
Ekip insan tübül benzeri hücreleri kültürde kemoterapi benzeri toksinler veya yüksek folik asitle yaraladığında hücreler UDP’yi çevre sıvıya saldı. Gerçek fare böbreklerinde hasara maruz kalan dokuların boyanması, tübüllerde pirimidin işleyen enzimin yüksek düzeyde olduğunu ve komşu destek hücreleri olan fibroblastların uyanıp şekil değiştirdiğini gösterdi. Fibroblastlar normalde tübüller arasında sessizce durur; ancak aktive olduklarında çoğalır ve böbrek dokusunu kalınlaştırıp sertleştiren kolajen ve diğer lifleri döşemeye yardım ederler. Bu gözlemler basit bir fikri öne sürdü: yaralanmış tübüller komşu fibroblastların algılayabileceği kimyasal sıkıntı sinyalleri “döküyor” olabilir.
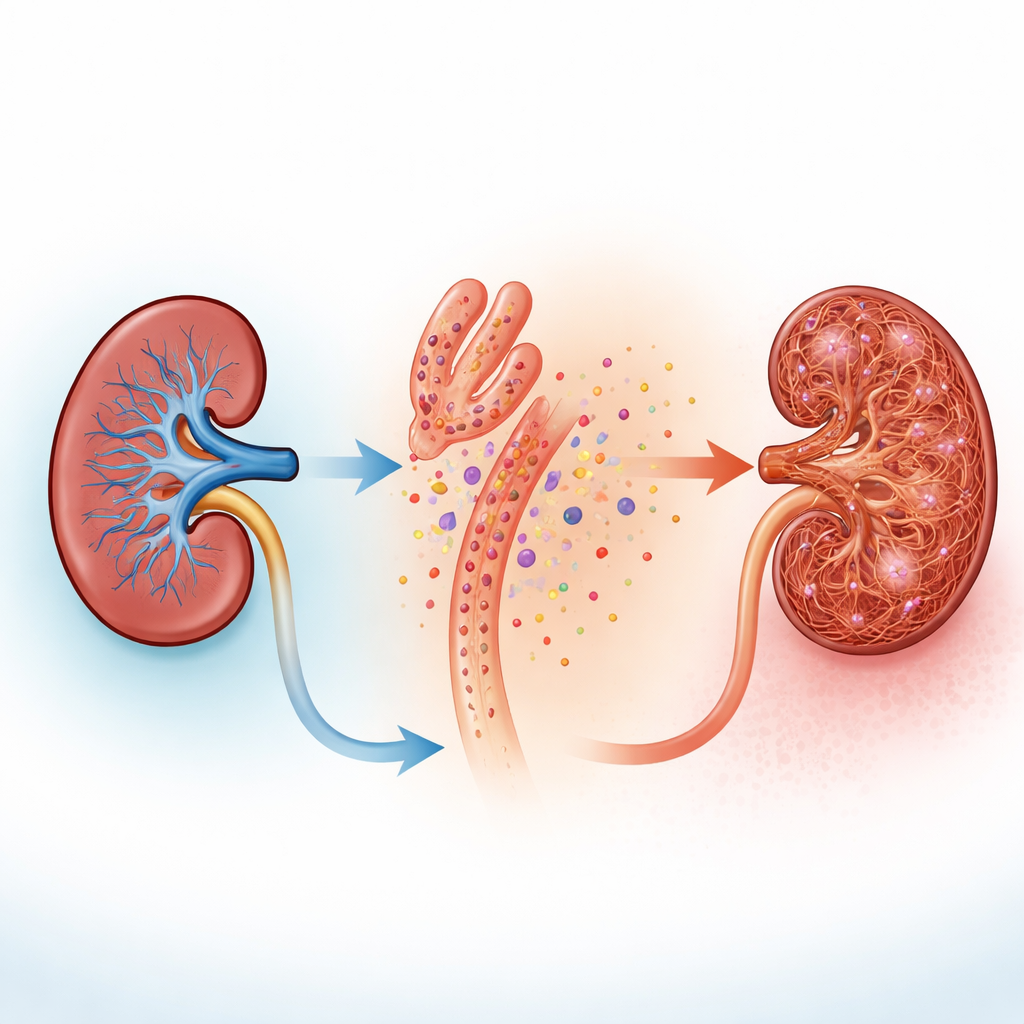
Fibroblastlar kalsiyum patlamalarıyla nasıl dinliyor
Fibroblastlardaki muhtemel “kulaklar” UDP’ye yanıt veren yüzey proteinleri olan P2Y6 reseptörleridir. Birkaç tek hücre veri setini tarayan yazarlar P2Y6’nın stromal hücrelerde göründüğünü ve kronik böbrek hastalığı fare modellerinde daha da yükseldiğini gördü. Tüm böbreklerde yapılan ölçümler iki farklı skar modeli de dahil olmak üzere P2Y6 düzeylerinde güçlü artışları doğruladı. Taze böbrek kesitlerinde ve hücre içi kalsiyum yükseldiğinde ışık veren şekilde tasarlanmış kültürlenmiş böbrek fibroblastlarında UDP veya P2Y6’yı aktive eden bir ilaç eklemek hızlı kalsiyum dalgalanmaları üretti. Bu flaşlar tübülleri saran uzun ince uzantılarda başladı, sonra hücre gövdesine yayıldı ve P2Y6 bloke edildiğinde veya kalsiyum kimyasal olarak bağlandığında kayboldu. Canlı farelerde yüksek çözünürlüklü intravital mikroskopi, tübüller etrafındaki fibroblastların sık, düzensiz kalsiyum etkinliği sergilediğini ve tübüller yaralandığında bu etkinliğin dramatik şekilde arttığını gösterdi; o sırada tübül hücreleri sessizleşiyordu.
Kısa sinyallerden kalıcı skarlara
Hücre içindeki kalsiyum patlamaları sadece havai fişek değildir; davranışı yeniden programlayabilirler. Kültürdeki fibroblastlar P2Y6’yı aktive eden bir bileşiğe maruz bırakıldığında daha hızlı çoğaldılar, daha kolay süründüler ve daha agresif bir “miyofibroblast” durumuyla ilişkilendirilen genleri açtılar. Bu genler doğrudan skar oluşumuna katkıda bulunan fibronektin, vimentin ve kolajen gibi proteinleri kodluyordu. P2Y6’yı bloke etmek veya kalsiyum yükselmelerini önlemek bu değişiklikleri sildi; reseptörün genini baskılamak yanıtı köreltti. Farelerde üreter tıkanıklığı ve folik asit nefropatisi olmak üzere iki farklı böbrek yaralanması aynı deseni gösterdi: yaralanmış böbreklerde daha çok çoğalan fibroblast, daha fazla miyofibroblast belirteci, daha fazla kolajen ve daha geniş fibrozis alanları vardı.
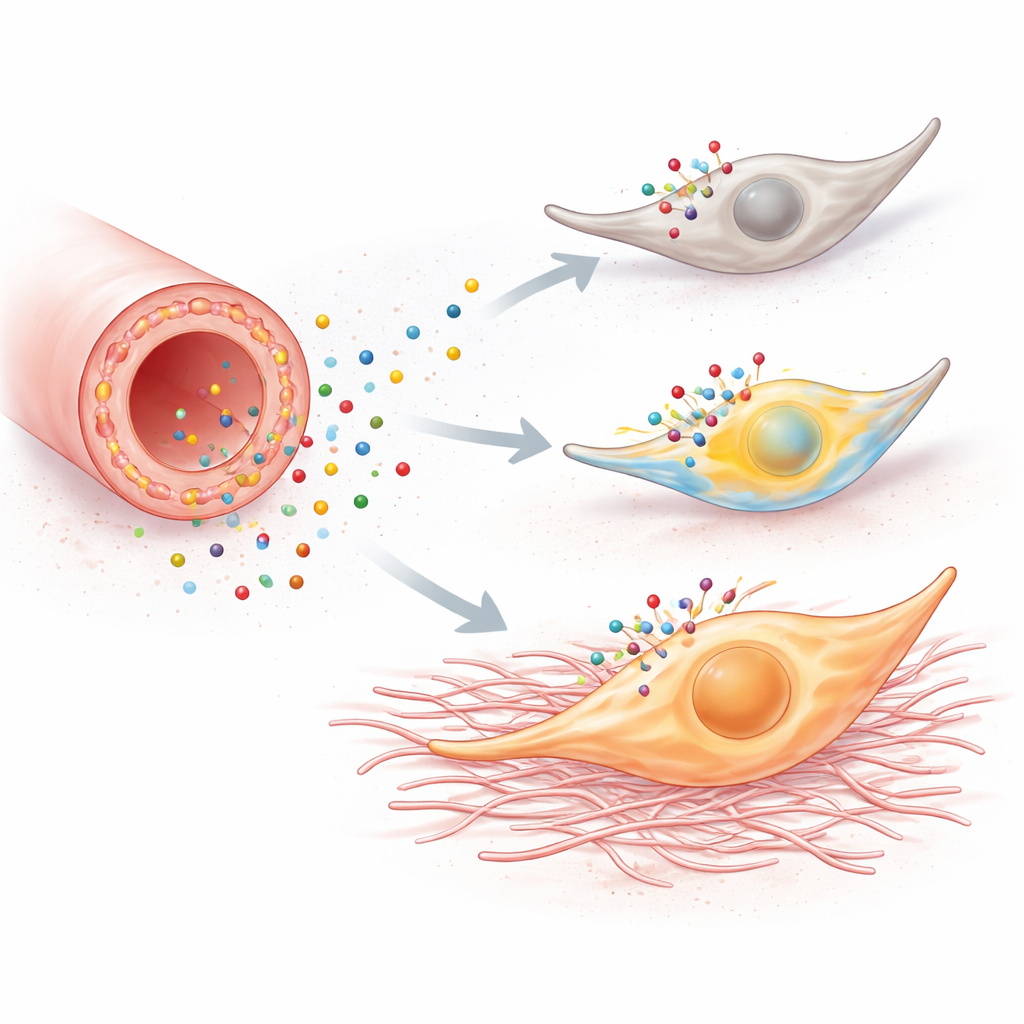
Zararlı sinyallemenin sesini kısmak
Bu yolun yalnızca var olduğunu değil gerçekten zararlı olduğunu test etmek için araştırmacılar P2Y6’yı ya genetik olarak ortadan kaldırdı ya da bir ilaçla bloke etti. Reseptörü olmayan fareler üreter tıkanıklığı veya folik asit hasarından sonra daha az böbrek fibrozisi geliştirdi: fibroblastları daha az çoğaldı, daha az fibröz matris biriktirdiler ve daha az inflamatuar hücre çektik. Kan testleri, bu genetik olarak eksik hayvanların böbrek filtreleme işlevini daha iyi koruduğunu da gösterdi. Normal farelere P2Y6'yı bloke eden bir bileşikle tedavi benzer koruma sağladı; fibroblastlarda kalsiyum etkinliğinin azalması ve skarın düşmesi dahil, ancak kan göstergelerindeki iyileşmeler daha değişkendi.
Gelecekteki tedaviler için anlamı nedir?
Birlikte alındığında, bu çalışma basit ama güçlü bir olay zincirini ortaya koyuyor. Böbrek tübül hücreleri zarar gördüğünde iç kimyalarını değiştirir ve UDP’yi çevre dokuya salar. Yakındaki fibroblastlar bu molekülü P2Y6 reseptörleriyle algılar, hücre içinde kalsiyum patlamalarıyla yanıt verir ve sonra skarlaşma moduna geçer—çoğalır, göç eder ve kolajen döşerler. Bu pirimidin temelli kalsiyum sinyallemesini, özellikle P2Y6 adımında kesmek, birden çok fare modelinde fibrozisi büyük ölçüde yumuşatır. Hastalar için bu, böbrekte seçici olarak P2Y6’yı bloke eden bileşiklerin günlük böbrek yaralanmaları ile kronik böbrek hastalığına yol açan yavaş, geri döndürülemez skarlaşma arasındaki bağı koparmaya yardımcı olabileceğini öne sürer.
Atıf: Figurek, A., Jankovic, N., Kollar, S. et al. Pyrimidinergic calcium signaling links tubular metabolism to fibrosis in kidney disease. Nat Commun 17, 3004 (2026). https://doi.org/10.1038/s41467-026-69602-x
Anahtar kelimeler: kronik böbrek hastalığı, renal fibrozis, fibroblast sinyallemesi, pirimidin metabolizması, P2Y6 reseptörü