Clear Sky Science · tr
Jeneratif difüzyon yapay zekâsı ve kontrastsız MRI ile glioma kan-beyin bariyeri durumunun kontrastsız belirlenmesi
Bu, beyin tümörü hastaları için neden önemli
Beyin tümörü olan kişiler rutin olarak MRI taramalarından geçer ve birçok hastaya doktorlar kan‑beyin bariyerinin zarar görüp görmediğini görmek için enjeksiyon yoluyla kontrast boya verilir. Bu bilgi cerrahi, radyasyon ve prognozu yönlendirir—ancak boyanın riskleri olabilir, süre ve maliyeti artırır ve her zaman erişilebilir değildir. Bu çalışma, rutin, boya içermeyen MRI görüntülerini okuyabilen ve eksik kontrast görüntülerini sanal olarak yeniden üreten bir yapay zekâ (YZ) sistemi sunar; böylece doktorlar herhangi bir kontrast ajan enjekte etmeden kan‑beyin bariyeri durumunu çıkarımlayabilir.
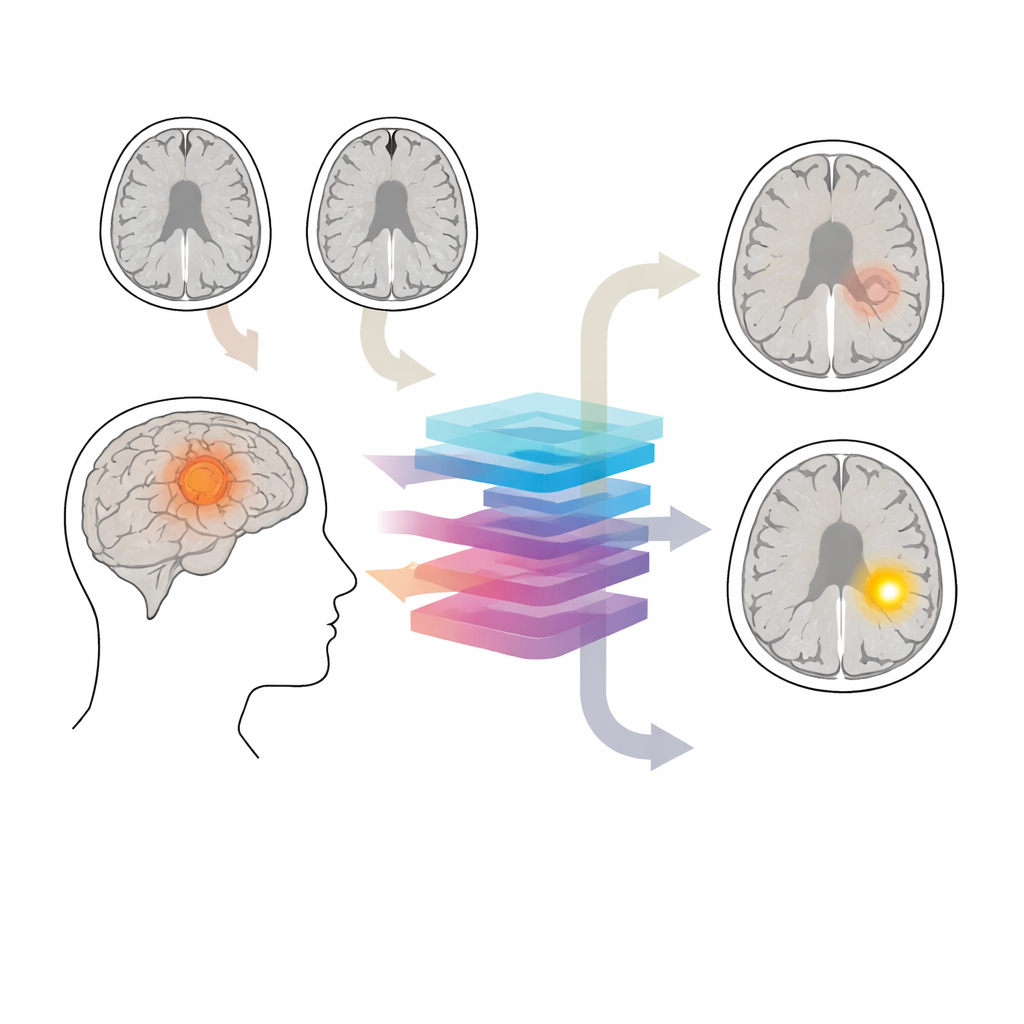
Beynin koruyucu nöbetçisi
Kan‑beyin bariyeri, beyindeki kan damarları etrafında mikroskobik bir filtre gibi davranır ve yalnızca çok küçük moleküllerin geçmesine izin verir. Birçok glioma tümöründe bu bariyer sızdırır hale gelir. Standart kontrast MRI’da, sızdıran alanlar enjeksiyondan sonra parlarken, sağlam bölgeler karanlık kalır. Bu desenler tümörün ne kadar agresif tedavi edileceğini etkiler ve cerrahi olarak neyin çıkarılacağı veya radyasyonla neyin hedefleneceğini belirlemeye yardımcı olur. Yine de kontrast taramalar bazen atlanır—örneğin erken değerlendirmelerde veya yavaş büyüyen tümörlerin uzun dönem takibinde—ve bazı hastalar böbrek hastalığı, alerjik reaksiyonlar veya gadolinyumun beyinde birikmesiyle ilgili endişeler nedeniyle kontrasttan tamamen kaçınmalıdır.
Olağan taramaları sanal kontrasta dönüştürmek
Yazarlar, halihazırda yaygın şekilde elde edilen kontrastsız MRI taramalarının, YZ’nin kontrastlı bir taramanın ne göstereceğini çıkarması için yeterli ince bilgiyi içerip içermediğini sorguladılar. İki yaygın sekansa odaklandılar: T1 ve T2‑FLAIR. Bunlar kan‑beyin bariyeri sızıntısını doğrudan göstermese de genellikle bariyer bozulmasına eşlik eden tümör yapısını, çevresel ödemi ve doku hasarını yakalarlar. Ekip, önce bu kontrastsız görüntülerden sentetik kontrastlı görüntüler üreten ve sonra bunları orijinal görüntülerle birlikte kullanarak her gliomada bariyerin sağlam mı yoksa bozulmuş mu olduğunu belirleyen CBSI adlı bir sistem geliştirdi.
Yeni YZ sistemi nasıl çalışıyor
CBSI’nin merkezinde bir difüzyon modeli vardır—gürültülü görüntülerden başlayıp bunları yineleyerek “gürültüsüzleştiren” bir tür YZ. Burada model, kontrastsız girdiyi iki alternatif sanal kontrast görüntüsüne dönüştürmeyi öğrenir: biri bariyerin sağlam olduğu varsayımıyla, diğeri bariyerin sızdırdığı varsayımıyla. Bir yönlendirme mekanizması modele hangi kontrastlanma desenine ulaşması gerektiğini söyler ve yardımcı bir segmentasyon adımı tümör bölgesine ekstra dikkat göstermesine yardımcı olur. İkinci aşamada, ayrı bir ağ her hasta için üretilen iki sentetik sonucu karşılaştırır ve hangisinin orijinal MRI verileriyle daha tutarlı olduğunu değerlendirir. Bu karar daha sonra öngörülen kan‑beyin bariyeri durumuna çevrilir.
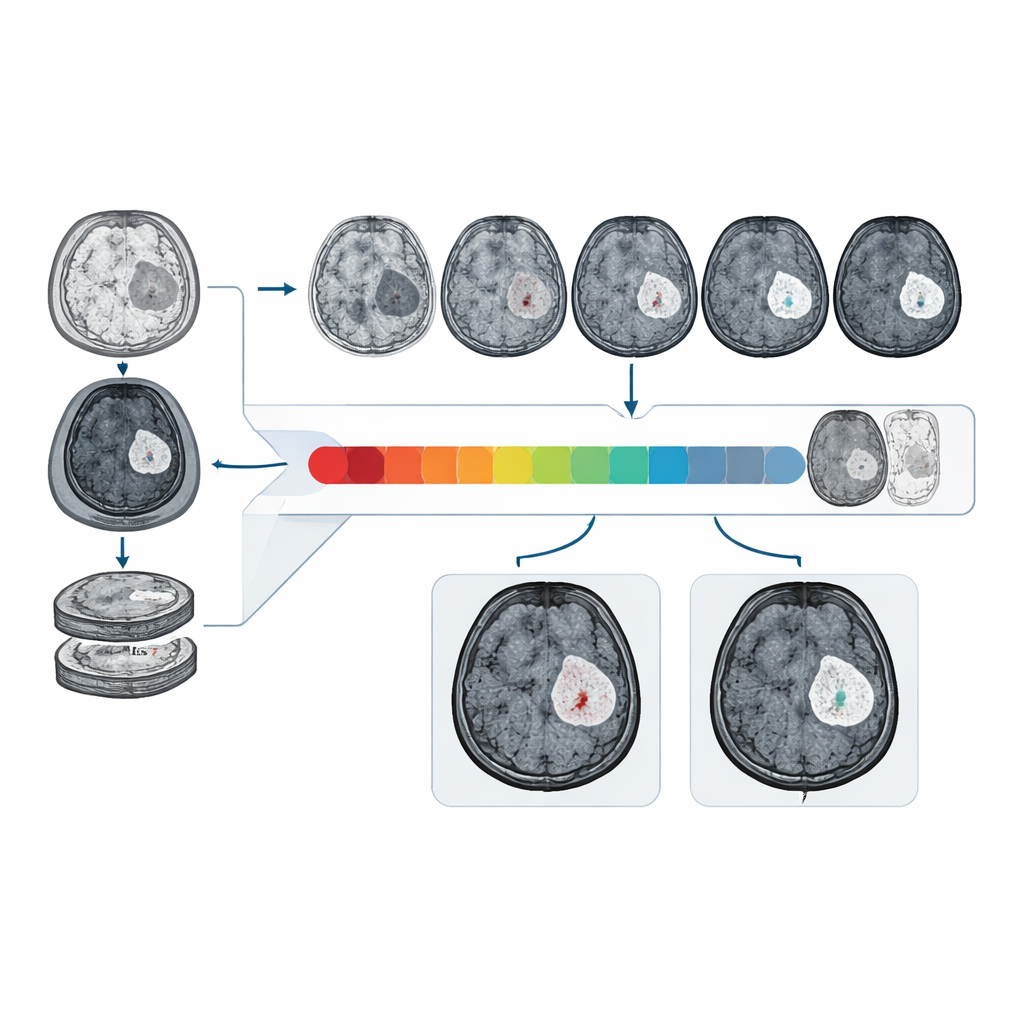
Gerçek ve çeşitli verilerde performansı
Araştırmacılar CBSI’yi çok sayıda hastaneden ve uluslararası kamu veri kümelerinden toplanan 1.535 glioma hastasına ait MRI verileri üzerinde eğitti ve test etti. Harici bir klinik test setinde CBSI, sağlam ile bozulmuş bariyerleri yaklaşık %81 civarında bir eğri altı alan (AUC) ile ayırt etti; bu, yalnızca kontrastsız görüntülere dayanan modellerden açıkça daha iyi ve gerçek kontrast taramalarına erişimi olan modellerin performansına yaklaşan bir sonuçtu. Radyologlar, sistemin gerçek ve sentetik kontrast görüntülerinin karıştırıldığı rastgele gösterimler sırasında, sentetik görüntülerin %90’dan fazlasını yüksek tanısal kalitede olarak değerlendirdiler ve sentetik görüntülerde kontrastlanmayı tanımlama yetenekleri gerçek taramalardaki performanslarına benzerdi.
Tedavi planlaması ve gelecekteki bakım için faydalar
CBSI tarafından üretilen sentetik kontrast görüntüleri tümör ayrıntılarını ve kontrastlanma desenlerini yakaladığından, tümör sınırlarının belirlenmesi ve tümör derecesinin tahmin edilmesi gibi sonraki görevlerde de iyileşme sağlandı—bunların her ikisi de büyük ölçüde kan‑beyin bariyerinin davranışına bağlıdır. Yöntem, Sub‑Sahara Afrika’daki veriler ve daha geniş uluslararası kohortlar dahil farklı tarayıcılara, görüntüleme protokollerine ve hasta popülasyonlarına iyi genelleşti. Yazarlar, herhangi bir derin öğrenme sisteminin biyolojiye doğrudan bir pencere değil, istatistiksel bir araç olarak kaldığını kabul etmekle birlikte, sonuçlar sanal kontrast görüntülemenin özellikle savunmasız hastalar veya kontrast taramalarının elde edilmesinin zor olduğu ortamlarda enjekte edilen ajanlara olan bağımlılığı azaltabileceğini öne sürüyor. Pratik olarak, bu YZ yaklaşımı doktorların hastaların zaten aldığı taramalardan kan‑beyin bariyeri hakkında tedavi planını şekillendiren kilit bilgileri—ek bir iğne gerektirmeden—çıkarmasına olanak verebilir.
Atıf: Zheng, K., Zhang, Y., Shu, H. et al. Contrast-free identification of glioma blood-brain barrier status via generative diffusion AI and non-contrast MRI. Nat Commun 17, 2162 (2026). https://doi.org/10.1038/s41467-026-69578-8
Anahtar kelimeler: glioma, kan-beyin bariyeri, beyin MRI, tıbbi görüntüleme yapay zekâsı, kontrastsız görüntüleme