Clear Sky Science · tr
Poxvirüs RNA polimerazı ve onun TBP/TFIIB-benzeri ortağı tarafından gerçekleştirilen işbirlikçi kelepçe aracılı promotor tanıma
Bir Virüsün Hücre İçindeki Gen Kontrolünü Nasıl Yeniden Düzenlediği
Çiçek hastalığına tarihsel olarak yol açan virüsü de içeren poxvirüsler, tüm gen ifadelerini hücrelerimizin çekirdeğinde yer alan DNA kontrol merkezinden uzakta, sitoplazmada gerçekleştirir. Bunu başarmak için yanlarında kendi küçük “genetik fabrikalarını” getirirler. Bu çalışma, atomik ayrıntıda, Vaccinia adlı bir virüsün enfeksiyon ortasında belirli bir gen dalgasını nasıl açtığını, viral kopyalama makinesiyle birlikte çalışan beklenmedik kelepçe benzeri bir protein kullanarak nasıl gerçekleştirdiğini ortaya koyuyor.
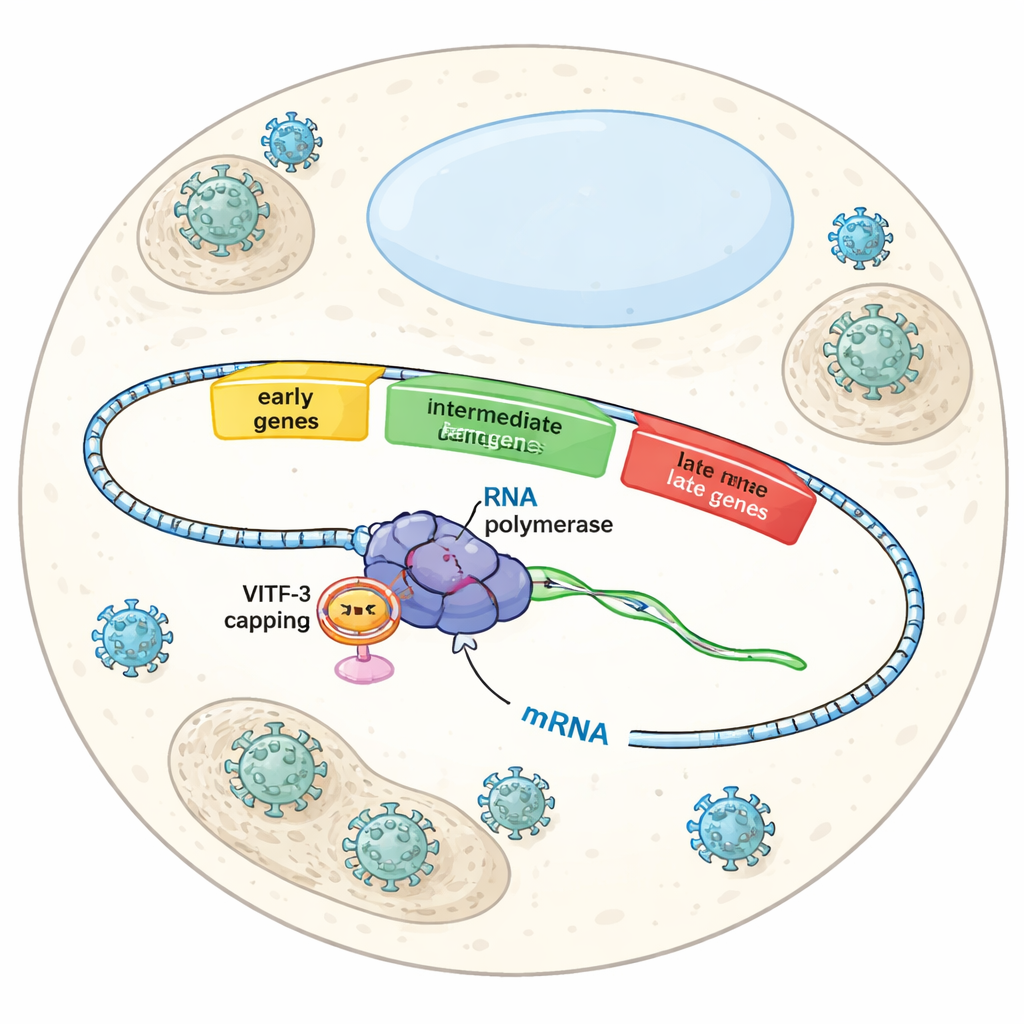
Viral Ele Geçirmede Üç Dalga
Vaccinia bir hücreyi enfekte ettiğinde tüm genlerini aynı anda açmaz. Bunun yerine erken, ara ve geç genlerden oluşan dikkatle zamanlanmış bir senaryoyu izler. Erken genler viral çoğalma için zemin hazırlar, ara genler yeni virüs partiküllerinin yapılması için gereken araçları inşa etmeye yardımcı olur ve geç genler montajı ve paketlemeyi tamamlar. Her dalga aynı viral RNA polimerazına—DNA’yı okuyup RNA yapan enzim—bağlıdır, fakat farklı yardımcı faktörler polimerazın hangi gen grubunu her aşamada etkinleştireceğini belirler. Bugüne dek bilim insanları erken gen kontrolünü oldukça iyi anlamıştı, ancak virüsün ara genleri nasıl özel olarak tanıyıp aktifleştirdiği gizemini koruyordu.
Ortak Gerektiren Halka Şeklinde Bir Yardımcı
Ara genleri açmak için gerekli olduğu bilinen VITF‑3 adlı iki parçalı proteína odaklanıldı. İnsanlar da dahil olmak üzere birçok organizma, RNA polimerazlarını DNA üzerinde doğru başlangıç noktasına yönlendirmek için TBP ve TFIIB adı verilen bir çift protein kullanır. Ekip, VITF‑3’ün bu eski çiftin oldukça değiştirilmiş bir versiyonu olduğunu gösterdi. Ancak hücresel akrabalarının aksine VITF‑3 tek başına DNA’ya tutunamıyor. Bunun yerine iki alt birimi birbirine kenetlenerek kapalı bir halka oluşturuyor ve viral RNA polimeraz mevcut olmadıkça bu halka DNA’ya karşı etkisiz kalıyor. Bu beklenmedikti; çünkü çoğu sistemde TBP-benzeri bileşen önce promotor DNA’sına bağlanır ve sonra polimerazı işe alır; burada ise virüs olayların sıralamasını yeniden düzenlemiş gibi görünüyor.
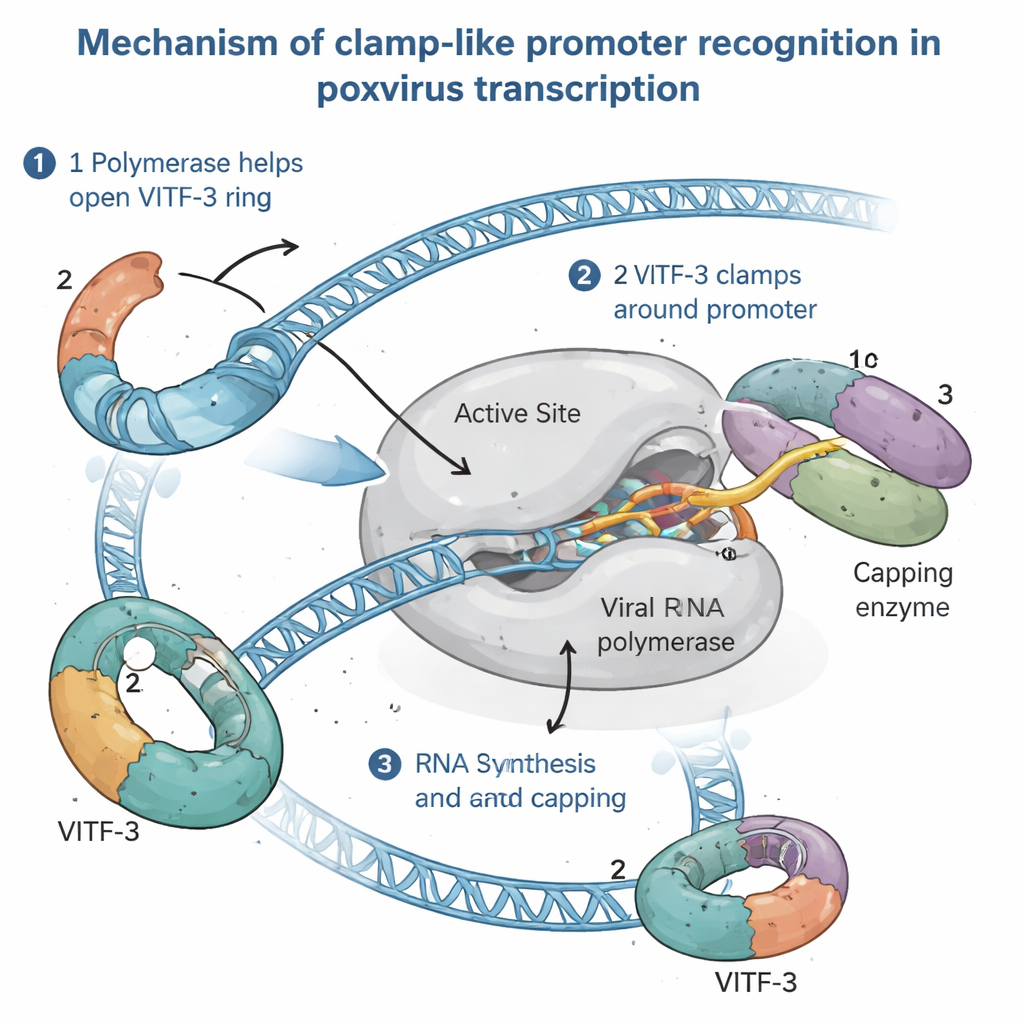
Ara Transkripsiyon Makinesini Eylem Halinde Görmek
Bu sıra dışı düzenin nasıl çalıştığını anlamak için yazarlar, enfekte insan hücrelerinden RNA sentezi başlamadan hemen önce hazır hâlde bulunan tam ara ön-başlatma kompleksi topladılar. Yüksek çözünürlüklü kriyo-elektron mikroskobisi kullanarak kompleksi yaklaşık 2.4 Å ayrıntıda görselleştirdiler; bu, amino asit yan zincirlerini ve tek tek DNA bazlarını görmek için yeterli incelikteydi. Görüntüler, promotor DNA’sını kavrayan viral RNA polimerazı ve VITF‑3’ün başlangıç noktasının hemen yukarısında AT bakımından zengin bir DNA dizisi etrafında sıkı bir halka oluşturduğunu ortaya koydu. Bu halka DNA’yı yaklaşık 90 derece büküyor ve onu polimerazdaki bir yarığa doğru besliyor. Aynı zamanda viral bir kaplama (capping) enzimi—viral RNA’nın 5′ ucuna koruyucu kapağı eklemekten sorumlu—polimeraz üzerinde demirlenmiş halde, yeni transkriptler ortaya çıkar çıkmaz onları modifiye etmeye hazır bulunuyor.
Ruhen Ödünç Alınmış Bir Kelepçe-Yükleyici Mekanizması
Yapısal anlık görüntüleri biyokimyasal testlerle birleştirerek çalışma, viral RNA polimerazın VITF‑3’ü DNA’ya aktif şekilde yüklediğini, bir “kelepçe-yükleyici” gibi davrandığını öne sürüyor. Önce polimeraz bir ara promotora bağlanıyor ve VITF‑3 halkasını açmaya yardımcı oluyor. Ardından, kaplama enzimiyle birlikte AT-zengin bölge etrafında halkayı kapatıp kompleksi yerine kelepçeliyor. DNA, başlangıç noktasına yakın bölgede eriyor (melt), ve polimeraz RNA sentezinin tam olarak nerede başlaması gerektiğini işaretleyen kısa dört harfli bir sinyali (TAAA motifi) doğrudan okuyor. RNA büyüdükçe, başlangıç kompleksinde VITF‑3’ün işgal ettiği aynı yolu izliyor; dolayısıyla ortaya çıkan RNA muhtemelen VITF‑3’ü kenara iterek polimerazın promotordan ayrılmasına ve gen üzerinde ilerlemesine izin veriyor; VITF‑3 ise aynı promotörün yeniden kullanılmasını hızlandırmak üzere geride kalabilir.
Bu Bulguların Poxvirüsleri Anlama ve Hedefleme Açısından Önemi
Basitçe söylemek gerekirse bu çalışma, Vaccinia virüsünün evrensel bir gen-kontrol modülünü yalnızca kendi RNA polimerazı onu yönlendirdiğinde DNA’yı kavrayan bir kelepçeye dönüştürdüğünü gösteriyor. Bu zekice düzenleme, virüsün tek bir çekirdek enzimi farklı yardımcı faktörlerle değiştirerek üç çok farklı transkripsiyon programını işletmesine izin veriyor. Aynı tür faktörler pek çok poxvirüste, insan patojenleri dahil, korunmuş olduğundan yeni ortaya konan kelepçe-yükleyici mekanizma ve benzersiz VITF‑3 halkası, enfeksiyon sırasında virüsün genlerini zamanlamasını ve kontrol etmesini bozmayı amaçlayan antiviral stratejiler için somut yapısal hedefler sunuyor.
Atıf: Jungwirth, S., Bartuli, J., Lamer, S. et al. Cooperative clamp-mediated promoter recognition by poxviral RNA polymerase and its TBP/TFIIB-like partner. Nat Commun 17, 1648 (2026). https://doi.org/10.1038/s41467-026-69571-1
Anahtar kelimeler: poxvirüs transkripsiyonu, Vaccinia virüsü, RNA polimeraz, promotor tanıma, transkripsiyon faktörleri