Clear Sky Science · tr
Kirleticilerin parçalanmasına yönelik periodat aktivasyonunda mekanistik farklılıkları açıklayan evrensel belirteç olarak hidratlanmış metal yük yoğunluğu
Akıllı Kimya ile Suyu Temizlemek
Birçok ilaç ve endüstriyel kimyasal, geleneksel su arıtma tesislerinden geçip nehirler ve içme suyuna karışıyor. Bu çalışma, yaygın bir oksitleyici olan periodat kullanarak bu inatçı kirleticileri parçalamanın umut verici bir yolunu araştırıyor ve su içindeki metal iyonlarının basit bir özelliğinin bu kimyanın ne kadar iyi — ve ne kadar güvenli — işleyeceğini öngörebildiğini gösteriyor. Bu kuralı anlamak, mühendislerin çeşitli gerçek dünya sularında daha temiz ve daha verimli arıtma sistemleri tasarlamasına yardımcı olabilir.
Kirletici Ayrışmasında Metal Seçiminin Önemi
İleri oksidasyon süreçleri, organik molekülleri parçalamak için güçlü reaktif türler kullanır. Periodat bu oksitleyicilerden biridir ve çözünmüş metal iyonları tarafından “aktive” edilebilir. Yazarlar, aynı periyodik tablo sütununa ait ve benzer davranması beklenebilecek üç yakından ilişkili metali — demir, rutenyum ve osmiyum — karşılaştırdı. Üçü de periodatı aktive edip test ilaç kirleticisi karbamazepini yok etmeye yardımcı olabiliyor. Ancak deneyler çarpıcı farklılıklar gösterdi: rutenyum son derece hızlı çalıştı, demir daha yavaştı ve osmiyum ortada yer aldı. Daha da şaşırtıcı olan, osmiyumun çok çeşitli kirleticileri ayırt etmeden uzaklaştırması, oysa demir ve rutenyumun bazı bileşiklere diğerlerine göre çok daha seçici saldırmasıydı.
İki Çok Farklı Kimyasal Yol
Bu farklılıkların ardındaki nedenleri ortaya çıkarmak için ekip, her metal–periodat sisteminde hangi kısa ömürlü oksitleyici türlerin ortaya çıktığını izledi. Demir ve rutenyum sistemlerinde hakim oyuncular, kirleticinin belirli bölgelerine doğrudan bir oksijen atomu aktaran hassas araçlar gibi davranan “metal–oksijen” birimleriydi. Bu yollar genellikle tek bir oksijen atomu ekleyen epoksit ürünler — halkalı yapılar — oluşturuyordu ve bunun reaksiyonun oldukça seçici olduğunu gösterdi. Osmiyum sisteminde ise ana aktörler, neredeyse herhangi bir yakın organik moleküle saldıran son derece reaktif hidroksil radikalleriydi; bu da hidroksillenmiş ürünler ve küçük halka açılmış parçacıklar oluşmasına yol açtı. Kimyasal problar ve spin‑tuzağı spektroskopisi ile yapılan testler, osmiyum bulunduğunda kirletici yok edilmesinin çoğunu yüksek değerlikli osmiyum–oksijen birimlerinin değil, hidroksil radikalleri ve ilgili reaktif oksijen türlerinin yönettiğini doğruladı.
Su Koşullarının Reaksiyonları Nasıl Şekillendirdiği
Ekip ayrıca pH ve doğal su bileşenlerinin bu süreçleri nasıl etkilediğini inceledi. Osmiyum için kirletici giderimi, su daha alkalin hale geldikçe güçlendi; bu durumda metale çevredeki ekstra hidroksit iyonlarının koordinasyonu elektron hareketini ve radikal oluşumunu kolaylaştırıyordu. Ancak yüksek metal veya oksidan dozlarında osmiyum sistemi, yeni oluşan radikallerin fazlalık kimyasallar tarafından kirleticiler yerine yok edilmesi nedeniyle “kendini söndürdü”. Oksidasyon reaksiyonlarına sıklıkla müdahale eden doğal organik madde, osmiyum kaynaklı bozulma üzerinde şaşırtıcı derecede az etki yaptı; bu da radikal yolunun gerçekçi sularda dayanıklı kaldığını düşündürüyor. Buna karşılık, demir ve rutenyum asidik koşullarda en iyi performansı gösterdi ve doğal organik madde, anahtar metal–oksijen oksidanlarını bağlayarak aktivitelerini güçlü biçimde bastırdı.
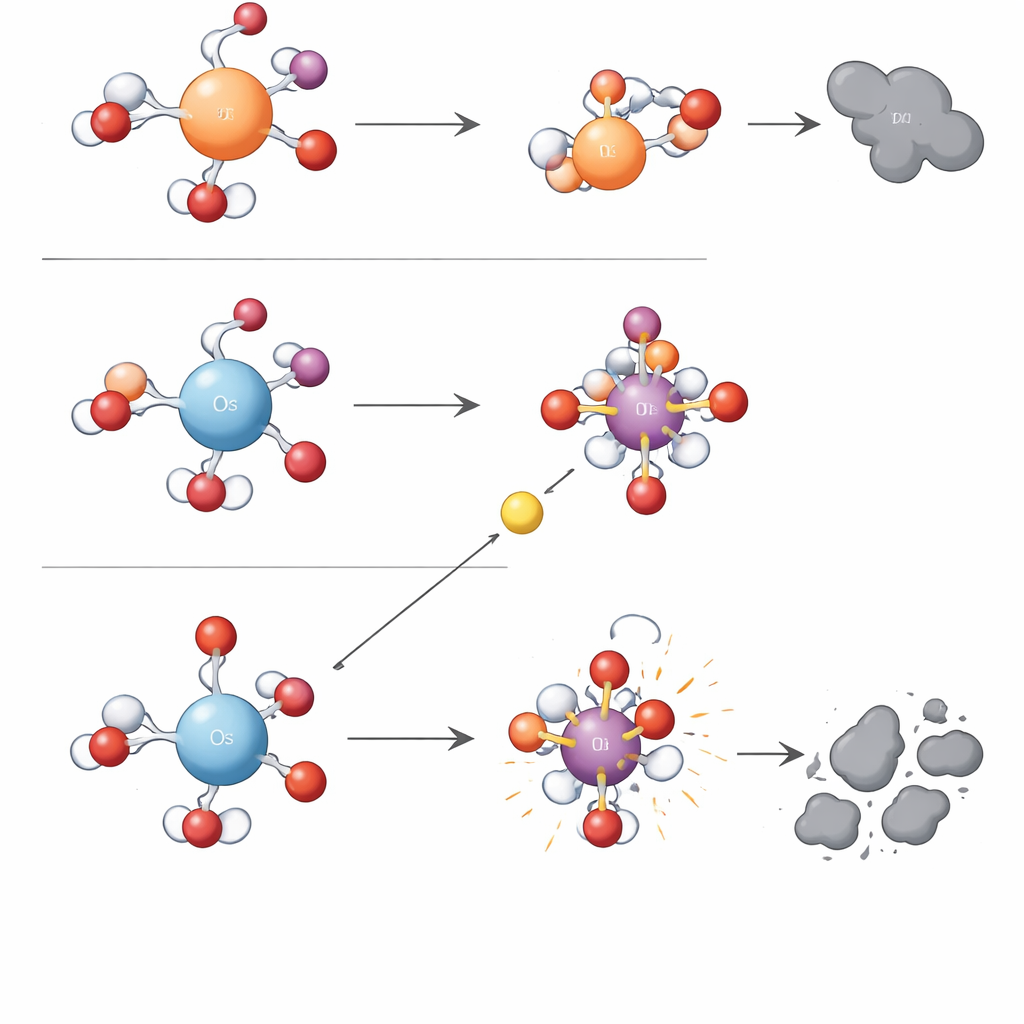
Karmaşık Kimyanın Arkasındaki Basit Bir Yük Kuralı
Deneme‑yanılmadan öteye geçmek için araştırmacılar kuantum‑kimyasal hesaplamalara başvurdu. Bir elektronik özellik — hidratlanmış metal merkezinin pozitif yük yoğunluğu — iki reaksiyon tipi arasındaki ayrımı açıklayabildi. Suda osmiyum, demir veya rutenyuma göre daha yüksek yoğunlukta pozitif yük taşıyor. Bu güçlü pozitif merkez bağlı oksijen atomuna sıkı sıkıya tutunuyor, metal–oksijen birimini kararlı ama doğrudan oksijen aktarımı konusunda ağırmetalik hale getiriyor. Aynı zamanda, çevredeki su ve iyonlar üzerindeki güçlü çekim, periodattaki bir oksijen bağının tek elektron adımlarıyla kırılmasının ve hidroksil radikallerinin açığa çıkmasının enerji bariyerini düşürüyor. Daha düşük yük yoğunluğuna sahip metaller (demir ve rutenyum gibi), elektronları daha sıkı tutuyor ve serbest radikaller yerine seçici metal–oksijen oksidanlarının oluşumunu ve kullanılmasını destekliyor. Yazarlar bu düzenleyici fikre "Yük Yoğunluğu Kontrol Mekanizması" adını veriyor ve mangan gibi diğer metaller için bildirilen eğilimleri de bunun rasyonelize ettiğini gösteriyor.
Tek Bir Düğmeyle Daha İyi Su Arıtımı Tasarlamak
Çok sayıda gözlemi tek bir basit belirtece — suyla çevrili bir metalin yük yoğunluğuna — bağlayarak, bu çalışma ileri oksidasyon süreçlerini kişiselleştirmek için bir yol haritası sunuyor. Yüksek yük yoğunluklu metaller, özellikle alkalin veya organikçe zengin sularda, geniş kapsamlı, radikal tabanlı karma kirletici karışımlarının parçalanmasını desteklemelidir. Düşük yük yoğunluklu metaller ise, her şeyi aşırı oksitlemeden belli kirleticileri dönüştürmek gibi seçici ve daha nazik oksidasyon istendiğinde daha uygundur. Pratik yönden, bu, kimyagerlerin ve mühendislerin su arıtımı için katalizörleri her sistemi deneme‑yanılmayla optimize etmek yerine, metal merkezlerinin sulu ortamlarında yükü ne kadar sıkı tuttuklarını ayarlayarak tarayabilecekleri veya tasarlayabilecekleri anlamına gelir.
Atıf: Qian, Y., Sun, Y., Xu, J. et al. Hydrated metal charge density as a universal descriptor explaining mechanistic variations in periodate activation toward pollutant degradation. Nat Commun 17, 2683 (2026). https://doi.org/10.1038/s41467-026-69496-9
Anahtar kelimeler: ileri oksidasyon süreçleri, periodat aktivasyonu, su arıtımı, geçiş metali katalizi, hidroksil radikalleri