Clear Sky Science · tr
STING, TGF-β ve PD-L1’in üçlü hedeflenmesi CXCL16–CXCR6 sinyalini güçlendirerek güçlü antitumör yanıtı sağlar
Soğuk Tümörleri Sıcak Hale Getirmek
Kanser immünoterapisi bazı hastalar için tedaviyi dönüştürdü, ancak birçok tümör bu güçlü ilaçlara hâlâ direnç gösteriyor. Bu çalışma, belli kanserlerin modern bağışıklık “kontrol noktası” ilaçlarına neden dirençli olduğunu araştırıyor ve vücudun savunmasını uyandıran, seçkin öldürücü T hücrelerini çekip tümör içinde aktif tutan akıllı, üç yönlü bir saldırı öneriyor.
Mevcut İmmün İlaçlar Neden Yeterli Değil
Onaylanmış immünoterapilerin çoğu, PD-1/PD-L1 yolakları gibi bağışıklık hücrelerindeki tek bir fren noktasını hedef alıyor. Daha yeni bir ilaç sınıfı ise TGF-β’yi de bloke ederek ileri evre kanserlerde güçlü şekilde baskı yapan bu molekülleri devre dışı bırakmaya çalışıyor. YM101 adlı bir bileşik, tek bir antikor içinde TGF-β ve PD-L1 blokajını birleştiriyor ve farelerde ümit verici sonuçlar gösterdi. Yine de genetik olarak özdeş hayvanlarda bazı tümörler neredeyse hiç küçülmedi. Yanıt veren ve dirençli tümörleri karşılaştırarak, araştırmacılar başarılı tedavinin güçlü “doğal” bağışıklık aktivasyonu ile, özellikle anormal DNA’yı algılayıp antiviral benzeri alarm sinyalleri başlatan STING adlı yolak üzerinden gelen sinyalleme ile el ele gittiğini buldular.
Üçüncü Bir Kolu Eklemek: STING Yolu
Zayıf doğal aktivasyonun eksik halka olduğunu düşünerek ekip, YM101’i MSA-2 adlı hap şeklinde bir STING agonisti ile çeşitli fare tümör modellerinde, tipik olarak tedaviye dirençli “soğuk” tümörler de dahil olmak üzere kombinledi. STING aktivasyonu ile TGF-β ve PD-L1 blokajını birleştiren üçlü yaklaşım tümörleri daha etkili şekilde küçülttü, yaşam süresini uzattı ve sıklıkla yeniden meydan okuma sonrası tümör geri oluşumuna karşı fareleri koruyarak uzun süreli bağışıklık belleğini gösterdi. Bu, yalnızca STING agonisti ile PD-L1 blokajının eşleştirilmesinden daha üstün performans gösterdi ve yalnızca TGF-β bloke edildiğinde bile STING agonist tedavisini güçlendirdi; bu da TGF-β’nin STING kaynaklı bağışıklık üzerinde önemli bir fren görevi gördüğünü ortaya koydu. 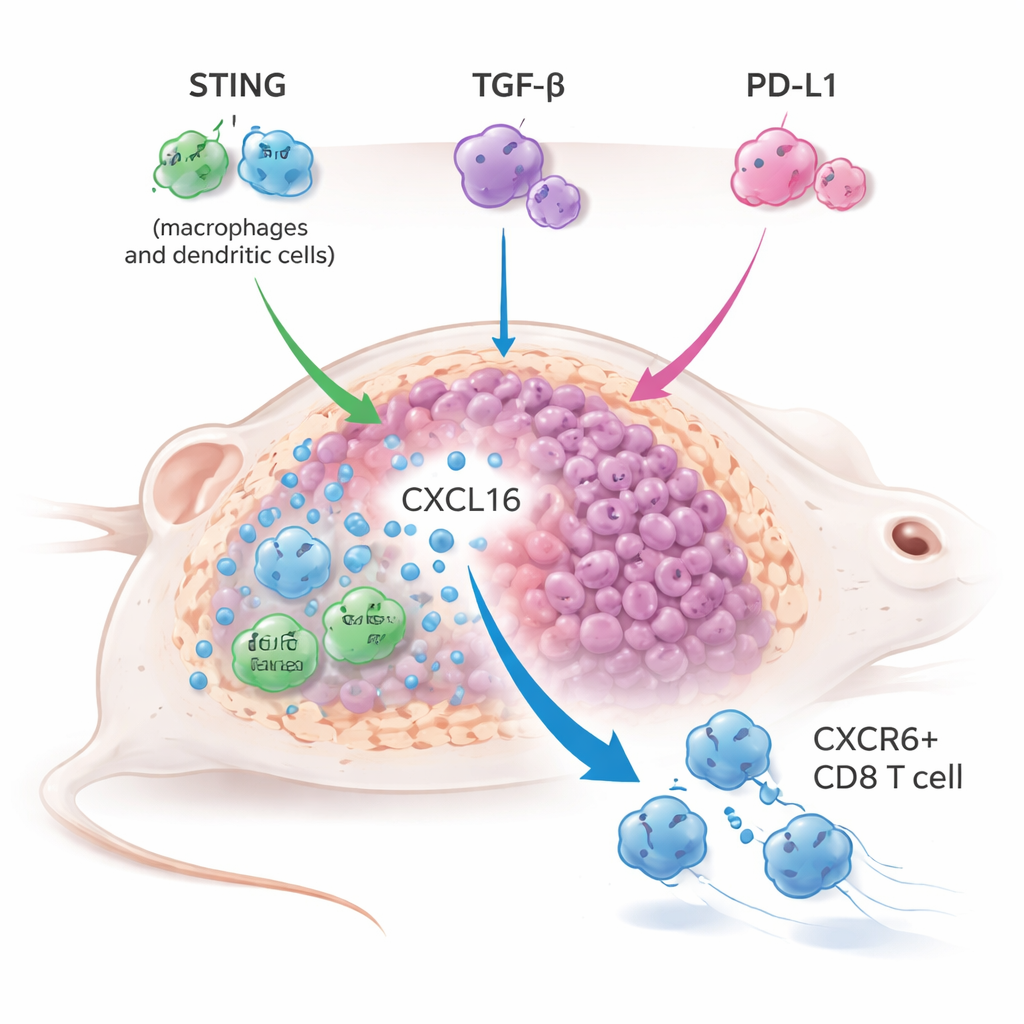
Uzman Bir Öldürücü Birliği Çağırmak
Bu üçlü stratejinin nasıl işe yaradığına dair anlayış için araştırmacılar tek hücreli RNA dizilemesi ve tedavi edilen tümörlerin ayrıntılı bağışıklık profillemesini kullandılar. CXCR6 reseptörü ile işaretlenmiş belirli bir öldürücü T hücresi alt grubunun çarpıcı bir şekilde genişlediğini keşfettiler. Bu CXCR6+ CD8 T hücreleri yüksek seviyede granzim, perforin ve iltihabi moleküller ifade ederek son derece donanımlıydı ve güçlü aktivasyon ve proliferasyon belirtileri gösteriyordu. Aynı zamanda tümör ilişkili makrofajlar ve dendritik hücreler, CXCR6’ye bağlanan ve bu T hücrelerini tümörde tutmaya yardımcı olan CXCL16 adlı bir kemokin üretimini artırdı. CXCL16–CXCR6 bağlantısı ya CXCL16’yı bloke ederek ya da T hücrelerinde genetik olarak CXCR6’yı silerek bozulduğunda kombine tedavi büyük ölçüde antitümör gücünü kaybetti; bu eksen terapinin başarısında merkezi bir rol oynadığını kanıtladı.
Sinyal Kaskadı Nasıl Açılıyor
Daha derine inerek ekip, STING aktivasyonu ile TGF-β blokajının birlikte CXCL16’yı nasıl artırdığını sordu. İnsan ve fare bağışıklık hücrelerinde STING agonistleri CXCL16 ve antiviral sitokin IFN‑β’yi güçlü şekilde artırırken, eklenen TGF-β her ikisini de keskin şekilde azalttı. Araştırmacılar STING’in IFN‑I sinyallemesini tetiklediğini, bunun da transkripsiyon faktörü STAT1’i aktive ettiğini; STAT1’in ardından doğrudan CXCL16 geninin kontrol bölgesine bağlanıp onu açtığını gösterdiler. TGF-β, muhtemelen HDAC4 adlı bir protein ve reaktif oksijen türleri yoluyla STING sinyallemesindeki kritik bir adımı bozarak bu zinciri kesintiye uğratıyor; bu da IRF3 aktivasyonunu ve aşağı yönlü IFN‑β ile CXCL16 üretimini azaltıyor. TGF-β’yi bloke etmek bu freni kaldırıyor ve STING agonistlerinin miyeloid hücrelerde STAT1–CXCL16 yolunu tam olarak ateşlemesine izin veriyor; böylece CXCR6+ T hücrelerini tümörde kalmaları ve savaşmaları için gerekli sinyallerle besliyor.
Tek Bir Hassas İlaç Oluşturmak
Bu karmaşık rejimi daha pratik ve tümöre odaklı hale getirmek için araştırmacılar Y101S adlı tek bir “immün-uYarıcı antikor konjugatı” mühendislik ettiler. Bu molekül, çift TGF-β/PD-L1 blokajı yapan antikoru, koparılarak serbest bırakılabilen bir bağlayıcıyla tutturulmuş bir STING agonistiyle birleştiriyor. Y101S, tümörde PD-L1 pozitif miyeloid hücrelere yöneliyor, hücre içine alınarak STING ilacını bu hücrelerin içinde serbest bırakıyor. Birkaç fare kanser modelinde Y101S, yüksek doz serbest STING agonistiyle birlikte verilen YM101’in etkinliğine eşdeğer veya üstün performans gösterdi; üstelik yalnızca çok küçük bir STING dozu taşımasına rağmen. CXCL16+ makrofajlar ve dendritik hücreleri artırdı, CXCR6+ CD8 T hücrelerini genişletti, kalıcı immün bellek indükledi ve iltihabi sinyalleri sağlıklı organları koruyarak tümörlerde yoğunlaştırdı; farelerde kabul edilebilir bir güvenlik profili gösterdi. 
Gelecekteki Kanser Tedavisi İçin Anlamı
Uzman olmayanlar için ana mesaj şudur: tek veya çift bağışıklık anahtarına saldırmak yeterli olmayabilir—özellikle tümörler erken alarm sistemlerini aktif biçimde susturduğunda. Bu çalışma, STING aktivasyonunu TGF-β ve PD-L1 blokajıyla birleştirmenin tümör ortamını yeniden kablolayabileceğini, seçkin bir öldürücü T hücresi grubunu güçlü şekilde çekip sürdürebileceğini ve preklinik modellerde daha derin, daha kalıcı yanıtlar elde edebileceğini gösteriyor. Üçlü hedefli antikor–ilaç Y101S bu stratejiyi tek, hedeflenmiş bir ilaçta somutlaştırıyor ve şu anda standart kontrol noktası ilaçlarına dirençli olan tümörlere yönelik yeni nesil immünoterapiler için bir yol haritası sunuyor.
Atıf: Yi, M., Li, T., Gu, Y. et al. Triple targeting of STING, TGF-β, and PD-L1 boosts CXCL16–CXCR6 signaling for potent antitumor response. Nat Commun 17, 1441 (2026). https://doi.org/10.1038/s41467-026-69456-3
Anahtar kelimeler: kanser immünoterapisi, STING yolakları, TGF-beta blokajı, PD-L1 antikoru, CXCL16 CXCR6 T hücreleri