Clear Sky Science · tr
RAS-bağlanma ve sistein açısından zengin domainler arasındaki pozitif işbirliği, RAF’ın membrana bağlanma kinetiğini yanal yeniden tutunma yoluyla düzenler
Bu küçük moleküler dans neden önemli
Hücrelerimizin içinde büyüme, bölünme ve hayatta kalma gibi yaşamı belirleyen kararlar sıklıkla hücre zarının yüzeyinde alınır. Bu kararların kilit oyuncularından biri, büyüme sinyallerini ileten ve kanserde sıklıkla yanlış düzenlenen RAF adlı bir proteindir. Bu çalışma, RAF’ın hücre zarına nasıl tutunduğunu, ne kadar süre orada kaldığını ve RAS adlı başka bir proteinin yoğun kümelerinin neden RAF’ı beklenenden daha uzun süre aktif tutabildiğini eşi görülmemiş kinetik ayrıntıyla ortaya koyuyor.
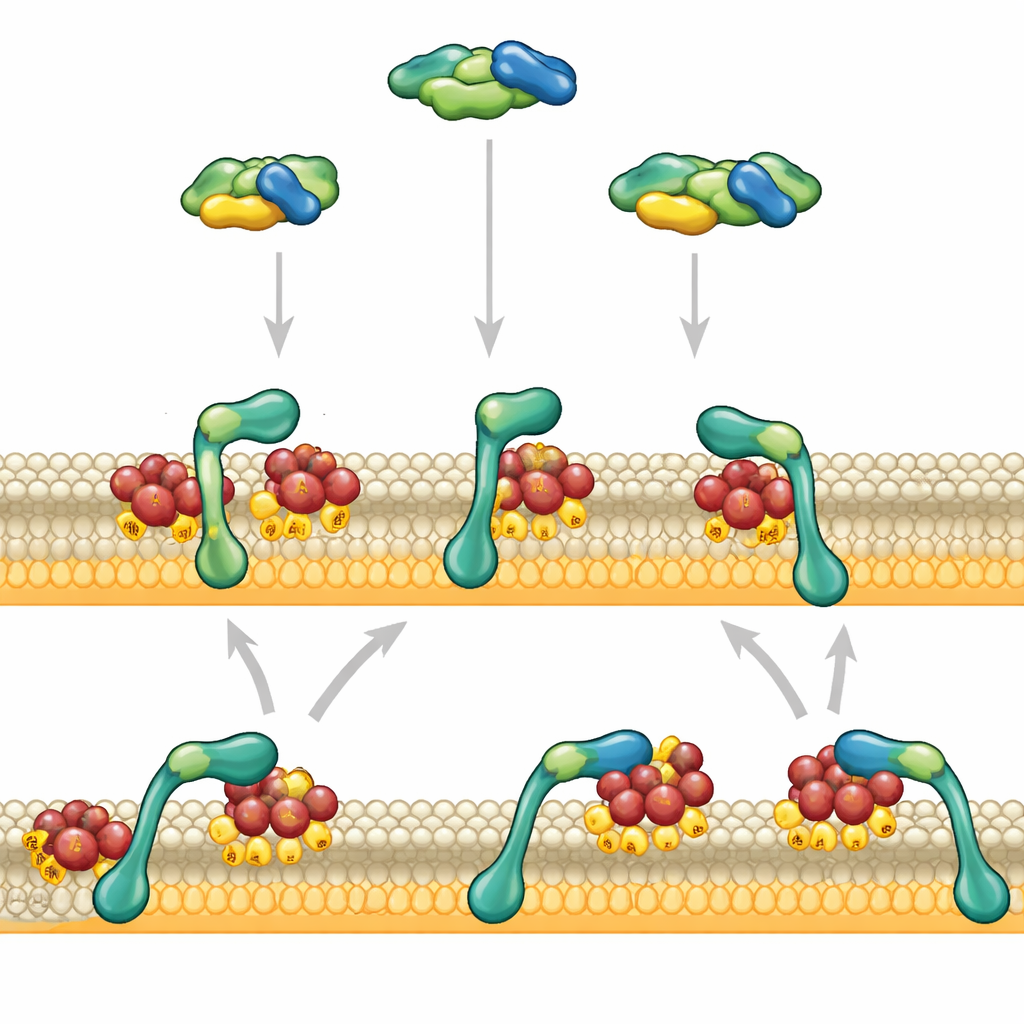
Hücre yüzeyinde buluşan sinyaller
RAF, dış uyarıları—örneğin büyüme faktörlerini—gen ifade değişikliklerine bağlayan MAPK yolunda görev yapan önemli bir sinyal koridorunda çalışır. Dinlenme halinde RAF, hücre içinde katlanmış ve kendi kendini baskılayan bir biçimde salınır. Yalnızca RAS ile karşılaştığında açılır; RAS, hücre zarının iç yüzeyine bağlı küçük bir moleküler anahtardır. RAF’ın işe alınması ve aktive olması için RAS’ın “açık” durumda olması ve doğru tür lipidlere gömülü olması gerekir. RAF molekülleri birçok diğer sinyal bileşenine kıyasla nispeten az olduğundan, onların zarla nasıl etkileşime girdiği ve erken salınımdan nasıl kaçındığı, bir hücrenin bir büyüme sinyaline zayıf mı yoksa güçlü mü yanıt vereceğini büyük ölçüde etkiler.
Zarı kavramak için iki el
Yazarlar RAF’ın ön ucundaki iki bölgeye odaklandı: birisi RAS’ı tutan, diğeri negatif yüklü zar lipidlerini seven bölge. Yapay zarlar ve saflaştırılmış proteinler kullanarak, gelişmiş mikroskopiyle tek tek RAF parçacıklarının RAS ile kaplı yüzeylere bağlanmasını izlediler. Sadece RAS-bağlayan bölge tek başına davrandığında, zarla kısa süreli temas ediyor ve yaklaşık bir saniye içinde ayrılıyordu. Lipid seven bölge tek başına neredeyse hiç tutunmuyordu. Ancak bu iki bölge birbirine bağlandığında davranış çok farklılaştı: RAF artık güçlü şekilde bağlanıyor ve özellikle gerçek hücrelerdeki lipidlere benzer çok sayıda negatif yüklü lipid taşıyan zarlar üzerinde onlarla ifade edilebilecek sürelerde—onlarca saniye—uzun süre kaldı.
Çıkışı yavaşlatan işbirliği
Bu dramatik değişim, RAF’ın zarı daha hızlı bulmasından değil, daha yavaş ayrılmasından kaynaklandı. Önce, RAF’ın RAS-bağlayan segmenti aktive olmuş RAS’ı tanır ve RAF’ı zar üzerine yanaştırır. Bu ilk tokalaşmadan sonra lipid-bağlayan bölge çevredeki lipidlerle tam olarak etkileşime girer, RAF’ın yanal hareketini yavaşlatır ve onu daha sıkı sabitler. Bu ikinci temas ise orijinal RAS–RAF etkileşimini stabilize ederek protein–protein ile protein–lipid temasları arasında pozitif geri besleme oluşturur. İki bölgeyi birbirine bağlayan kısa bağlantıyı (linker) değiştiren deneyler, sıkı mekânsal koordinasyonun kritik olduğunu gösterdi: linkeri daha esnek veya daha uzun yapmak, RAF’ın zar üzerinde kalma yeteneğini zayıflattı.
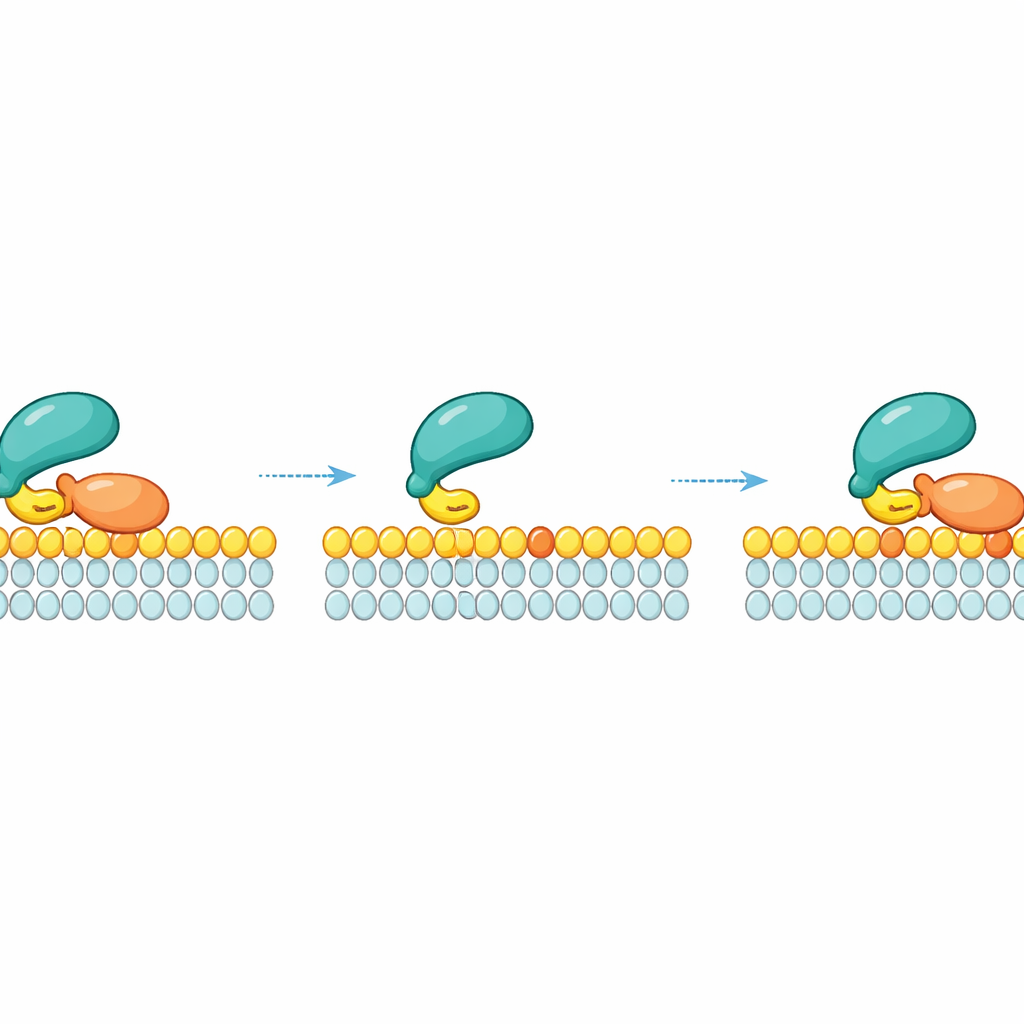
Yanal yeniden tutunma: düşmek yerine kaymak
Çalışmanın önemli bir bulgusu şudur: RAF, belirli bir RAS molekülünden ayrıldıktan sonra basitçe çevre sıvıya kopup gitmez. Bunun yerine RAS serbest kaldıktan sonra RAF, zayıf lipid temasları üzerinden kısa süreliğine zarla bağlı kalabilir ve yanal olarak kayabilir. Bu geçici durumda iken aynı zar yaması üzerindeki komşu bir RAS molekülünü yeniden “yakalayabilir”. Bu yanal yeniden tutunma kinetik bir güvenlik ağı yaratır: yüksek yerel RAS yoğunluğunda—RAS moleküllerinin sıkça paketlendiği nanokümeler gibi—RAF’ın uzaklaşmadan önce RAS ile yeniden etkileşime girme şansı çok daha fazladır. Ölçümler ve simülasyonlar, zar üzerindeki aktif RAS yoğunluğu arttıkça RAF’ın tekrar eden yerel yeniden bağlanmalar nedeniyle daha uzun süre membrana bağlı kaldığını gösterdi.
Uzun ziyaretlerden güvenilir aktivasyona
RAF’ın zar üzerinde geçirdiği uzamış zamanın önemli sonuçları vardır. RAF aktivasyonu tek bir olay değil, şekil değişiklikleri, baskılayıcı işaretlerin kaldırılması ve iki RAF molekülünün aktif bir dimer oluşturmak üzere eşleşmesi gibi çok adımlı bir dizidir. Çalışma, yalnızca zar üzerinde yeterince uzun süre kalan RAF moleküllerinin bu diziyi tamamlayabileceğini; bu durumun, kısa ömürlü ve zayıf sinyallerin kazara aktivasyona yol açmasını engelleyen bir tür “kinetik doğrulama” olduğunu öne sürüyor. RAS bağlanması, lipid etkileşimi ve yanal yeniden tutunma arasındaki etkileşimin RAF’ın membran ikametini nasıl belirlediğini ortaya koyarak, çalışma hücrelerin zar üzerindeki birçok küçük, zayıf etkileşimi kullanarak güçlü sinyal yollarını hassas biçimde ayarlama stratejisini genel olarak tanımlıyor.
Atıf: Jimenez Salinas, A., Tevdorashvili, K., Grim, J. et al. Positive cooperativity between RAS-binding and cysteine-rich domains regulates RAF membrane binding kinetics via lateral rebinding. Nat Commun 17, 2593 (2026). https://doi.org/10.1038/s41467-026-69437-6
Anahtar kelimeler: RAS, RAF kinaz, hücre zarı sinyalleşmesi, yanal yeniden tutunma, kinetik doğrulama