Clear Sky Science · tr
İnsan fosforibozilformilglisinamidin sentezazının allosterik düzenlenmesi ve katalitik bağlanmasının yapısal ve moleküler temeli
Bu Enzimin Sağlık Açısından Önemi
Vücudunuzdaki her hücre, reaksiyonları hızlandıran, enerjiyi depolayan ve genetik bilgiyi taşıyan küçük moleküller olan pürinlere bağımlıdır. Hızla bölünen kanser hücreleri özellikle pürinlere açtır ve genellikle bunların sentez yollarını yeniden düzenlerler. Bu çalışma, pürinleri sıfırdan inşa etmede kilit bir rol oynayan FGAMS adlı insan enzimi üzerine odaklanıyor. FGAMS’in üç boyutlu yapısını ve parçalarının nasıl hareket edip iletişim kurduğunu ortaya koyarak yazarlar, enzimin nasıl açılıp kapandığını ve tümörü yavaşlatmak için nasıl hedeflenebileceğini açığa çıkarıyorlar.
Yaşamın Yapıtaşları Kontrol Altında
Hücreler, enerji kullanan ve bir dizi enzim gerektiren zorlu bir montaj hattı olan de novo yoluyla pürinleri üretir; bu yol karmaşık bir halkayı birleştirir. FGAMS bu dizide dördüncü adımı gerçekleştirir ve bileşenleri verimli şekilde yönlendirmeye yardımcı olan purinosom adlı daha büyük bir enzim kümesinin merkezinde yer alır. Hızla büyüyen kanser hücreleri genellikle bu yolu güçlendirdiği için FGAMS gibi enzimler çekici ilaç hedefleridir: bunları engellemek, tümörleri ihtiyaç duydukları nükleotidlerden mahrum bırakırken sağlıklı hücreler geri dönüşüm yollarına güvenebilir.
Şekil Değiştiren Bir Moleküler Makine
FGAMS, her biri farklı bir işi yapan ve doğru sırayla işbirliği yapması gereken üç bağlı bölümden (domain) oluşur. Bir domain glutamin amino asidinden amonyağı keser, başka bir domain o amonyağı küçük bir şeker bazlı molekülü değiştirmek için kullanır ve üçüncü domain düzenleyici bir merkez görevi görür. Yüksek çözünürlüklü cryo-elektron mikroskobu kullanarak araştırmacılar FGAMS’i üç farklı çalışma halinde yakaladılar: bir enerji taşıyan molekül bağlıyken, kısa ömürlü bir ara ürün tuzaklanmışken ve birden çok substrat ile ara ürün aynı anda bulunurken. Bu durumların karşılaştırılması esnek döngülerin ve N-terminal “kolun” dramatik biçimde hareket ettiğini ve kimya ilerledikçe enzimi yeniden yapılandırdığını ortaya koydu.
Gizli Tünel ve Moleküler Kapılar
Önemli bir bilmece, bir domainde salınan amonyağın, uzak kullanım yerine zarar vermeden nasıl güvenli biçimde ulaştığıydı. Yeni yapılar, iki bölgeyi birbirine bağlayan daha önce görülmemiş bir iç tüneli ve belirli amino asitlerden oluşan bir dizi “kapıyı” açığa çıkarıyor. Uygun substratlar bağlandığında ve ara ürün oluştuğunda merkezi bir döngü düzenli bir konuma fırlıyor, N-terminal domaini çekiyor ve katalitik domaindeki yakın döngüleri yeniden düzenliyor. Bu koreografi, glutaminin işlenebilmesi için iki giriş kapısını açarken bağ kırılmasını sağlayan yüksek enerjili ara ürünü stabilize eden bir bölgeyi geçici olarak yeniden şekillendiriyor.
Hareket Yoluyla Kimyanın Bağlanması
Reaksiyon ilerledikçe enzim basitçe beklemez; her kimyasal adımı bir sinyal olarak kullanır. Amonyak üreten domainde kovalent bir tioester ara ürün oluştuğunda önceki hareketler kısmen tersine döner. Bu, merkezi döngünün gevşemesine ve kapıların kaçış yollarını kapatacak şekilde yeniden konumlanmasına neden olurken tünelin her iki ucundaki iki ek kapı açılır. Bir avuç “darboğaz” kalıntısında meydana gelen ince kaymalar, iç geçidi genişleterek bir amonyak molekülünün tünelden doğrudan ikinci aktif bölgeye seyahat etmesine izin verir; burada tuzaklanmış ara ürünle reaksiyona girerek son ürünü üretir. Kapı kalıntıları mutasyona uğradığında amonyak sızar veya reaksiyonun iki yarısı birbirinden ayrılır; bu da bu kapılama ve kanal sisteminin verimli kataliz için zorunlu olduğunu doğrular.
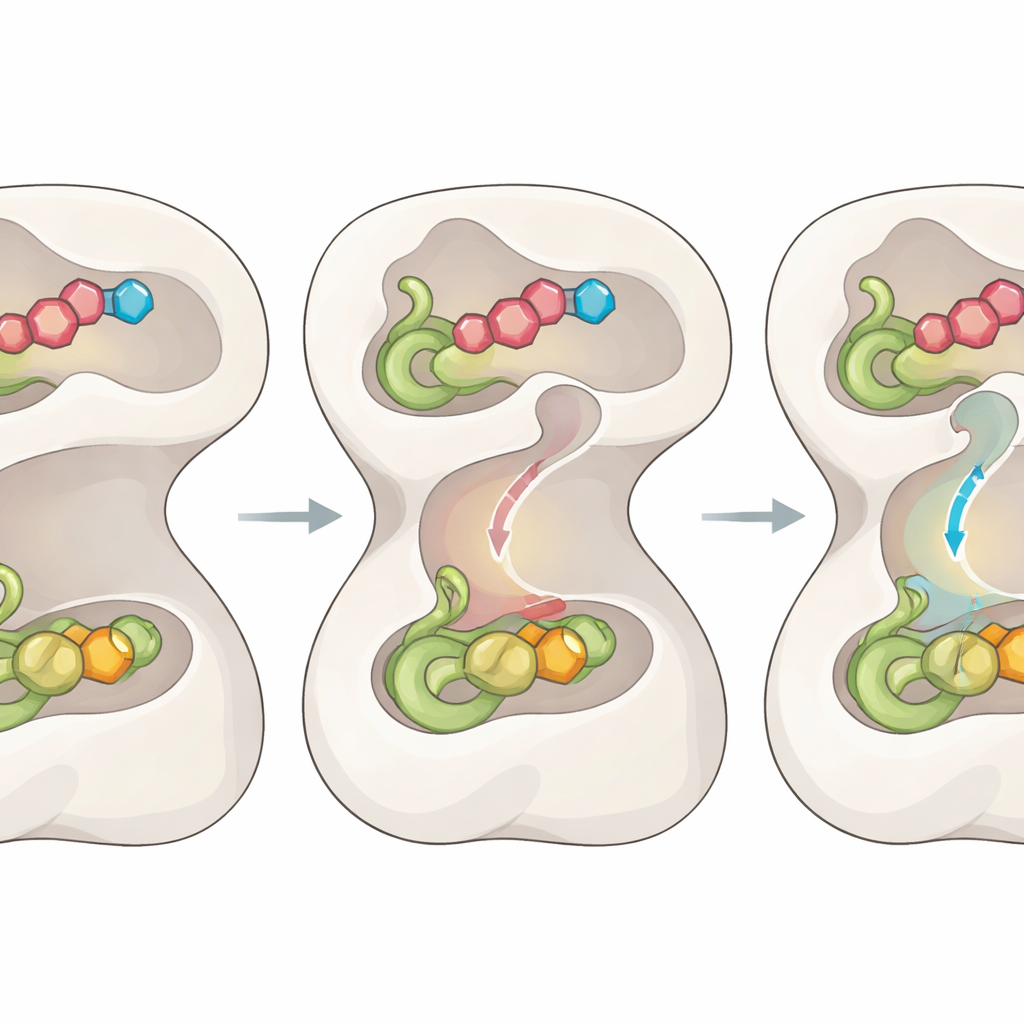
Yapısal İçgöründen Terapötik Yollara
FGAMS’i katalitik döngüsü boyunca izleyerek çalışma, domain hareketlerinin, esnek döngülerin, iç kapıların ve geçici bir tünelin kimyayı koordine etmek için nasıl bir araya bağlandığını ayrıntılı biçimde ortaya koyuyor. Genel olarak söylenecek en önemli nokta, enzimin küçük bir programlanabilir fabrika gibi davranmasıdır: yalnızca tüm doğru parçalar yerinde olduğunda kapılarını ve iç konveyörünü açar; bu da hız ve güvenliği sağlar. FGAMS pürin üretimini desteklediği ve karaciğer tümörlerinde kötü sağkalım ile ilişkili olduğu için yapısal planlar ve yeni tanımlanan kontrol noktaları, tüneli tıkayan, kapıları donduran veya kilit ara ürünleri tuzağa düşüren ilaçlar tasarlamak için birden çok yaklaşım sunar; bu da hedefe yönelik yeni bir antikanser ilaç sınıfı ortaya çıkarabilir.
Atıf: Sharma, N., Zhou, W. & French, J.B. Structural and molecular basis for allosteric regulation and catalytic coupling of human phosphoribosylformylglycinamidine synthase. Nat Commun 17, 2732 (2026). https://doi.org/10.1038/s41467-026-69423-y
Anahtar kelimeler: pürin biyosentezi, allosterik düzenleme, amonyak kanallama, kanser metabolizması, kryo-EM yapı