Clear Sky Science · tr
Amiloid-β fibrillerindeki yapısal kusurlar ikincil nükleasyonu tetikliyor
Beyin proteinlerindeki küçük kusurlar neden önemli?
Alzheimer ve ilişkili beyin hastalıklarında belirli proteinler, amiloid fibriller adı verilen uzun, ipliksi yapılar halinde kümelenir. Bu fibriller yalnızca hastalığın işareti olmakla kalmaz; aynı zamanda beyinde hasara yol açabilen yeni, yüksek derecede toksik protein parçacıklarının oluşumunu da tetiklerler. Bu çalışma basit ama etkili bir soruyu ortaya koyuyor: amiloid fibrillerin içindeki nadir yapısal “kusurlar”, yeni zararlı büyümeyi başlatan ana sıcak noktalar mı? Cevap, tüm bir protein yüzeyini hedeflemek yerine sadece birkaç kritik bölgeyi hedefleyerek bu bozuklukları yavaşlatma veya durdurma yollarına işaret edebilir. 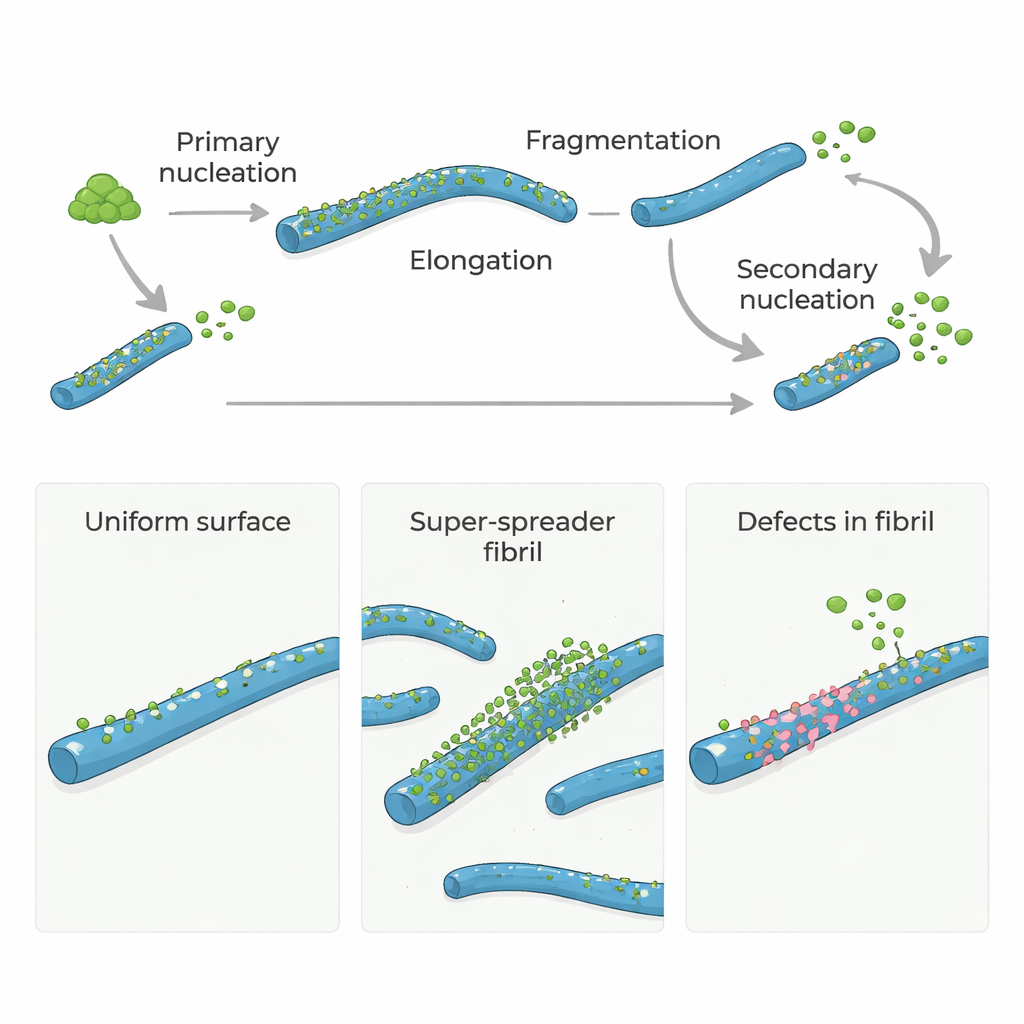
Sessiz proteinden kontrolsüz zincir reaksiyonuna
Alzheimer hastalığında merkezi rol oynayan Amiloid‑β (Aβ) proteinleri normalde kendi başlarına hızla kümelenmezler. Başlamak için birkaç monomerin yavaşça ilk küçük fibrilleri oluşturması gerekir; bu adıma primer nükleasyon denir. Bu ilk fibriller oluştuğunda, daha fazla monomer uçlarına eklenerek hızla büyürler. Daha da önemlisi, mevcut fibriller yüzeylerinde yeni fibrillerin ortaya çıkmasını tetikleyebilir; buna ikincil nükleasyon denir. Yüzey kaynaklı bu adım, sistemi yeni fibrillerle ve küçük, toksik oligomerlerle doldurabilir ve yavaş bir damlamayı kontrolsüz bir zincir reaksiyonuna dönüştürebilir.
Tüm fibril yüzeyleri eşit derecede tehlikeli mi?
Birçok model, bir amiloid fibrilinin tüm yüzeyinin ikincil nükleasyonu katalize etme konusunda eşit derecede yetenekli olduğunu varsaymıştır. Ancak son deneyler yalnızca küçük bir yüzey fraksiyonunun gerçekten aktif olduğunu ima etmişti. Bunu araştırmak için yazarlar, Aβ40 ve Aβ42’nin ikincil nükleasyonunu engellediği bilinen doğal bir moleküler “şaperon” olan Brichos’u kullandılar. Fluoresan ile etiketlenmiş Brichos’un fibrillere ne kadar yapıştığını dikkatle ölçerek, Brichos’un güçlü bağlandığını fakat çok düşük sayılarda bağlandığını buldular: bir fibrilde yaklaşık her 100–150 Aβ molekülüne bir Brichos molekülü. Buna rağmen bu seyrek örtü, ikincil nükleasyonun %90’ından fazlasını baskılamak için yeterliydi; bu da yeni toksik yapıları üretenin tüm yüzey değil, nadir ve lokalize bölgeler olduğunu gösteriyor.
Gizli kusurların rolünü araştırmak
Bu bulgular, kritik nükleasyon bölgelerinin fibriller büyürken oluşan küçük düzensizlikler—hizalanmamış katmanlar veya kısmen açığa çıkmış iç çekirdekler gibi yapısal kusurlar—olabileceğini öne sürdü. Bu fikri doğrudan test etmek için araştırmacılar Aβ40 fibrillerini iki farklı koşulda büyüttüler. Bir grup, hızlı büyümeyi ve kusurların kinetik kapanmasını teşvik eden tipik, güçlü doygunluk üstü (süpersaturasyon) koşullarında oluşan “kontrol” fibrilleri idi. Diğer grup ise yavaş, sıcaklık kontrollü bir tavlama (annealing) protokolü kullanılarak oluşturuldu: fibriller çok düşük etkin itici kuvvette, çözünebilirlik limitlerine yakın koşullarda büyütüldü; böylece yanlış yapılar kilitlenmeden önce eriyebilir veya onarılabilirdi. Yüksek çözünürlüklü kriyo-elektron mikroskobu, her iki fibril setinin genel şekil ve burulma açısından özde aynı göründüğünü gösterdi; bu da tavlama işleminin temel morfolojiyi değiştirmediğini işaret ediyor. 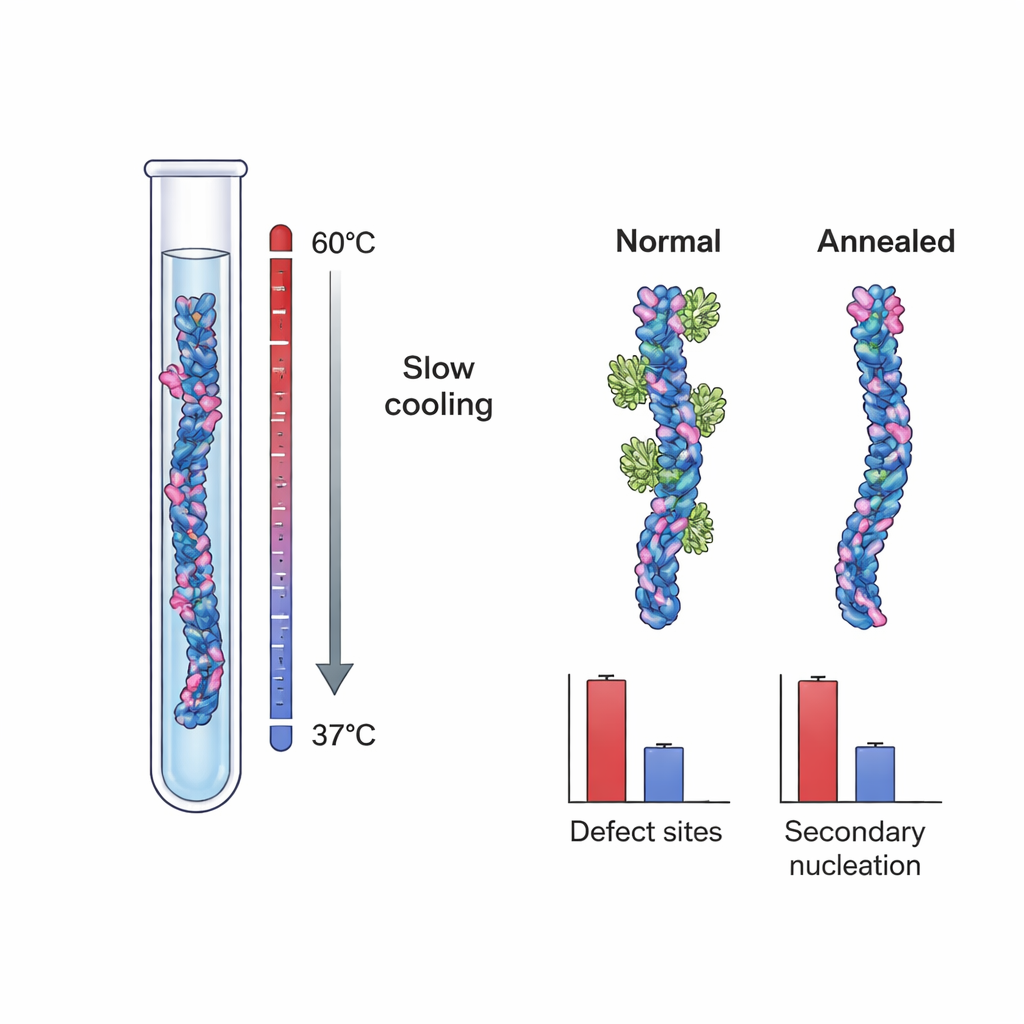
Daha az kusur, daha az tehlikeli büyüme noktası
Grup bu iki fibril tipine Brichos bağlanmasını ölçtüğünde çarpıcı bir fark buldu. Kontrol Aβ40 fibrilleri yaklaşık her ~100 monomere bir Brichos bağlanma sitesi gösteriyordu; bu yine nadir ama önemli bölgeleri işaret ediyordu. Ancak tavlanmış fibrillerde bu oran yaklaşık her ~800 monomere bir siteydi—site sıklığında neredeyse %90’lık bir azalma. Bu fibriller taze Aβ40 çözeltilerine “tohum” olarak eklendiğinde, tavlanmış fibriller yeni agregasyonu tetikleme konusunda, toplam kütleleri kontrol fibrilleriyle eşleştirildiğinde bile çok daha az etkiliydi. Ayrıntılı kinetik modelleme, bu tohumlama gücündeki düşüşün yalnızca fibril uzunluğundaki farklılıklarla açıklanamayacağını gösterdi. Bunun yerine, düşüş nicel olarak Brichos bağlanma sitesi sayısındaki azalma ile uyumluydu ve büyüme kusurlarının ikincil nükleasyonun ana motorları olduğu fikrini güçlü biçimde destekledi.
Terapötik vaat taşıyan genel bir ilke
Termodinamik argümanları, önceki çalışmaların yeniden analizini ve birkaç amiloid oluşturan protein arasındaki karşılaştırmaları birleştirerek, yazarlar nadir büyüme kusurlarının yalnızca Alzheimer ile ilişkili Aβ’de değil, birçok sistemde ikincil nükleasyonun merkezinde olma olasılığının yüksek olduğunu savunuyor. Bu kusurlar fibrilin sıkıca paketlenmiş iç çekirdeğini kısmen açığa çıkarır ve yeni oligomerlerin ve fibrillerin düzgün bir yüzeye kıyasla çok daha kolay oluşabileceği hazır bir iskelenme sağlar. Bu kusurları ana suçlular olarak tanımak ilaç tasarımı için yeni yollar açar. Bir fibril yüzeyindeki tüm etkileşimleri engellemeye çalışmak yerine, terapiler bu nadir kusur bölgelerini örtmeyi veya onarmayı ya da bunların oluştuğu koşulları azaltmayı hedefleyebilir. Pratikte bu, beyindeki amiloid oluşturan proteinlerin etkin konsantrasyonunu düşürmek veya Brichos’tan ilham alan, kusur kaynaklı nükleasyon sıcak noktalarını tanıyan ve nötralize eden moleküller tasarlamak anlamına gelebilir. Başarılı olursa, bu tür stratejiler toksik oligomerlerin ana kaynağını kesebilir ve amiloid bağlantılı hastalıkların ilerlemesini yavaşlatabilir.
Atıf: Hu, J., Scheidt, T., Thacker, D. et al. Structural defects in amyloid-β fibrils drive secondary nucleation. Nat Commun 17, 1933 (2026). https://doi.org/10.1038/s41467-026-69377-1
Anahtar kelimeler: amiloid fibriller, Alzheimer hastalığı, ikincil nükleasyon, protein agregasyonu, Brichos şaperon